Aktif maddeler: Adalimumab
Pediatrik kullanım için HUMIRA 40 mg / 0.8 ml enjeksiyonluk çözelti
Paket boyutları için Humira prospektüsleri mevcuttur:- Pediatrik kullanım için HUMIRA 40 mg / 0.8 ml enjeksiyonluk çözelti
- Kullanıma hazır şırıngada HUMIRA 40 mg enjeksiyonluk çözelti
- HUMIRA 40 mg enjeksiyonluk çözelti, iğne güvenlik cihazı ile kullanıma hazır enjektörde
- Kullanıma hazır kalem içinde Humira 40 mg enjeksiyonluk çözelti
Humira neden kullanılır? Bu ne için?
Humira, seçici bir bağışıklık baskılayıcı ajan olan adalimumab etkin maddesini içerir. Humira, 2-17 yaş arası çocuklarda poliartiküler jüvenil idiyopatik artrit, 6-17 yaş arası çocuklarda entezit ile ilişkili artrit, 6-17 yaş arası Crohn hastalığı, 17 yaş ve 4 ila 4 yaş arası çocuklarda plak psoriazis tedavisinde endikedir. 17 yıl. Bu hastalıkların iltihaplanma sürecini azaltan bir ilaçtır. Etkin madde, adalimumab, hücre kültürleri tarafından üretilen bir insan monoklonal antikorudur. Monoklonal antikorlar, diğer proteinleri tanıyan ve onlara bağlanan proteinlerdir. Adalimumab, poliartiküler jüvenil idiyopatik artrit, entezit ile ilişkili artrit, Crohn hastalığı ve plak sedef hastalığı gibi inflamatuar hastalıklarda yüksek seviyelerde bulunan spesifik bir proteine (tümör nekroz faktörü veya TNFa) bağlanır.
Poliartiküler jüvenil idiyopatik artrit ve entezit ile ilişkili artrit
Poliartiküler jüvenil idiyopatik artrit ve entezit ile ilişkili artrit inflamatuar hastalıklardır. Humira, poliartiküler jüvenil idiyopatik artrit ve entezit ile ilişkili artrit tedavisinde kullanılır. Metotreksat gibi hastalığı modifiye edici ilaçlar tanı anında verilebilir. Bu ilaçlara yanıt yeterli değilse, çocuğa poliartiküler jüvenil idiyopatik artrit veya entezit ile ilişkili artrit tedavisi için Humira verilecektir.
Çocuklarda Crohn hastalığı
Crohn hastalığı, sindirim sisteminin inflamatuar bir hastalığıdır. Humira, 6 ila 17 yaş arası çocuklarda Crohn hastalığının tedavisi için endikedir. Çocuğa önce başka ilaçlar verilir. Çocuğunuz bu ilaçlara yeterince iyi yanıt vermezse, Crohn hastalığının belirti ve semptomlarını azaltmak için ona HUMIRA verilecektir.
Pediatrik plak sedef hastalığı
Plak sedef hastalığı, gümüşi pullarla kaplı kırmızımsı, pullu, sertleşmiş cilt lekelerine neden olan bir cilt rahatsızlığıdır. Sedef hastalığının, vücudun bağışıklık sistemindeki cilt hücrelerinin üretiminin artmasına neden olan bir sorundan kaynaklandığı düşünülmektedir. Humira, topikal terapi ve fototerapinin optimal olarak işe yaramadığı veya endike olmadığı 4-17 yaş arası çocuklarda ve ergenlerde şiddetli plak sedef hastalığını tedavi etmek için kullanılır.
Kontrendikasyonlar Humira ne zaman kullanılmamalıdır?
Humira'yı kullanmayınız.
- Çocuğunuzun adalimumab'a veya bu ilacın diğer bileşenlerinden herhangi birine alerjisi varsa (bölüm 6'da listelenmiştir).
- "Aktif tüberküloz dahil ciddi bir enfeksiyonunuz varsa ("Uyarılar ve Önlemler" bölümüne bakın).ateş, yaralar, yorgunluk hissi, diş problemleri.
- Orta veya şiddetli kalp yetmezliği varlığında. Ciddi bir kalp rahatsızlığı olup olmadığını doktorunuza söylemeniz önemlidir ("Uyarılar ve Önlemler" bölümüne bakınız).
Kullanım Önlemleri HUMIRA'yı kullanmadan önce dikkat edilmesi gerekenler
Humira'yı kullanmadan önce çocuğunuzun doktoru veya eczacısı ile konuşunuz.
- Göğüste sıkışma, hırıltılı solunum, baş dönmesi, şişme veya kızarıklık gibi semptomlarla birlikte herhangi bir alerjik reaksiyonunuz varsa, HUMIRA'yı vermeyi bırakın ve derhal doktorunuzla iletişime geçin.
- Uzun süreli veya lokalize enfeksiyonlar (örneğin bacak ülserleri) dahil bir enfeksiyonunuz varsa, HUMIRA ile tedaviye başlamadan önce doktorunuza danışın.Emin değilseniz, doktorunuzla iletişime geçin.
- Humira ile tedavi olurken enfeksiyonlara daha kolay yakalanabilirsiniz. Bebeğin akciğer fonksiyonu bozulursa bu risk artabilir. Bu enfeksiyonlar ciddi olabilir ve tüberküloz, virüslerin, mantarların, parazitlerin veya bakterilerin neden olduğu enfeksiyonları veya diğer fırsatçı enfeksiyonları ve nadir durumlarda yaşamı tehdit edebilen sepsisi içerir. Ateş, yaralar, yorgunluk veya diş problemleri gibi belirtileri doktorunuza söylemeniz önemlidir. Doktorunuz Humira'yı geçici olarak durdurmanızı önerebilir.
- Humira alan hastalarda tüberküloz vakaları bulunduğundan, doktorun Humira tedavisine başlamadan önce çocuğun tipik tüberküloz belirtileri veya semptomları olup olmadığını kontrol etmesi gerekecektir. Bu, çocuğun tıbbi geçmişi ve uygun klinik testleri (örn. göğüs röntgeni ve tüberkülin testi) dahil olmak üzere ayrıntılı bir tıbbi değerlendirmenin toplanmasını içerecektir.Bu tür testlerin performansı ve sonuçları Hasta için Uyarı Kartına kaydedilmelidir. Çocuğun daha önce tüberküloz geçirip geçirmediğini veya tüberküloz hastalarıyla yakın teması olup olmadığını doktora söylemek çok önemlidir. Çocuk tüberküloz için önleyici tedavi görmüş olsa bile tedavi sırasında tüberküloz oluşabilir. Tedavi sırasında veya sonrasında tüberküloz semptomları (sürekli öksürük, kilo kaybı, halsizlik, orta dereceli ateş) veya başka enfeksiyonlar ortaya çıkarsa derhal doktorunuza başvurun.
- Çocuğunuz histoplazmoz, koksidiyomikoz veya blastomikoz gibi mantar enfeksiyonlarının endemik olduğu bölgelerde yaşıyorsa veya bu bölgelere seyahat ediyorsa doktorunuza söyleyin.
- Çocuğunuzun tekrarlayan enfeksiyonları olup olmadığını veya enfeksiyon riskini artıran durumları olup olmadığını doktorunuza söyleyin.
- Çocuğunuzun hepatit B virüsü (HBV) taşıyıcısı olup olmadığını, aktif bir hepatit B virüsü enfeksiyonu olup olmadığını veya hepatit B virüsüne yakalanma riski altında olabileceğini düşünüyorsanız, doktorunuza söyleyin. Doktor çocuğu hepatit için test etmelidir. B virüsü enfeksiyonu Humira almak, bu virüsü taşıyan kişilerde hepatit B virüsünün yeniden aktif hale gelmesine neden olabilir. Bazı nadir durumlarda, özellikle hasta bağışıklık sistemini baskılayan başka ilaçlarla tedavi görüyorsa, hepatit B virüsünün yeniden etkinleştirilmesi yaşamı tehdit edebilir.
- Ateş, yara, yorgunluk veya diş problemleri gibi enfeksiyon belirtileri ortaya çıkarsa, çocuğunuzun doktoruna söylemeniz önemlidir.
- Ameliyattan veya dişçilik işlemlerinden önce doktorunuza çocuğunuzun HUMIRA aldığını söyleyin. Doktorunuz geçici olarak askıya alınmasını önerebilir.
- Çocuğunuzun multipl skleroz gibi demiyelinizan hastalıkları varsa, doktor Humira'ya başlanıp başlanmayacağına karar verecektir.
- Bazı aşılar enfeksiyonlara neden olabilir ve Humira ile tedavi edilirken verilmemelidir. Çocuğunuza herhangi bir aşı yapmadan önce doktorunuza danışın. Çocuklarda, mümkünse, Humira tedavisine başlamadan önce mevcut aşılama kılavuzlarına uygun olarak planlanan aşılama programının uygulanması önerilir. HUMIRA'yı hamileliğiniz sırasında aldıysanız, hamilelik sırasında aldığınız son dozdan yaklaşık 5 ay sonrasına kadar bebeğinizin bu enfeksiyona yakalanma riski artabilir. Hamilelik sırasında, bebeğinizin herhangi bir aşı türünü ne zaman alması gerektiğine karar verebilirler.
- Hafif kalp yetmezliği ve eş zamanlı HUMIRA tedavisi durumunda, doktorun bebeğin kalbinin durumunu dikkatle değerlendirmesi ve izlemesi gerekecektir. Geçmişteki ve şimdiki herhangi bir kalp problemini doktorunuza söylemeniz önemlidir. Yeni kalp yetmezliği semptomları ortaya çıkarsa veya mevcut semptomlar kötüleşirse (örneğin, nefes darlığı veya ayaklarda şişme), derhal doktorunuza başvurun. Çocuğun Humira'yı alıp alamayacağına doktor karar verecektir.
- Bazı hastalarda vücut, enfeksiyonla savaşmak veya kanamayı durdurmak için yeterli kan hücresi üretemeyebilir. Çocuğunuzda kalıcı ateş, kolayca morarma veya kanama veya solgunluk varsa hemen doktorunuza başvurun. İkincisi tedaviyi bırakmaya karar verebilir.
- Hem çocuklarda hem de yetişkinlerde, Humira veya diğer anti-TNF ilaçları ile tedavi gören hastalarda bazı tümör türleri çok nadiren ortaya çıkmıştır. Uzun süreli şiddetli romatoid artritli hastalarda lenfoma (lenf sistemini etkileyen bir kanser türü) ve lösemi (kan ve kemik iliğini etkileyen bir kanser türü) gelişme riski ortalamadan daha yüksek olabilir. Çocuğunuz HUMIRA alırsa, lenfoma, lösemi veya diğer kanserlere yakalanma riski artabilir. Nadir durumlarda, Humira alan hastalarda spesifik ve şiddetli bir lenfoma tipi gözlenmiştir. Bu hastalardan bazıları ayrıca azatioprin veya 6-merkaptopurin tedavisi görüyordu. HUMIRA ile birlikte azatioprin veya 6-merkaptopurin alıyorsanız doktorunuza söyleyiniz. Ek olarak, Humira alan hastalarda melanotik olmayan cilt kanseri vakaları gözlenmiştir. Tedavi sırasında veya sonrasında yeni cilt lezyonları ortaya çıkarsa veya mevcut lezyonların görünümü değişirse lütfen doktorunuza bildirin.
- Başka bir anti-TNF ile tedavi edilen Kronik Obstrüktif Akciğer Hastalığı (KOAH) adı verilen belirli bir akciğer hastalığı tipine sahip hastalarda lenfomaya ek olarak malignite vakaları olmuştur. Çocuğunuzun KOAH'ı varsa veya çok sigara içiyorsa, bir anti-TNF tedavisinin uygun olup olmadığını doktorunuzla görüşmelisiniz.
Çocuklar ve ergenler
- Aşılar: Mümkünse, çocuğunuzun Humira'yı kullanmadan önce tüm aşılarını yaptırmış olması gerekir.
- 2 yaşından küçük poliartiküler jüvenil idiyopatik artritli çocuklara HUMIRA vermeyin.
Etkileşimler Hangi ilaçlar veya yiyecekler HUMIRA'nın etkisini değiştirebilir?
Diğer ilaçlar ve Humira
Çocuğunuz başka ilaçlar alıyorsa, yakın zamanda aldıysa veya alacaksa, çocuğunuzun doktoruna veya eczacısına söyleyin.
HUMIRA, metotreksat veya diğer hastalık modifiye edici antiromatizmal ilaçlar (sülfasalazin, hidroksiklorokin, leflunomid ve parenteral altın tuzları), steroidler veya steroidal olmayan antienflamatuar ilaçlar (NSAID'ler) dahil olmak üzere analjeziklerle birlikte alınabilir.
Humira, aktif bileşen olarak anakinra veya abatacept içeren ilaçlarla birlikte alınmamalıdır. Emin değilseniz, doktorunuza sorun.
Yiyecek ve içecek ile Humira
Humira deri altına (deri altına) enjekte edildiğinden yiyecek ve içecekler Humira'yı etkilemez.
Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme
HUMIRA'nın hamile kadınlarda etkileri bilinmemektedir, bu nedenle HUMIRA'nın hamile kadınlarda kullanımı önerilmemektedir. Humira ile tedavi sırasında ve tedaviden sonra en az 5 ay boyunca yeterli kontrasepsiyon kullanılarak hamilelikten kaçınılması önerilir. "Son ilaç tedavisi Bebeğiniz hamile kalırsa, bebeğin doktorunu görmelisiniz.
Adalimumabın anne sütüne geçip geçmediği bilinmemektedir.
Humira alan kişi emziren genç bir kadınsa, Humira tedavisi sırasında ve Humira ile son tedavisinden sonra en az 5 ay emzirmeyi bırakmalıdır. HUMIRA'yı hamilelik sırasında aldıysanız, bebeğinizin enfeksiyon kapma riski artabilir.Bebeğiniz herhangi bir ilaç almadan önce, hamilelik sırasında HUMIRA kullanımınızı çocuk doktorunuza veya başka bir sağlık uzmanına söylemeniz önemlidir. (daha fazla bilgi için aşı bölümüne bakınız).
Kızınızın hamile kalmaya başladığından veya hamile kalmayı planladığından şüpheleniyorsanız, bu ilacı kullanmadan önce doktorunuza veya eczacınıza danışınız.
Araç ve makine kullanma
Humira, araç kullanma, bisiklete binme veya makine kullanma becerisini az da olsa etkileyebilir. Humira'yı aldıktan sonra görme bozuklukları ve çevrenizin döndüğü hissi olabilir.
Dozaj ve kullanım yöntemi Humira nasıl kullanılır: Dozaj
Bu ilacı her zaman tam olarak çocuğunuzun doktoru veya eczacısının size söylediği şekilde kullanın. Şüpheniz varsa, çocuğunuzun doktoruna veya eczacısına danışın.
Poliartiküler jüvenil idiyopatik artritli çocuklar
2 ila 12 yaş arasındaki poliartiküler jüvenil idiyopatik artrit hastaları için önerilen HUMIRA dozu çocuğun boyuna ve kilosuna bağlıdır.Çocuğunuzun doktoru size doğru doz konusunda tavsiyede bulunacaktır.Poliartiküler jüvenil idiyopatik artrit hastaları için önerilen HUMIRA dozu 13-17 yaş arası iki haftada bir 40 mg'dır.
Entezit ile ilişkili artritli çocuklar
6 ila 17 yaşları arasındaki entezit ile ilişkili artritli hastalar için önerilen HUMIRA dozu, çocuğun boyuna ve kilosuna bağlıdır.
Crohn hastalığı olan çocuklar veya ergenler
40 kg'ın altındaki çocuklar veya ergenler:
Olağan doz rejimi başlangıçta 40 mg, ardından iki hafta sonra 20 mg'dır.Daha hızlı bir yanıt gerekirse, doktor 80 mg'lık bir başlangıç dozu (bir günde iki enjeksiyon olarak) ve ardından iki hafta sonra 40 mg'lık bir başlangıç dozu reçete edebilir. Bundan sonra, olağan doz iki haftada bir 20 mg'dır.Çocuğun yanıtına bağlı olarak, doktor doz sıklığını haftada bir 20 mg'a çıkarabilir.
40 kg veya daha ağır olan çocuklar veya ergenler:
Olağan doz rejimi başlangıçta 80 mg, ardından iki hafta sonra 40 mg'dır.Daha hızlı bir yanıt gerekirse, doktor 160 mg'lık bir başlangıç dozu reçete edebilir (günde 4 enjeksiyon veya 2 kez günde 2 enjeksiyon şeklinde). ardışık günler) ardından iki hafta sonra 80 mg. Daha sonra, normal doz iki haftada bir 40 mg'dır. Çocuğun yanıtına bağlı olarak, doktor doz sıklığını 40 mg'a çıkarabilir Tam doz 40 mg HUMIRA reçete edilen hastalar için, 40 mg kalem ve 40 mg kullanıma hazır şırınga da mevcuttur.
Sedef hastalığı olan çocuklar veya ergenler
4 ila 17 yaş arası plak sedef hastalığı olan hastalar için önerilen HUMIRA dozu çocuğunuzun ağırlığına bağlıdır. Çocuğunuzun doktoru, kullanmanız gereken doğru doz konusunda size tavsiyede bulunacaktır.
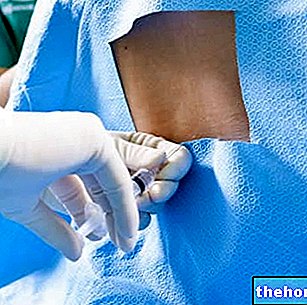
Uygulama yöntemi ve yolu
Humira deri altına enjeksiyonla (deri altı enjeksiyonla) verilir.
Humira'nın hazırlanması ve enjekte edilmesi için talimatlar:
Aşağıdaki talimatlar HUMIRA'nın nasıl enjekte edileceğini açıklamaktadır. Talimatları dikkatlice okuyun ve adım adım izleyin. Kendi kendine uygulama tekniği ve çocuğunuza ne kadar vereceğiniz konusunda doktorunuz veya asistanı tarafından bilgilendirileceksiniz.İlacı nasıl hazırlayacağınızı ve uygulayacağınızı anladığınızdan emin olana kadar enjekte etmeyin. Uygun talimatlardan sonra enjeksiyon sizin tarafınızdan veya bir aile üyesi veya arkadaş gibi başkaları tarafından yapılabilir.
Aşağıdaki talimatların açıklandığı gibi izlenmemesi, kontaminasyona neden olabilir ve bu da bebekte enfeksiyona neden olabilir. Şırınganın içeriği aynı şırınga veya flakon içinde başka ilaçlarla karıştırılmamalıdır.
1) Hazırlık
- Dozunuz için gereken uygun miktarı (hacimi) bildiğinizden emin olun. Miktarı bilmiyorsanız, DURDURUN ve daha fazla talimat için doktorunuzla iletişime geçin.
- Keskin nesneler için veya hemşireniz, doktorunuz veya eczacınız tarafından belirtildiği gibi özel bir atık kabına ihtiyacınız olacak.Kabı çalışma yüzeyinizin üzerine yerleştirin.
- Ellerinizi iyice yıkayın.
- Bir şırınga, bir flakon adaptörü, bir flakon, 2 alkollü bez ve bir iğne içeren bir kutuyu kartondan çıkarın.Kartonda bir sonraki uygulamanız için kullanmak üzere ikinci bir kutu varsa hemen buzdolabına geri koyun.
- Karton üzerindeki son kullanma tarihini kontrol edin. Son kullanma tarihinden sonra kutudaki herhangi bir öğeyi KULLANMAYIN.
- Aşağıdaki öğeleri, henüz ambalajlarından herhangi bir öğeyi ÇIKARMADAN, temiz bir yüzeye yerleştirin. Bir adet 1 ml şırınga Bir flakon adaptörü Bir pediatrik enjeksiyonluk Humira solüsyonu flakonu İki alkol pedi veya Bir iğne
- Humira berrak, renksiz bir sıvıdır. Sıvı opaksa, rengi bozulmuşsa veya içinde topaklanma veya partikül varsa KULLANMAYIN.
2) Enjeksiyon için Humira dozunun hazırlanması
Genel Talimatlar: Enjeksiyon tamamlanana kadar hiçbir öğeyi ATMAYIN.
- Paketi şırınganın sarı konektörüne en yakın ucundan kısmen açarak iğneyi hazırlayın. Paketi, sarı şırınga konektörünü ortaya çıkaracak kadar açın. Paketi, hafif tarafı yukarı bakacak şekilde yerleştirin.
- Şişe tıpasının üst kısmını görene kadar plastik kapağı şişeden çıkarın.
- Şişe kapağını temizlemek için alkollü bezlerden birini kullanın. Swab ile temizledikten sonra flakon kapağına DOKUNMAYIN.
- Kapağı, paketinden çıkarmadan flakon adaptör paketinden çıkarın.
- Şişeyi kapağı ters olacak şekilde tutun.
- Orak adaptörü şeffaf ambalajdayken, adaptör tık sesi gelene kadar iterek flakon tıpasına takın.
- Adaptörün flakona takılı olduğundan emin olduğunuzda, paketi flakondan dışarı doğru çekiniz.
- Şişeyi ve adaptörü, düşürmemeye dikkat ederek temiz bir çalışma yüzeyine nazikçe yerleştirin.Adaptöre DOKUNMAYIN.
- Ambalajı beyaz pistona en yakın uçtan kısmen açarak şırıngayı hazırlayın.
- Şeffaf paketi, şırıngayı paketinden çıkarmadan beyaz pistonu açığa çıkaracak kadar açın.
- Şırınga paketini tutarak, pistonu, belirtilen dozun 0.1 ml üzerinde YAVAŞÇA dışarı çekin (örneğin, reçete edilen doz 0,5 ml ise, pistonu 0,6 ml'ye itin). Öngörülen doz ne olursa olsun, 0,9 ml'ye karşılık gelen konumu ASLA aşmayın.
- Hacim, sonraki bir adımda öngörülen doza kadar ayarlanacaktır.
- Beyaz pistonu şırıngadan tamamen dışarı itmeyin.
NOT: Beyaz piston şırıngadan tamamen dışarı itilmişse şırıngayı atın ve değiştirme için Humira tedarikçinizle iletişime geçin. Beyaz pistonu tekrar takmaya ÇALIŞMAYIN.
- Şırıngayı ambalajından çıkarmak için beyaz pistonu KULLANMAYIN. Şırıngayı dereceli tarafından tutun ve paketinden çıkarın. Şırıngayı hiçbir zaman yere BIRAKMAYIN.
- Adaptörü tutarken, şırınganın ucunu adaptöre sokun ve şırıngayı durana kadar bir elinizle saat yönünde çevirin.
- Şişeyi tutarken beyaz pistonu sonuna kadar itin. Bu adım, doğru dozu almak için önemlidir. Beyaz piston çubuğunu tutun ve flakonu ve şırıngayı ters çevirin.
- Beyaz pistonu, belirtilen dozun 0.1 ml üzerine YAVAŞÇA çekin. Uygun dozu geri çekmek önemlidir. Reçete edilen doza eşdeğer hacim, Dozun Hazırlanması adım 4'te belirlenecektir. Öngörülen doz 0,5 ml ise, beyaz pistonu 0,6 ml hacme çekin. Sıvı flakondan şırıngaya geçecektir.
- Sıvıyı şişeye geri itmek için beyaz pistonu sonuna kadar itin. Beyaz pistonu yeniden YAVAŞÇA, belirtilen dozun 0,1 ml üzerine ulaşana kadar çekin; uygun dozun geri çekilmesi ve sıvı veya boş boşluklarda hava kabarcıklarının oluşmasının önlenmesi önemlidir.Reçete edilen doza eşdeğer hacim 4. adımda, Dozun Hazırlanmasında belirlenecektir.
- Şırıngada hava kabarcığı veya boşluk kalırsa, bunu üç defaya kadar tekrarlayabilirsiniz.Şırıngayı sallamayın.
NOT: Beyaz piston şırıngadan tamamen dışarı itilmişse şırıngayı atın ve değiştirme için Humira tedarikçinizle iletişime geçin. Beyaz pistonu tekrar takmaya ÇALIŞMAYIN.
- Şırıngayı dereceli tarafından hala dik tutarken, diğer elinizle adaptörü çevirerek flakon adaptörünü çıkarın.Flakon adaptörünü şırıngadan çıkardığınızdan emin olun. Şırınganın ucuna DOKUNMAYIN.
- Şırınga ucunun yakınında büyük bir hava kabarcığı veya boş alan fark ederseniz, sıvı şırınga ucuna girmeye başlayana kadar beyaz pistonu YAVAŞÇA şırınganın içine itin. Doz konumunu geçtikten sonra beyaz pistonu İTMEYİN.
- Örneğin, reçete edilen doz 0,5 ml ise, beyaz pistonu 0,5 ml konumunu geçmeyecek şekilde itmeyin.
- Şırıngada kalan sıvının en azından çekilen doza eşdeğer olduğunu doğrulayın. Daha düşükse şırıngayı KULLANMAYIN ve sağlık uzmanınıza başvurun.
- Serbest elinizle sarı şırınga konektörü aşağı bakacak şekilde iğne paketini alın.
- Şırıngayı yukarıya bakacak şekilde tutarak, şırınga ucunu sarı konektöre sokun ve şırıngayı şekildeki okla gösterildiği gibi durana kadar döndürün.İğne şimdi şırıngaya takılıdır.
- İğneyi paketinden çıkarın, ancak şeffaf iğne kapağını ÇIKARMAYIN.
- Şırıngayı temiz bir çalışma yüzeyine yerleştirin. Uygulama yeri ve doz hazırlama adımlarına hemen devam edin.
3) Bir enjeksiyon bölgesinin seçimi ve hazırlanması
- Uyluğunuzda veya karnınızda bir nokta seçin: Son enjeksiyon için kullanılan aynı yeri KULLANMAYIN.
- Yeni enjeksiyon, son enjeksiyon yerinden en az 3 cm uzakta yapılmalıdır.
- Derinin kırmızı, morarmış veya sert olduğu bölgelere enjekte ETMEYİN Bu bir enfeksiyon belirtisi olabilir; bu nedenle doktorunuzla iletişime geçmelisiniz.
- Enfeksiyon kapma olasılığını azaltmak için enjeksiyon bölgesini diğer alkollü pamukla silin.Enjeksiyondan önce bölgeye tekrar DOKUNMAYIN.
4) Dozun hazırlanması
- İğne yukarı bakacak şekilde şırıngayı alın.
- Pembe iğne kapağını şırıngaya doğru çevirmek için diğer elinizi kullanın.
- Diğer elinizle yukarı çekerek şeffaf iğne kapağını çıkarın.
- İğne temiz.
- İğneye DOKUNMAYIN.
- Şeffaf iğne kapağı çıkarıldıktan sonra şırıngayı aşağı doğrultmayın.
- Şeffaf kapağı tekrar iğneye takmaya ÇALIŞMAYIN.
- Sıvı miktarını net bir şekilde görmek için şırıngayı iğne yukarı bakacak şekilde göz hizasında tutun.İlacı gözünüze kaçırmamaya dikkat edin.
- Aldığınız ilaç miktarını tekrar kontrol edin.
- Beyaz pistonu, şırınga reçete edilen ilaç miktarını içerene kadar şırınganın içine yavaşça itin. Piston basılıyken aşırı sıvı iğneden dışarı sızabilir.İğneyi veya şırıngayı ÇIKARMAYIN.
humira enjeksiyonu
- Serbest elinizle alkolle ovulmuş bölgeyi nazikçe alın ve sabit tutun.
- Diğer elinizle şırıngayı enjeksiyon bölgesine 45 ° açıyla tutun.
- Sert ve hızlı bir hareketle iğnenin tamamını deriye doğru itin.
- Elinizle deriyi bırakın.
- Şırınga boşalana kadar ilacı enjekte etmek için beyaz pistonu itin.
- Şırınga boşaldığında, iğneyi yerleştirildiği açıyla aynı açıda çekerek deriden çıkarın.
- Serbest elinizle alkolle ovulmuş bölgeyi nazikçe alın ve sabit tutun.
- Diğer elinizle şırıngayı enjeksiyon bölgesine 45 ° açıyla tutun.
- Sert ve hızlı bir hareketle iğnenin tamamını deriye doğru itin.
- Elinizle deriyi bırakın.
- Şırınga boşalana kadar ilacı enjekte etmek için beyaz pistonu itin.
- Şırınga boşaldığında, iğneyi soktuğunuz açıyla çekerek cildinizden çıkarın.
- Pembe iğne kapağını iğnenin üzerinden nazikçe yukarı çekin ve iterek açın ve iğneli şırıngayı çalışma yüzeyinize yerleştirin.Şeffaf kapağı iğneye geri KOYMAYIN.
- Bir parça gazlı bez ile enjeksiyon bölgesine 10 saniye boyunca basınç uygulayın. Biraz kanama olabilir. Enjeksiyon bölgesine masaj YAPMAYIN. İsterseniz bir yama uygulayın.
Malzemelerin bertarafı
- Keskin nesneler için bir kap gibi veya hemşireniz, doktorunuz veya eczacınız tarafından belirtildiği gibi özel bir atık kabına ihtiyacınız olacaktır.
- İğneli, flakonlu ve adaptörlü şırıngayı keskin nesneler için özel bir kaba koyun. Bu öğeleri ev çöp konteynerinize KOYMAYIN.
- Şırınga, iğne, flakon ve adaptör ASLA tekrar KULLANILMAMALIDIR.
- Bu kabı daima çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
- Ev çöp konteynerinizde kullanılan diğer tüm malzemeleri atın.
Aşırı doz Humira'yı çok fazla aldıysanız ne yapmalısınız?
Kullanmanız gerekenden daha fazla HUMIRA kullandıysanız:
Yanlışlıkla daha fazla HUMIRA enjekte ederseniz veya doktorunuzun size söylediğinden daha sık enjekte ederseniz, doktorunuza danışınız ve çocuğunuzun daha fazla ilaç kullandığını söyleyiniz.İlaç kutusunu veya flakonunu boş olsa bile daima saklayınız.
Kullanmanız gerekenden daha az HUMIRA kullandıysanız:
HUMIRA'yı yanlışlıkla daha az enjekte ederseniz veya çocuğunuzun doktoru veya eczacısının önerdiğinden daha az sıklıkla enjekte ederseniz, çocuğunuzun doktoru veya eczacısı ile iletişime geçin ve çocuğunuzun daha az ilaç aldığını söyleyin.İlaç kutusunu veya flakonunu boş olsa bile daima saklayınız.
HUMIRA'yı kullanmayı unutursanız:
Çocuğunuza HUMIRA enjeksiyonu yapmayı unutursanız, hatırladığı anda HUMIRA dozunu enjekte etmesi gerekir.Daha sonra çocuğa bir sonraki dozu öngörülen programa göre düzenli olarak verin.
Çocuğunuz HUMIRA almayı bırakırsa
HUMIRA kullanımına son verme kararı çocuğun doktoruyla görüşülmelidir.Çocuğun semptomları, tedavinin kesilmesinden sonra geri dönebilir. Bu ilacın kullanımıyla ilgili başka sorularınız varsa, doktorunuza veya eczacınıza sorunuz.
Yan Etkiler Humira'nın yan etkileri nelerdir?
Tüm ilaçlar gibi, bu ilaç da yan etkilere neden olabilir, ancak bunları herkes almayabilir. Çoğu yan etki hafif ila orta şiddettedir. Bununla birlikte, bazıları şiddetli olabilir ve tedavi gerektirebilir. Yan etkiler, son Humira enjeksiyonundan 4 ay sonrasına kadar ortaya çıkabilir.
Aşağıdaki reaksiyonlardan herhangi birini fark ederseniz hemen doktorunuza söyleyiniz:
- şiddetli deri döküntüsü, kurdeşen veya diğer alerjik reaksiyon belirtileri;
- yüzün, ellerin, ayakların şişmesi;
- nefes almada zorluk, yutma güçlüğü;
- eforla veya uzanırken veya şişmiş ayaklarda nefes darlığı.
Aşağıdaki reaksiyonlardan herhangi birini fark ederseniz, mümkün olan en kısa sürede doktorunuza söyleyiniz:
- ateş, kendini iyi hissetmeme, yaralar, diş problemleri, idrar yaparken yanma gibi enfeksiyon belirtileri;
- yorgunluk veya zayıflık;
- öksürük;
- karıncalanma;
- uyuşma;
- çift görme;
- kolların veya bacakların zayıflığı;
- iyileşmeyen şişlik veya açık yara
- Kalıcı ateş, morluklar, kanamalar, solgunluk gibi hematopoietik sistemi etkileyen rahatsızlıkların görünümünü düşündüren belirti ve semptomlar.
Yukarıda açıklanan semptomlar, HUMIRA ile görülen aşağıdaki yan etkilerin belirtileri olabilir:
Çok yaygın (10 kişiden 1'inden fazlasını etkileyebilir):
- enjeksiyon bölgesi reaksiyonları (ağrı, şişme, kızarıklık veya kaşıntı dahil);
- solunum yolu enfeksiyonları (soğuk algınlığı, burun akıntısı, sinüzit ve pnömoni dahil);
- baş ağrısı;
- karın ağrısı;
- mide bulantısı ve kusma;
- döküntü;
- kas-iskelet ağrısı.
Yaygın (10 kişiden 1'ini etkileyebilir):
- şiddetli enfeksiyonlar (septisemi ve grip dahil);
- cilt enfeksiyonları (selülit ve herpes zoster enfeksiyonu dahil);
- kulak enfeksiyonları;
- oral enfeksiyonlar (diş enfeksiyonları ve herpes simpleks dahil);
- üreme sistemi enfeksiyonları;
- İdrar yolu enfeksiyonları;
- mantar enfeksiyonları;
- eklem enfeksiyonları;
- iyi huylu tümörler;
- Cilt kanseri;
- alerjik reaksiyonlar (mevsimsel alerji dahil);
- dehidrasyon;
- ruh hali değişiklikleri (depresyon dahil);
- endişe;
- uyku bozuklukları;
- karıncalanma, seğirme veya uyuşma gibi hassasiyet bozuklukları;
- migren;
- sinir kökü sıkışması (bel ağrısı ve bacak ağrısı dahil);
- görsel rahatsızlıklar;
- göz iltihabı;
- göz kapaklarının iltihabı ve gözlerin şişmesi;
- baş dönmesi;
- hızlı kalp atışı hissi;
- hipertansiyon;
- sıcak basmalar;
- hematom;
- öksürük;
- astım;
- nefes darlığı;
- Sindirim sistemi kanaması;
- hazımsızlık (hazımsızlık, şişkinlik, mide ekşimesi);
- asit reflü bozukluğu;
- sicca sendromu (kuru gözler ve ağız dahil);
- kaşıntı;
- kaşıntılı döküntü;
- çürük;
- cilt iltihabı (egzama gibi);
- el ve ayak parmaklarının tırnaklarının kırılması;
- artan terleme;
- saç kaybı;
- sedef hastalığının başlangıcı veya kötüleşmesi;
- kas spazmları;
- idrarda kan;
- böbrek sorunları;
- göğüs ağrısı;
- ödem;
- ateş;
- kanama veya morarma riskini artıran sangdaki trombositlerin azalması;
- iyileşmede zorluk.
Yaygın olmayan (100 kişiden 1'ini etkileyebilir):
- fırsatçı enfeksiyonlar (tüberküloz ve bağışıklık savunması azaldığında ortaya çıkan diğer enfeksiyonları içerir);
- nörolojik enfeksiyonlar (viral menenjit dahil);
- göz enfeksiyonları;
- Bakteriyel enfeksiyonlar;
- divertikülit (kalın bağırsağın iltihabı ve enfeksiyonu);
- tümörler;
- lenfatik sistem tümörleri;
- melanom;
- akciğerleri, deriyi ve lenf düğümlerini etkileyebilen bağışıklık sistemi bozuklukları (çoğunlukla sarkoidoz olarak ortaya çıkar);
- vaskülit (kan damarlarının iltihabı);
- titreme;
- felç;
- nöropati;
- çift görme;
- işitme kaybı, çınlama;
- çarpıntı gibi düzensiz kalp atışı hissi;
- nefes darlığına veya ayak bileklerinde şişmeye neden olabilen kalp sorunları;
- Akut miyokard infarktüsü;
- ana arter duvarında kese oluşumu, damarda iltihaplanma ve pıhtı, kan damarının tıkanması;
- nefes darlığına neden olan akciğer hastalığı (iltihap dahil);
- pulmoner emboli (pulmoner arter tıkanıklığı);
- plevral efüzyon (plevral boşlukta anormal sıvı toplanması);
- karında ve sırtta şiddetli ağrıya neden olan pankreas iltihabı;
- yutma zorluğu;
- yüz ödemi;
- safra kesesi iltihabı, safra kesesi taşları;
- yağlı karaciğer;
- gece terlemeleri;
- yara izi;
- anormal kas katabolizması;
- sistemik lupus eritematozus (cilt, kalp, akciğer, eklemler ve diğer organların iltihabı dahil)
- kesintili uyku;
- iktidarsızlık;
- iltihaplar.
Seyrek (1.000 kişiden 1'ini etkileyebilir):
- lösemi (periferik düzeyde (kan) ve kemik iliğinde hematopoietik sistemi etkileyen malign neoplazm);
- şok ile şiddetli alerjik reaksiyon;
- çoklu skleroz;
- nörolojik bozukluklar (kas zayıflığına, anormal duyumlara, kollarda ve vücudun üst kısmında karıncalanmaya neden olabilen optik sinir iltihabı ve Guillain-Barré sendromu gibi);
- kalp durması;
- pulmoner fibroz (akciğerde yara izi);
- bağırsak perforasyonu;
- hepatit;
- hepatit B'nin yeniden etkinleştirilmesi;
- otoimmün hepatit (kendi bağışıklık sisteminizin neden olduğu karaciğer iltihabı);
- kutanöz vaskülit (derideki kan damarlarının iltihabı);
- Stevens-Johnson sendromu (erken belirtiler halsizlik, ateş, baş ağrısı ve döküntüdür);
- alerjik reaksiyonlarla ilişkili yüz ödemi;
- eritema multiforme (inflamatuar deri döküntüsü);
- lupus benzeri sendrom.
Bilinmiyor (eldeki verilerden sıklık tahmin edilemiyor):
- hepato-dalak T hücreli lenfoma (genellikle ölümcül olan nadir bir kan kanseri);
- Merkel hücreli karsinom (bir tür cilt kanseri);
- Karaciğer yetmezliği;
- dermatomiyozit adı verilen bir durumun kötüleşmesi (kas güçsüzlüğünün eşlik ettiği bir döküntü olarak kendini gösterir).
Humira ile görülen bazı yan etkiler asemptomatik olabilir ve sadece kan testlerinde bulunabilir. Bunlar şunları içerir:
Çok yaygın (10 kişiden 1'inden fazlasını etkileyebilir):
- düşük beyaz kan hücresi sayısı;
- düşük kırmızı kan hücresi sayısı;
- artan kan lipidleri;
- artan karaciğer enzimleri.
Yaygın (10 kişiden 1'ini etkileyebilir):
- artan beyaz kan hücresi sayısı;
- azaltılmış trombosit sayısı;
- kanda artan ürik asit;
- kandaki sodyum değişimi;
- kandaki kalsiyumun azalması;
- kandaki fosforun azalması;
- artan kan şekeri;
- artan kan laktat dehidrojenaz;
- kanda otoantikorların varlığı.
Seyrek (1.000 kişiden 1'ini etkileyebilir):
- düşük beyaz kan hücresi, kırmızı kan hücresi ve trombosit sayısı.
Bilinmiyor (eldeki verilerden sıklık tahmin edilemiyor):
- Karaciğer yetmezliği.
Yan etkilerin raporlanması
Çocuğunuz herhangi bir yan etki yaşarsa, bu broşürde listelenmeyen olası yan etkiler de dahil olmak üzere çocuğunuzun doktoru veya eczacısıyla konuşun. Yan etkileri doğrudan Ek V'te listelenen ulusal raporlama sistemi aracılığıyla da bildirebilirsiniz. Yan etkileri bildirerek bu ilacın güvenliği hakkında daha fazla bilgi sağlanmasına yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
EXP sonrası etiket/blister/karton üzerinde belirtilen son kullanma tarihinden sonra bu ilacı kullanmayınız.Son kullanma tarihi o ayın son gününü ifade etmektedir.
Buzdolabında (2°C - 8°C) saklayınız. Dondurmayın.
İlacı ışıktan korumak için flakonu uygun ambalajında saklayınız.
Herhangi bir ilacı atık su veya evsel atık yoluyla atmayın.Doktorunuza veya eczacınıza artık kullanmadığınız ilaçları nasıl atacağınızı sorun.Bu, çevrenin korunmasına yardımcı olacaktır.
Kompozisyon ve farmasötik form
Humira'nın içeriği
Aktif madde adalimumab'dır.
Diğer bileşenler mannitol, sitrik asit monohidrat, sodyum sitrat, sodyum dihidrojen fosfat dihidrat, disodyum fosfat dihidrat, sodyum klorür, polisorbat 80, sodyum hidroksit ve enjeksiyonluk sudur.
Bu tıbbi ürün 0,8 ml'lik doz başına 1 mmol'den (23 mg) daha az sodyum içerir, bu nedenle esasında "sodyum içermez" ve koruyucu içermez.
Humira şişelerinin görünümü ve paketin içeriği
HUMIRA 40 mg enjeksiyonluk çözelti, 0.8 ml çözelti içinde çözülmüş 40 mg adalimumab'ın steril bir çözeltisi olarak sağlanır.
Humira flakonları, bir cam flakonda bulunan bir adalimumab solüsyonundan oluşur. Bir paket, her biri 1 flakon, bir boş steril şırınga, 1 iğne, 1 flakon adaptörü ve 2 alkollü swab içeren 2 karton içerir.
Humira ayrıca kullanıma hazır şırınga veya kullanıma hazır kalem olarak da mevcuttur.
+ Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
HUMIRA 40 MG / 0.8 ML ÇOCUK KULLANIM İÇİN ENJEKSİYON ÇÖZÜMÜ
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Her 0.8 ml tek dozluk flakon 40 mg adalimumab içerir.
Adalimumab, Çin Hamsteri Yumurtalık hücrelerinde eksprese edilen bir rekombinant insan monoklonal antikorudur.
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakın.
03.0 FARMASÖTİK FORM
Enjeksiyon için berrak çözüm.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Jüvenil idiopatik artriti
Poliartiküler jüvenil idiyopatik artrit
Humira, metotreksat ile kombinasyon halinde, bir veya daha fazla hastalığı modifiye edici anti-romatizmal ilaca (DMARD) yetersiz yanıt veren 2 yaşından büyük hastalarda aktif poliartiküler jüvenil idiyopatik artrit tedavisinde endikedir.HUMIRA monoterapi olarak uygulanabilir. metotreksat intoleransı durumunda veya metotreksat ile tedaviye devam edilmesi uygun olmadığında (monoterapideki etkinlik için bkz. bölüm 5.1). Humira, 2 yaşından küçük hastalarda çalışılmamıştır.
Entezit ile ilişkili artrit
HUMIRA, yetersiz yanıt veren veya geleneksel tedaviye tolerans göstermeyen 6 yaşından büyük hastalarda entezit ile ilişkili artritin aktif formlarının tedavisinde endikedir (bkz. bölüm 5.1).
Pediatrik hastalarda Crohn hastalığı
Humira, birincil beslenme tedavisi, kortikosteroid tedavisi ve bir immünomodülatör dahil olmak üzere geleneksel tedaviye yetersiz yanıt veren veya tedaviye toleransı olmayan veya kontrendikasyonları olan pediyatrik hastalarda (6 yaşından itibaren) şiddetli aktif Crohn hastalığının tedavisinde endikedir. bu tür terapiler.
04.2 Pozoloji ve uygulama yöntemi
Dozaj
Humira tedavisi, Humira'nın endike olduğu durumların tanı ve tedavisinde deneyimli uzman doktorlar tarafından başlatılmalı ve izlenmelidir. Humira ile tedavi edilen hastalara özel bir uyarı kartı verilmelidir.
Humira enjeksiyon tekniği hakkında uygun talimat verildikten sonra hastalar, doktorları uygun görürse ve gerektiğinde periyodik tıbbi kontrollerle kendilerine enjeksiyon yapabilirler.
Pediatrik popülasyon
Jüvenil idiopatik artriti
2 ila 12 yaş arası poliartiküler jüvenil idiyopatik artrit.
2 ila 12 yaş arasındaki poliartiküler jüvenil idiyopatik artrit hastaları için önerilen HUMIRA dozu 24 mg/m2 vücut yüzey alanıdır ve maksimum tek doz 20 mg adalimumab (2 yaş altı hastalar için deri altı olarak uygulanır. Hacim d " enjeksiyon seçilir. hastanın boy ve kilosuna göre (Tablo 1).
Tablo 1. Poliartiküler jüvenil idiyopatik artriti ve entezit ile ilişkili artriti olan hastaların boy ve kilolarına göre mililitre (ml) cinsinden humira dozu
* Maksimum tek doz 40 mg'dır (0,8 ml)
13 yaşından itibaren poliartiküler jüvenil idiyopatik artrit
13 yaş ve üzeri hastalarda vücut yüzey alanından bağımsız olarak iki haftada bir 40 mg'lık bir doz uygulanır.
Bu tür hastalar için, 40 mg'lık bir dozun uygulanması için 40 mg'lık kalemler ve 40 mg'lık kullanıma hazır şırıngalar da mevcuttur.
Mevcut veriler, klinik yanıtın genellikle tedaviden sonraki 12 hafta içinde elde edildiğini göstermektedir. Bu süre içinde tedaviye yanıtı yetersiz olan hastalarda tedaviye devam edilmesi gerekliliği dikkatle değerlendirilmelidir.
Bu endikasyonda 2 yaşından küçük hastalarda HUMIRA'nın ilgili kullanımı yoktur.
Entezit ile ilişkili artrit
6 yaş ve üzeri, entezit ile ilişkili artritli hastalarda önerilen HUMIRA dozu, iki haftada bir subkutan enjeksiyon yoluyla uygulanan maksimum tek doz 40 mg adalimumab olmak üzere 24 mg/m2 vücut yüzey alanıdır. Enjeksiyon hacmi hastanın boyuna ve kilosuna göre seçilir (Tablo 1).
Humira, entezit ile ilişkili artriti olan 6 yaşından küçük hastalarda çalışılmamıştır.
Pediatrik hastalarda Crohn hastalığı
Pediatrik hastalarda Crohn hastalığı
Şiddetli Crohn hastalığı olan pediatrik gönüllülerde HUMIRA'nın önerilen indüksiyon dozu 0. haftada 40 mg, ardından 2. haftada 20 mg'dır. Tedaviye daha hızlı yanıt gerekiyorsa, 0. haftada 80 mg'lık bir rejim kullanılabilir. doz bir günde iki enjeksiyon olarak verilebilir) ve daha yüksek indüksiyon dozunun kullanılmasıyla advers olay riskinin daha yüksek olabileceği anlayışıyla 2. haftada 40 mg.
İndüksiyon tedavisinden sonra önerilen doz, deri altı enjeksiyon yoluyla iki haftada bir 20 mg'dır. Yetersiz yanıt veren bazı kişiler, doz sıklığının her hafta 20 mg HUMIRA'ya yükseltilmesinden fayda görebilir.
≥ 40 kg pediyatrik hastalarda Crohn hastalığı:
Şiddetli Crohn hastalığı olan pediatrik gönüllülerde HUMIRA'nın önerilen indüksiyon dozu 0. haftada 80 mg, ardından 2. haftada 40 mg'dır. Tedaviye daha hızlı yanıt gerekiyorsa, 0. haftada 160 mg'lık bir rejim kullanılabilir. doz bir günde dört enjeksiyon olarak veya iki ardışık gün boyunca günde iki enjeksiyon olarak) ve daha yüksek doz kullanımıyla advers olay riskinin daha yüksek olabileceği anlayışıyla 2. haftada 80 mg olarak verilebilir. indüksiyon.
İndüksiyon tedavisinden sonra önerilen doz, subkutan enjeksiyon yoluyla iki haftada bir 40 mg'dır. Yetersiz yanıt veren bazı kişiler, doz sıklığının her hafta 40 mg HUMIRA'ya yükseltilmesinden fayda görebilir.
12. haftada yanıt vermeyen bir hastada tedaviye devam edilmesi dikkatle düşünülmelidir.
Tam 40 mg doza ihtiyaç duyan hastalarda uygulama için 40 mg'lık bir kalem ve 40 mg'lık kullanıma hazır şırınga da mevcuttur.
Bu endikasyonda 6 yaşından küçük çocuklarda HUMIRA'nın ilgili kullanımı yoktur.
Böbrek ve/veya karaciğer yetmezliği
Humira bu tip popülasyonda çalışılmamıştır. Dozaj tavsiyesi verilemez.
Uygulama yöntemi
Humira deri altına enjeksiyon yoluyla verilir. Kullanım için tam talimatlar paket broşüründe verilmiştir.
04.3 Kontrendikasyonlar
Etkin maddeye veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
Aktif tüberküloz veya sepsis ve fırsatçı enfeksiyonlar gibi diğer ciddi enfeksiyonlar (bkz. bölüm 4.4).
Orta ila şiddetli kalp yetmezliği (NYHA sınıf III / IV) (bkz. bölüm 4.4).
04.4 Özel uyarılar ve uygun kullanım önlemleri
Biyolojik tıbbi ürünlerin izlenebilirliğini artırmak için uygulanan ürünün ticari markası ve seri numarası açıkça kaydedilmelidir (veya işaretlenmelidir).
Enfeksiyonlar
TNF antagonistleri ile tedavi edilen hastalar ciddi enfeksiyonlara karşı daha hassastır. Bozulmuş akciğer fonksiyonu enfeksiyon geliştirme riskini artırabilir, bu nedenle hastalar HUMIRA tedavisi öncesinde, sırasında ve sonrasında tüberküloz dahil olmak üzere enfeksiyonlara karşı dikkatli bir şekilde taranmalıdır. Adalimumabın eliminasyonu dört aya kadar sürebileceğinden, bu dönemde izlemeye devam edilmelidir.
Kronik veya lokalize enfeksiyonlar dahil aktif enfeksiyonları olan hastalarda, bunlar kontrol altına alınana kadar HUMIRA tedavisine başlanmamalıdır. Tüberküloza maruz kalmış hastalarda ve histoplazmoz, koksidiyomikoz veya blastomikoz gibi yüksek tüberküloz veya endemik mikoz riski olan bölgelere seyahat eden hastalarda, tedaviye başlamadan önce HUMIRA tedavisinin risk ve yararı düşünülmelidir (bkz. Diğer fırsatçı enfeksiyonlar).
HUMIRA tedavisi sırasında yeni bir enfeksiyon gelişen hastalar yakından takip edilmeli ve tam bir tanısal değerlendirmeye tabi tutulmalıdır. Yeni bir ciddi enfeksiyon veya sepsis gelişirse, HUMIRA uygulaması durdurulmalı ve enfeksiyon kontrol altına alınana kadar uygun antimikrobiyal veya antifungal tedavi başlatılmalıdır. Doktorlar, tekrarlayan enfeksiyon öyküsü olan veya eşlik eden durumlarla birlikte HUMIRA kullanırken dikkatli olmalıdır. immünosupresif ilaçların eşzamanlı kullanımı da dahil olmak üzere hastaları enfeksiyonlara yatkın hale getirir.
Şiddetli enfeksiyonlar:
HUMIRA ile tedavi edilen hastalarda bakteri, mikobakteri, istilacı mantar, parazit, virüs veya listeriosis, lejyonelloz ve pnömokistoz gibi diğer fırsatçı enfeksiyonların neden olduğu sepsis dahil ciddi enfeksiyonlar bildirilmiştir.
Klinik çalışmalarda görülen diğer ciddi enfeksiyonlar arasında pnömoni, piyelonefrit, septik artrit ve septisemi bulunur. Enfeksiyonlarla ilişkili hastaneye yatış veya ölümcül olaylar bildirilmiştir.
Tüberküloz:
HUMIRA kullanan hastalarda reaktivasyon ve yeni tüberküloz başlangıcı dahil tüberküloz bildirilmiştir. Akciğer ve akciğer dışı (yani yaygın) tüberküloz vakaları bildirilmiştir.
HUMIRA ile tedaviye başlamadan önce, tüm hastalar aktif veya inaktif ("gizli") tüberküloz varlığı açısından incelenmelidir. Bu değerlendirme, "önceden tüberküloz öyküsü olan veya aktif tüberkülozlu kişilerle herhangi bir teması olan ve önceki ve/veya eşzamanlı immünosupresif tedavileri olan hastaların ayrıntılı tıbbi öyküsünü içermelidir. Uygun tarama testleri (örn. tüberkülozda deri testi ve göğüs röntgeni) ) tüm hastalarda (yerel kılavuzlara uyulabilir.) Bu testlerin yapılması ve sonuçların hasta uyarı kartına kaydedilmesi önerilir. Hekimler, özellikle ağır hasta veya bağışıklığı baskılanmış hastalarda, yanlış negatif tüberkülin deri testi sonuçları riskine karşı dikkatli olmalıdır.
Aktif tüberküloz teşhisi konulursa, HUMIRA tedavisi başlatılmamalıdır (bkz. bölüm 4.3).
Aşağıda açıklanan tüm durumlarda, "HUMIRA tedavisinin risk/fayda oranının dikkatli bir değerlendirmesi yapılmalıdır.
Gizli tüberkülozdan şüpheleniliyorsa, tüberküloz tedavisinde uzmanlaşmış bir doktora danışmanız önerilir.
Gizli tüberküloz teşhisi konulursa, Humira ile tedaviye başlamadan önce yerel önerilere göre anti-tüberküloz profilaksisi başlatılmalıdır.
Tüberküloz testi negatif olmasına rağmen tüberküloz için farklı veya önemli risk faktörleri olan hastalarda ve tıbbi geçmişinde kişisel geçmişinde latent veya aktif tüberküloz öyküsü bulunan hastalarda HUMIRA tedavisine başlamadan önce anti-tüberküloz profilaksisi tedavisi de düşünülmelidir. geçirdikleri tedavinin seyrinin yeterli olup olmadığını teyit etmek mümkün değildir.
Tüberkülozun profilaktik tedavisine rağmen, HUMIRA ile tedavi edilen hastalarda tüberkülozun reaktivasyonu vakaları meydana gelmiştir. Aktif tüberküloz tedavisi gören bazı hastalarda Humira tedavisi sırasında tekrar tüberküloz görülmüştür.
HUMIRA tedavisi sırasında veya sonrasında olası tüberküloz enfeksiyonunu düşündüren belirti/semptomlar (örn. inatçı öksürük, halsizlik, kilo kaybı, orta derecede ateş, halsizlik) ortaya çıkarsa, hastalara tıbbi yardım almaları tavsiye edilmelidir.
Diğer fırsatçı enfeksiyonlar:
HUMIRA alan hastalarda invaziv mantar enfeksiyonları dahil fırsatçı enfeksiyon vakaları gözlenmiştir. Bu enfeksiyonlar, TNF-antagonistleri alan hastalarda doğru bir şekilde teşhis edilmemiştir ve bu, uygun tedavide gecikmeye ve bazen ölümcül sonuçlara neden olmuştur.
Ateş, halsizlik, kilo kaybı, terleme, öksürük, dispne ve/veya pulmoner infiltrat veya eşlik eden şokla birlikte veya eşlik etmeyen diğer ciddi sistemik hastalık gibi belirti ve semptomlar gelişen hastalarda, invaziv bir mantar enfeksiyonundan şüphelenilmeli ve tedavi derhal durdurulmalıdır. Humira'nın Uygulanması Bu hastalarda teşhis ve ampirik antifungal tedavinin uygulanması, invaziv mantar enfeksiyonları olan hastaların tedavisinde uzmanlaşmış bir hekime danışılarak yapılmalıdır.
Hepatit B'nin Reaktivasyonu
HUMIRA dahil TNF antagonistleri ile tedavi edilen kronik hepatit B virüsü taşıyıcılarında hepatit B'nin yeniden aktivasyonu (örn. yüzey antijeni pozitif) meydana gelmiştir. Bazı vakaların ölümcül sonuçları oldu. HUMIRA ile tedaviye başlamadan önce, hastalar hepatit B virüsü enfeksiyonu için test edilmelidir.Hepatit B virüsü testi pozitif olan hastalar için hepatit B tedavisinde deneyimli bir hekime danışılması önerilir.Hepatit B.
HUMIRA ile tedavi gerektiren hepatit B virüsü taşıyıcıları, sadece tedavi boyunca değil, aynı zamanda tedavinin kesilmesini takip eden aylarda da aktif hepatit B virüsü enfeksiyonunun belirti ve semptomları açısından yakından izlenmelidir.Hastaların tedavisinden yeterli veri mevcut değildir. Hepatit B virüsünün TNF-antagonist tedavisi ile birlikte yeniden aktifleşmesini önlemek için anti-viral tedavi gören hepatit B virüsü ile Hepatit B virüsü reaktivasyonu gelişen hastalarda, HUMIRA uygulaması kesilmeli ve aşağıdakilerle birlikte etkili anti-viral tedavi başlatılmalıdır. yeterli destekleyici tedavi.
nörolojik olaylar
Humira dahil TNF-antagonistleri, nadir vakalarda, klinik semptomların yeni başlangıcı veya alevlenmesi ve/veya multipl skleroz, optik nörit ve Guillain-Barrè sendromu dahil periferik demiyelinizan hastalıklar dahil olmak üzere merkezi sinir sistemi demiyelinizan hastalıkların radyografik kanıtları ile ilişkilendirilmiştir. Merkezi veya periferik demiyelinizan bozuklukların daha önce veya yakın zamanda başladığı hastalarda HUMIRA kullanımında kullanılmalıdır.
Alerjik reaksiyonlar
Klinik çalışmalarda, Humira ile ilişkili ciddi alerjik reaksiyonlar nadirdi. Klinik çalışmalar sırasında HUMIRA ile ilişkili ciddi olmayan alerjik reaksiyonlar yaygın değildir. HUMIRA uygulamasını takiben anafilaksi dahil ciddi alerjik reaksiyonlar bildirilmiştir Anafilaktik reaksiyonlar veya diğer şiddetli alerjik belirtiler meydana gelirse, HUMIRA uygulaması derhal durdurulmalı ve uygun tedavi başlatılmalıdır.
bağışıklık bastırma
Humira ile tedavi gören romatoid artritli 64 hasta üzerinde yapılan bir çalışmada, gecikmiş aşırı duyarlılığın inhibisyonu, immünoglobulin seviyelerinde azalma veya T, B, NK, monosit/hücre lenfositleri, makrofajlar ve nötrofillerin sayısında değişiklik olduğuna dair bir kanıt yoktu.
Neoplazmalar ve lenfoproliferatif hastalıklar
TNF antagonisti klinik çalışmalarının kontrollü bölümlerinde, TNF-bloker alan hastalarda kontrol grubuna göre lenfoma dahil daha fazla malignite vakası gözlendi. Ancak vakalar nadirdi. Pazarlama sonrası çalışmalarda, bir TNF-antagonisti ile tedavi edilen hastalarda lösemi vakaları bildirilmiştir. Risk değerlendirmesini zorlaştıran inflamatuar bir hastalık olan ciddi derecede aktif ve uzun süreli romatoid artritli hastalarda lenfoma ve lösemi gelişme riski daha yüksektir.Mevcut bilgilerle lenfoma gelişimi göz ardı edilemez.Hastalarda lösemi ve diğer maligniteler anti-TNF ilaçlarla tedavi edilir.
Pazarlama sonrası çalışmalarda, adalimumab dahil TNF antagonistleri (tedavi başlangıcı ≤ 18 yıl) ile tedavi edilen çocuklarda, ergenlerde ve genç erişkinlerde (22 yaşına kadar) bazıları ölümcül olan kanser vakaları bildirilmiştir. Vakaların yaklaşık yarısı lenfoma idi. Diğer vakalar çok sayıda farklı kanseri temsil ediyordu ve genellikle immünosupresyonla ilişkili nadir kanserleri içeriyordu. TNF antagonistleri ile tedavi edilen çocuklarda ve ergenlerde tümör gelişimi riski göz ardı edilemez.
Adalimumab ile tedavi edilen hastalarda pazarlama sonrası nadir görülen hepatosplenik T hücreli lenfoma vakaları gözlenmiştir.Bu nadir T hücreli lenfoma tipi çok agresif bir klinik seyir gösterir ve genellikle ölümcüldür. Bu hepatosplenik T hücreli lenfoma vakalarından bazıları, Humira ile tedavi edilen ve inflamatuar bağırsak hastalığını tedavi etmek için kullanılan ilaçlar olan azatioprin veya 6-merkaptopurin ile eş zamanlı tedavi alan genç yetişkin hastalarda meydana geldi. Azatioprin veya 6-merkaptopurin ve HUMIRA kombinasyonundan kaynaklanan potansiyel risk dikkatle değerlendirilmelidir. HUMIRA ile tedavi edilen hastalarda hepatosplenik T hücreli lenfoma gelişme riski göz ardı edilemez (bkz. bölüm 4.8).
Kanser öyküsü olan hastalarda veya kanser geliştikten sonra HUMIRA tedavisine devam edilen hastalarda hiçbir klinik çalışma yapılmamıştır. Bu nedenle, bu hasta popülasyonunda HUMIRA tedavisi ek dikkatle düşünülmelidir (bkz. bölüm 4.8).
HUMIRA ile tedaviden önce ve tedavi sırasında, tüm hastalar, özellikle yoğun immünosupresif tedavi öyküsü olanlar veya PUVA ile tedavi öyküsü olan sedef hastalığı olanlar, olası bir melanotik olmayan cilt kanseri varlığı açısından incelenmelidir. Adalimumab dahil TNF antagonistleri ile tedavi edilen hastalarda melanom ve Merkel hücreli karsinom da bildirilmiştir (bkz. bölüm 4.8).
Orta ila şiddetli kronik obstrüktif akciğer hastalığı (KOAH) olan hastalarda başka bir TNF antagonisti olan infliksimabın kullanımını değerlendiren bir keşif amaçlı klinik çalışmada, infliksimab ile tedavi edilen hastalarda kontrol hastalarına göre daha fazla malignite bildirilmiştir. Tüm hastalarda ağır sigara içiciliği öyküsü vardır.Bu nedenle KOAH hastalarında ve aşırı sigara içimine bağlı malignite riski yüksek hastalarda herhangi bir TNF-antagonisti kullanırken dikkatli olunmalıdır.
Mevcut verilere dayanarak, adalimumab tedavisinin displazi veya kolon kanseri geliştirme riskini etkileyip etkilemediği bilinmemektedir. Kolon displazisi veya karsinom riski yüksek olan tüm ülseratif kolitli hastalar (örneğin, uzun süredir ülseratif kolit veya primer sklerozan kolanjit olan hastalar) veya daha önce displazi veya kolon kolon kanseri öyküsü olan tüm hastalar taranmalıdır. hastalık boyunca displazi için düzenli olarak. Bu değerlendirme, yerel önerilere dayalı kolonoskopileri ve biyopsileri içermelidir.
Hematopoetik sistemi etkileyen reaksiyonlar
Anti-TNF ilaçlarının kullanımını takiben aplastik anemi oluşumu da dahil olmak üzere nadir pansitopeni vakaları bildirilmiştir.Tıbbi açıdan HUMIRA ile tedavi edilen hastalarda önemli sitopeniler dahil hematopoietik sistemi etkileyen advers olaylar bildirilmiştir. (örneğin, trombositopeni, lökopeni) HUMIRA ile tedavi sırasında tüm hastalara, kan diskrazisinin varlığını düşündüren belirti ve semptomlar (örn. inatçı ateş, morarma, kanama, solgunluk) yaşarlarsa, yeterli yardım almak için derhal bir doktora danışmaları tavsiye edilmelidir. Hematopoietik sistemde doğrulanmış önemli değişiklikleri olan hastalarda, HUMIRA tedavisinin kesilmesi gerektiği düşünülmelidir.
aşılar
Adalimumab veya plasebo ile tedavi edilen romatoid artritli 226 yetişkin gönüllünün katıldığı bir çalışmada, standart 23 valanslı pnömokok aşısına ve üç valanslı influenza virüsü aşısına benzer antikor tepkileri gözlendi. Humira alan hastalar.
Pediyatrik hastalarda, Humira bazlı tedaviye başlamadan önce, mümkünse mevcut aşılama kılavuzlarına uygun olarak planlanan aşılama programının uygulanması tavsiye edilir.
Humira ile tedavi edilen hastalar, canlı aşılar hariç, eş zamanlı aşılar alabilirler. İn utero adalimumab'a maruz kalan bebeklere, annenin hamilelik sırasında son adalimumab uygulamasını takip eden 5 ay boyunca canlı aşı uygulanması önerilmez.
Konjestif kalp yetmezliği
Başka bir anti-TNF ilacıyla yapılan bir klinik çalışmada, konjestif kalp yetmezliğinin kötüleşmesi ve buna bağlı olarak artan mortalite gözlenmiştir. Humira ile tedavi edilen hastalarda konjestif kalp yetmezliğinde kötüleşme de gözlenmiştir. Hafif kalp yetmezliği olan hastalarda (NYHA sınıf I/II) HUMIRA dikkatli kullanılmalıdır. Humira orta veya şiddetli kalp yetmezliğinde kontrendikedir (bkz. bölüm 4.3) Konjestif kalp yetmezliğinin kötüleşmesi veya yeni semptomları olan hastalarda HUMIRA tedavisi kesilmelidir.
Otoimmün süreçler
Humira ile tedavi, otoimmün antikorların oluşumunu indükleyebilir. Humira ile uzun süreli tedavinin otoimmün hastalıkların gelişimi üzerindeki etkisi bilinmemektedir.Bir hasta Humira ile tedaviyi takiben lupus benzeri sendromu düşündüren semptomlar geliştirirse ve çift sarmallı DNA'ya karşı antikorlar için pozitifse, Humira ile daha fazla tedavi uygulamayın. verilmelidir (bkz. bölüm 4.8).
Biyolojik DMARDS veya TNF antagonistlerinin birlikte uygulanması
Anakinra ve başka bir anti-TNF ilacı olan etanercept ile kombinasyon tedavisinin klinik çalışmalarında, tek başına etanersept ile karşılaştırıldığında klinik yararı olmayan ciddi enfeksiyonlar gözlenmiştir.Anakinra ve etanercept kombinasyonu ile gözlenen advers olayların türü göz önüne alındığında, anakinra ve başka bir anti-TNF ilacının kombinasyonundan sonra benzer yan etkiler ortaya çıkabilir. Bu nedenle adalimumabın anakinra ile kombinasyonu önerilmez (bkz. bölüm 4.5).
Adalimumabın diğer biyolojik DMARDS (örn. anakinra ve abatacept) veya diğer TNF antagonistleri ile birlikte uygulanması, ciddi enfeksiyonlar ve diğer potansiyel ilaç etkileşimleri dahil olmak üzere olası enfeksiyon riskinde artış nedeniyle önerilmez (bkz. bölüm 4.5).
cerrahi müdahaleler
HUMIRA ile tedavi edilen hastalarda cerrahi prosedürlerin güvenliği konusunda "sınırlı" deneyim mevcuttur. Adalimumabın uzun yarılanma ömrü cerrahi planlanırken dikkate alınmalıdır. HUMIRA tedavisi görürken ameliyat olan bir hasta enfeksiyon gelişimi açısından yakından takip edilmeli, bu durumda önlem alınmalıdır. Humira kullanırken eklem replasman cerrahisi geçiren hastalarda güvenlikle ilgili "sınırlı" deneyim vardır.
İnce bağırsak tıkanıklığı
Crohn hastalığı tedavisine yanıt verilmemesi, ameliyat gerektirebilecek rijit fibrotik stenozun varlığını gösterebilir. Mevcut veriler, Humira'nın kötüleşmediğini veya darlıklara neden olmadığını göstermektedir.
Daha yaşlı insanlar
Humira ile tedavi edilen 65 yaş üstü hastalarda ciddi enfeksiyon sıklığı (%3.5), 65 yaş altı hastalardan (%1.5) daha yüksekti. Bunlardan bazılarının ölümcül sonuçları oldu. Yaşlı hastaların tedavisinde enfeksiyon riskine özellikle dikkat edilmelidir.
Pediatrik popülasyon
Yukarıdaki Aşılara bakın.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Humira tedavisi, romatoid artrit, poliartiküler jüvenil idiyopatik artrit ve psoriatik artritli hastalarda monoterapi olarak ve metotreksat ile kombinasyon halinde incelenmiştir. HUMIRA, monoterapiye göre metotreksat ile kombinasyon halinde verildiğinde antikor oluşumu daha düşüktü. HUMIRA'nın metotreksat olmadan uygulanması, adalimumabın antikor oluşumunun artmasına, klirensinin artmasına ve etkinliğinin azalmasına neden olmuştur (bkz. bölüm 5.1).
Humira ve anakinra kombinasyonu önerilmez (bkz. bölüm 4.4 "Biyolojik DMARD'ların veya TNF antagonistlerinin birlikte uygulanması").
Humira ve abatacept kombinasyonu önerilmez (bkz. bölüm 4.4 "Biyolojik DMARD'ların veya TNF antagonistlerinin birlikte uygulanması").
04.6 Hamilelik ve emzirme
Gebelik
HUMIRA için, gebeliklerde maruz kalmaya ilişkin sınırlı klinik veri mevcuttur.
Maymunlarda yürütülen bir gelişimsel toksisite çalışmasında, hiçbir maternal toksisite, embriyotoksisite veya teratojenisite bulunmamıştır. Adalimumabın doğum sonrası toksisitesine ilişkin klinik öncesi veriler mevcut değildir (bkz. bölüm 5.3).
TNFa inhibisyonu nedeniyle, hamilelik sırasında adalimumab uygulaması yenidoğanın normal bağışıklık tepkisini etkileyebilir, bu nedenle adalimumab uygulaması hamilelikte önerilmez.
Adalimumab plasentayı geçebilir ve hamilelik sırasında adalimumab ile tedavi edilen annelerden doğan bebeklerin serumuna ulaşabilir. Sonuç olarak, bu çocuklar daha büyük bir enfeksiyon riskine maruz kalmaktadır. İn utero adalimumab'a maruz kalan bebeklere, annenin hamilelik sırasında son adalimumab uygulamasını takip eden 5 ay boyunca canlı aşı uygulanması önerilmez.
Besleme zamanı
Adalimumabın insan sütüne geçip geçmediği veya yuttuktan sonra sistemik olarak emilip emilmediği bilinmemektedir.
Bununla birlikte, insan immünoglobulinleri sütle atıldığından, kadınlar son Humira tedavisinden sonra en az beş ay emzirmemelidir.
Doğurganlık
Adalimumabın doğurganlık üzerindeki etkilerine ilişkin klinik öncesi veriler mevcut değildir.
Çocuk doğurma çağındaki kadınlar. Erkeklerde ve kadınlarda kontrasepsiyon
Çocuk doğurma potansiyeli olan kadınlar, hamileliği önlemek için yeterli doğum kontrolü kullanmalı ve son Humira tedavisinden sonra en az beş ay boyunca kullanımına devam etmelidir.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
HUMIRA'nın araç veya makine kullanma yeteneği üzerinde minör etkileri vardır. HUMIRA uygulamasını takiben baş dönmesi ve görme bozuklukları meydana gelebilir (bkz. bölüm 4.8).
04.8 İstenmeyen etkiler
Humira, 8.198 hastada, pivot kontrollü ve açık etiketli klinik çalışmalarda 60 aya kadar veya daha uzun süre çalışılmıştır. Bu çalışmalar, erken başlangıçlı ve uzun süreli romatoid artritli, jüvenil idiyopatik artritli (poliartiküler jüvenil idiyopatik artrit ve entezit ile ilişkili artritli) hastalarda ve ayrıca aksiyel spondiloartritli hastalarda (ankilozan spondilit ve radyografik pondilozik kanıtı olmayan aksiyal spondiloartrit) yapılmıştır. ), psoriatik artrit, Crohn hastalığı, ülseratif kolit ve sedef hastalığı. Kontrol periyodu sırasında Humira alan 5.343 hastada ve plasebo veya aktif bir karşılaştırıcı alan 3.148 hastada pivot kontrollü çalışmalar yürütülmüştür.
Pivotal çalışmaların çift-kör, kontrollü fazı sırasında advers olaylar nedeniyle tedaviyi bırakan hastaların yüzdesi, HUMIRA alan hastalar için %6,1 ve kontrol edilen tedavi edilen hastalar için %5,7'dir.
Güvenlik profilinin özeti
En sık bildirilen advers reaksiyonlar enfeksiyonlar (nazofarenjit, üst solunum yolu enfeksiyonu ve sinüzit gibi), uygulama yeri reaksiyonları (eritem, kaşıntı, kanama, ağrı veya şişlik), baş ağrısı ve kas-iskelet ağrısıdır.
Humira için ciddi advers reaksiyonlar bildirilmiştir. Humira gibi TNF bloke eden ilaçlar bağışıklık sistemini etkiler ve bunların kullanımı vücudun enfeksiyonlara ve kansere karşı savunmasını etkileyebilir.
Humira uygulamasını takiben ölümcül enfeksiyon vakaları (sepsis, fırsatçı enfeksiyonlar ve TB vakaları dahil), HBV enfeksiyonunun reaktivasyonu ve çeşitli malignite türleri (lösemi, lenfoma ve hepato-lenfoma vakaları dahil) de bildirilmiştir. hücreler).
Şiddetli hematolojik, nörolojik ve otoimmün reaksiyonlar da bildirilmiştir. İkincisi, nadir görülen pansitopeni, aplastik anemi, merkezi ve periferik demiyelinizasyon olayları ve lupus, lupus ile ilgili durumlar ve Stevens-Johnson sendromu vakalarını içerir.
Pediatrik popülasyon
Pediyatrik hastalarda istenmeyen etkiler
Genel olarak, pediyatrik hastalardaki advers olaylar, hem sıklık hem de tip açısından yetişkin hastalarda görülenlere benzerdi.
Advers reaksiyonların listesinin tablosu
Aşağıdaki advers reaksiyonlar listesi, klinik çalışmalardan elde edilen deneyimlere ve pazarlama sonrası deneyimlere dayanmaktadır ve ilgili sistem/organ ve sıklığa göre sınıflandırılmıştır (çok yaygın ≥1/10; yaygın ≥1/100 ila
Tablo 2
Yan etkiler
* 4.3, 4.4 ve 4.8 bölümlerinde daha fazla bilgi bulunmaktadır.
** açık etiketli uzatma çalışmaları dahil
1) spontane raporlardan elde edilen veriler dahil
Seçilmiş advers reaksiyonların tanımı
Enjeksiyon bölgesindeki reaksiyonlar
Yetişkinlerde ve çocuklarda yapılan pivotal kontrollü klinik çalışmalarda, HUMIRA ile tedavi edilen hastaların %13,6'sında enjeksiyon bölgesi reaksiyonları (eritem ve/veya kaşıntı, kanama, ağrı veya ödem), plasebo veya aktif kontrol ile tedavi edilen hastaların %7,6'sında görülmüştür. genellikle ilacın kesilmesini gerektirmez.
Enfeksiyonlar
Yetişkinlerde ve çocuklarda yapılan pivot kontrollü klinik çalışmalarda, enfeksiyon oranı Humira grubunda hasta/yıl başına 1.52 ve plasebo ve aktif kontrol gruplarında hasta/yıl başına 1.45 idi.Enfeksiyonlar başlıca nazofarenjit, üst solunum yolu enfeksiyonları ve idrar yolu enfeksiyonu Çoğu hasta enfeksiyon temizlendikten sonra HUMIRA almaya devam etmiştir.
Ciddi enfeksiyon insidansı, Humira grubunda hasta başına / yıl başına 0.04 ve plasebo ve aktif kontrollü gruplarda hasta başına / yıl başına 0.03 idi.
HUMIRA ile yetişkinlerde ve çocuklarda yapılan kontrollü ve açık etiketli çalışmalarda, ciddi enfeksiyonlar (sadece nadiren meydana gelen ölümcül enfeksiyonlar dahil), tüberküloz vaka raporları (miliyer ve akciğer dışı yerleşimler dahil) ve invaziv fırsatçı enfeksiyonlar bildirilmiştir. örneğin, yayılmış veya ekstrapulmoner histoplazmoz, blastomikoz, koksidiyoidomikoz, pnömokistoz, kandidiyaz, aspergilloz ve listeriosis). Çoğu tüberküloz vakası, tedavinin başlamasından sonraki ilk sekiz ay içinde meydana geldi ve gizli hastalığın yeniden ortaya çıkması olarak yorumlanabilir.
Neoplazmalar ve lenfoproliferatif hastalıklar
Juvenil idiyopatik artritli (poliartiküler jüvenil idiyopatik artrit ve entezit ile ilişkili artrit) hastalara HUMIRA uygulanarak yapılan çalışmalarda, 655,6 hasta yılı maruziyeti olan 249 pediatrik hastada malignite gözlenmemiştir.Ayrıca 192 pediatrik hastada malignite gözlenmemiştir. Crohn hastalığı olan pediyatrik hastalara HUMIRA uygulanan bir çalışma sırasında 258.9 hasta yılı maruziyeti olan hastalar.
Orta ila şiddetli aktif romatoid artrit, ankilozan spondilit, radyografik ankilozan spondilit, psoriatik artrit, sedef hastalığı, Crohn hastalığı ve ülseratif kolit, neoplazmaları olmayan aksiyal spondiloartrit hastalarında en az 12 hafta süren HUMIRA ile yapılan yetişkin pivotal çalışmaların kontrollü bölümlerinde, Humira ile tedavi edilen 4.622 hastada 1.000 hasta-yılı başına 6.0 (3.7, 9.8) oranında lenfoma ve melanotik olmayan cilt kanseri (%95 güven aralığı) gözlenmiştir. ile 2.828 kontrol hastasının 1.000 hasta-yılı başına 5.1 (2.4, 10.7) oranı (ortanca tedavi süresi HUMIRA ile tedavi edilen hastalar için 5.1 ay ve hasta kontrolü için 4.0 aydı). Melanotik olmayan cilt kanserlerinin oranı (%95 güven aralığı) Humira ile tedavi edilen hastalarda 1.000 hasta yılı başına 9.7 (6.6; 14.3) ve kontrol hastalarında 1.000 hasta yılı başına 5.1 (2.4; 10 , 7) idi. Bu cilt kanserlerinden, skuamöz hücreli karsinomlar, Humira ile tedavi edilen hastalarda 1000 hasta-yılı başına 2,6 (1.2; 5.5) ve kontrol hastalarında 1.000 hasta-yılı başına 0.7 (0.1; 5.2) oranlarında (%95 güven aralığı) meydana geldi. Lenfoma oranı (%95 güven aralığı) Humira ile tedavi edilen hastalarda 1.000 hasta yılı başına 0,7 (0,2, 3,0) ve kontrol hastalarında 1000 hasta yılı başına 1,5 (0,4, 5,8) idi.
Bu çalışmaların bölümleri ve hem devam eden hem de tamamlanmış açık etiketli uzatma çalışmaları, 5.727 hasta dahil olmak üzere ortalama yaklaşık 3.4 yıl ve 24.568 hasta-yıldan fazla tedavi ile birleştirildiğinde, lenfoma ve melanotik olmayanlar dışında gözlenen neoplazma oranı cilt kanseri, 1000 hasta-yılı başına yaklaşık 8.8'dir. Gözlenen melanotik olmayan cilt kanseri oranı yaklaşık 1000 hasta-yılı başına 10.3'tür ve gözlenen lenfoma oranı 1.000 hasta-yılı için yaklaşık 1,4'tür.
Ocak 2003'ten Aralık 2010'a kadar olan bir pazarlama sonrası deneyimde, özellikle romatoid artritli hastalarda, rapor edilen neoplazma oranı 1.000 tedavi / hasta yılı için yaklaşık 2,7'dir. Melanotik olmayan cilt kanserleri ve lenfomalar için rapor edilen oranlar, 1000 tedavi/hasta yılı için sırasıyla yaklaşık 0,2 ve 0,3'tür (bkz. bölüm 4.4).
Adalimumab ile tedavi edilen hastalarda pazarlama sonrası deneyimde nadir hepatosplenik T hücreli lenfoma vakaları bildirilmiştir (bkz. bölüm 4.4).
otoantikorlar
Romatoid artrit IV çalışmalarında, hasta serum numuneleri çeşitli vesilelerle otoantikorlar için test edilmiştir.Bu çalışmalarda, kayıt sırasında antinükleer antikor değerleri negatif olan HUMIRA ile tedavi edilen hastaların %11,9'u ve plasebo ve aktif kontrollü hastaların %8,1'i 24. haftada pozitif değerlere sahipti. Tüm romatoid artrit ve Psöriatik artritte HUMIRA ile tedavi edilen 3.441 hastadan ikisi, lupus benzeri bir sendromun başlangıcını gösteren klinik belirtiler gösterdi. Tedavinin kesilmesinden sonra hastalar düzeldi. Hiçbir hastada lupus nefriti veya santral gelişme sinir sistemi belirtileri.
Hepato-biliyer olaylar
Kontrol süresi 4 ila 104 hafta olan romatoid artritli ve psoriatik artritli hastalarda Humira'nın kontrollü Faz 3 klinik çalışmalarında, HUMIRA ile tedavi edilen hastaların %3,7'sinde maksimum normal değerin 3 katına eşit veya daha fazla ALT transaminaz yükselmeleri meydana geldi. hastalar ve kontrol ile tedavi edilen hastaların %1.6'sı.
Kontrol periyodu süresi 12 ila 24 hafta arasında değişen plak psöriazisli hastalarda Humira'nın kontrollü Faz 3 klinik çalışmalarında, HUMIRA ile tedavi edilen hastaların %1.8'inde ve maksimum normal değerin 3 katına eşit veya daha fazla ALT yükselmeleri meydana geldi. Kontrol ile tedavi edilen hastaların yüzdesi.
4 ila 17 yaşları arasındaki poliartiküler jüvenil idiyopatik artrit hastalarında ve 6 ila 17 yaşları arasındaki entezit ile ilişkili artritli hastalarda Humira'nın kontrollü Faz 3 klinik çalışmalarında, ALT yükselmeleri 3 kat ULN'ye eşit veya daha fazla HUMIRA ile tedavi edilen hastaların %6.1'inde ve kontrol ile tedavi edilen hastaların %1.3'ünde meydana geldi. ALT transaminaz yükselmelerinin çoğu, metotreksatın eşzamanlı kullanımı ile meydana gelmiştir.
Kontrol süresi 4 ila 52 hafta arasında değişen Crohn hastalığı ve ülseratif koliti olan hastalarda Humira'nın kontrollü Faz 3 klinik çalışmalarında, HUMIRA ile tedavi edilen hastaların %0.9'unda maksimum normal değerin 3 katına eşit veya daha fazla ALT transaminaz yükselmeleri meydana geldi. hastalar ve kontrol ile tedavi edilen hastaların %0.9'u.
Humira'nın Chron hastalığı olan pediatrik hastalarda yapılan ve 52 haftaya kadar kiloya göre ayarlanmış indüksiyon tedavisini takiben idame tedavisi için iki kiloya göre ayarlanmış doz rejiminin güvenliliğini ve etkililiğini değerlendiren Faz 3 çalışmasında, ALT seviyeleri ≥ 3 x ULN bulunmuştur. Bazal immünosupresanlarla eşzamanlı tedaviye maruz kalan tüm hastaların %2,6'sı.
Klinik çalışmalarda, tüm endikasyonlarda, yüksek transaminaz düzeyleri olan hastalar asemptomatikti ve çoğu durumda yükselmeler geçiciydi ve tedavi sırasında düzeldi. Bununla birlikte, adalimumab ile tedavi edilen hastalarda, pazarlama sonrası karaciğer yetmezliği vakalarının yanı sıra, otoimmün hepatit dahil hepatit gibi karaciğer yetmezliğinden önce gelebilen daha az şiddetli karaciğer bozuklukları da bildirilmiştir.
Azatioprin / 6-merkaptopurin ile eşzamanlı tedavi
Yetişkin Crohn hastalığı çalışmalarında, tek başına Humira ile karşılaştırıldığında, Humira ve azatioprin / 6-merkaptopurin kombinasyonu ile ciddi enfeksiyonlar ve malignitelerle ilgili advers olay insidansı daha yüksek gözlenmiştir.
Şüpheli advers reaksiyonların raporlanması
İlacın ruhsatlandırılmasından sonra meydana gelen şüpheli advers reaksiyonların raporlanması, tıbbi ürünün fayda/risk oranının sürekli olarak izlenmesine olanak sağladığı için önemlidir.Sağlık profesyonellerinden, İtalyan İlaç Kurumu aracılığıyla şüpheli advers reaksiyonları bildirmeleri istenir. , web sitesi: http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Doz aşımı
Klinik çalışmalar sırasında doza bağlı toksisite gözlenmemiştir. Değerlendirilen en yüksek doz, intravenöz olarak 10 mg/kg'lık çoklu dozlardı; bu doz, önerilen dozun yaklaşık 15 katına eşittir.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: Seçici immünosupresif ajanlar. ATC kodu: L04AB04
Hareket mekanizması
Adalimumab seçici olarak TNF'ye bağlanır ve hücre zarı TNF reseptörleri p55 ve p75 ile etkileşimini bloke ederek biyolojik işlevini nötralize eder.
Adalimumab ayrıca, lökosit göçünden sorumlu adezyon moleküllerinin seviyelerindeki değişiklikler de dahil olmak üzere TNF tarafından indüklenen veya düzenlenen biyolojik tepkileri modüle eder (IC50'si 0.1-0, 2 nM olan ELAM-1, VCAM-1 ve ICAM-1).
farmakodinamik etkiler
HUMIRA ile tedavi sonrası romatoid artritli hastalarda akut faz proteinlerinde, inflamasyon indekslerinde (C reaktif protein -PCR, eritrosit sedimantasyon hızı -VES) ve serum sitokinlerinde (IL-6) bazale göre hızlı bir düşüş gözlendi. Kıkırdak yıkımından sorumlu doku yeniden şekillenmesinde rol oynayan matriks metalloproteinazların (MMP-1 ve MMP-3) serum seviyeleri de Humira uygulamasının ardından düşmüştür.Humira ile tedavi edilen hastalar genellikle kronik inflamasyonun kan kimyası belirtilerinde iyileşme göstermiştir.
Poliartiküler Jüvenil İdiyopatik Artrit, Crohn hastalığı ve ülseratif kolit hastalarında HUMIRA ile tedaviden sonra CRP (C reaktif protein) düzeylerinde hızlı bir düşüş gözlendi. Bağırsak mukozasının endoskopik çalışmaları, adalimumab ile tedavi edilen hastalarda mukozal iyileşmeyi göstermiştir.
Klinik etkinlik ve güvenlik
Juvenil İdiyopatik Artrit (JIA)
Poliartiküler Juvenil İdiyopatik Artrit (pJIA)
HUMIRA'nın güvenliliği ve etkililiği, farklı tipte JIA başlangıcı olan (en sık olarak romatoid faktör negatif veya pozitif poliartrit ve yaygın oligoartrit) aktif poliartiküler veya poliartiküler seyirli jüvenil idiyopatik artritli çocuklarda yapılan iki çalışmada (pJIA I ve II) değerlendirilmiştir.
pJIA-I
HUMIRA'nın güvenliliği ve etkililiği, poliartiküler jüvenil idiyopatik artritli (JIA) 171 çocukta (4-17 yaş) çok merkezli, randomize, çift kör, paralel gruplu bir çalışmada değerlendirilmiştir. = OL LI, hastalar MTX (metotreksat) grubu ve MTX ile tedavi edilmeyen grup olmak üzere iki gruba ayrıldı. Hastalara sabit dozlarda nonsteroidal antiinflamatuar ilaçlar (NSAID'ler) ve/veya prednizon (≤0.2 mg/kg/gün veya maksimum 10 mg/gün) verildi OL LI fazı sırasında, tüm hastalara HUMIRA 24 mg/gün verildi. m2 maksimum 40 mg doza kadar 16 hafta boyunca iki haftada bir Hastaların yaşa göre dağılımı ve OL LI fazı sırasında uygulanan minimum, ortalama ve maksimum doz Tablo 3'te gösterilmiştir.
Tablo 3
OL LI fazı sırasında uygulanan adalimumab dozu ve yaşa göre hastaların dağılımı
16. haftada bir pediatrik ACR30 yanıtı gösteren hastalar, Çift Kör (DB) fazına randomize edilmeye uygundu ve ek bir 32 hafta boyunca veya daha fazla olana kadar iki haftada bir maksimum 40 mg'a kadar HUMIRA 24 mg/m2 veya plasebo aldı. hastalık alevlenmesi. Hastalık alevlenmesini tanımlama kriterleri, "ACR Pediatrik çekirdek" in 6 ana kriterinden 3 veya daha fazlasının başlangıç değerine kıyasla %30'a eşit veya daha fazla (≥ %30) bir kötüleşme temelinde tanımlandı. 2 veya daha fazla aktif eklemin varlığı ve yukarıdaki 6 kriterden en fazla 1'inde %30'dan fazla iyileşme temelinde 32 hafta sonra veya hastalık alevlenmesi meydana geldiğinde, hastalar tedaviye kabul edilmeye uygun kabul edildi. açık uzatma aşaması.
Tablo 4
JIA çalışması sırasında PedACR 30 yanıtı
48. haftada bir PedACR 30/50/70 yanıtları, plasebo ile tedavi edilen hastalarda elde edilenlerden önemli ölçüde daha yüksekti
bp = 0.015
cp = 0.031
Tedaviye 16. haftada yanıt verenler arasında (n = 144), Ped ACR 30/50/70/90 yanıtları, tüm stüdyo boyunca Humira alan hastalarda OLE fazı sırasında altı yıla kadar korunmuştur. Genel olarak, 4 ila 12 yaşları arasındaki baz gruptan 11 ve 13 ila 17 yaşları arasındaki baz gruptan 8 olmak üzere 19 süje 6 yıl veya daha uzun süre tedavi edildi.
Genel tepkiler genellikle daha iyiydi Ve Humira ve MTX kombinasyon tedavisi ile tedavi edildiğinde, tek başına verilen Humira tedavisine kıyasla birkaç hastada antikor gelişti. Bu sonuçlar göz önünde bulundurularak, MTX kullanımı önerilmeyen hastalarda HUMIRA'nın MTX ile kombinasyon halinde ve monoterapi olarak kullanılması önerilir (bkz. bölüm 4.2).
pJİA II
Humira'nın güvenliği ve etkinliği, 32 çocukta (Humira'nın 2-2 vücut yüzey alanı, en az 24 hafta boyunca tek bir subkutan doz olarak iki haftada bir maksimum 20 mg'a kadar) açık etiketli çok merkezli bir çalışmada değerlendirildi. çalışmada, çoğu denek aynı anda MTX kullanıyordu ve bazı denekler kortikosteroid veya nonsteroidal anti-inflamatuar ilaçların (NSAID'ler) kullanıldığını bildirdi.
12. haftada ve 24. haftada PedACR30 yanıtı, gözlemlenen veri yaklaşımı kullanılarak sırasıyla %93.5 ve %90.0 idi.12. haftada ve 24. haftada PedACR50 / 70/90 olan deneklerin oranları sırasıyla %90.3 / %61.3 idi. / %38.7 ve %83.3 / %73.3 / %36.7 24. haftada yanıt verenler (PedACR30) arasında (n = 27/30), PedACR30 yanıtları, bu süre boyunca HUMIRA alan hastalarda 60 haftaya kadar korunmuştur. -etiket uzatma çalışması Toplamda 20 denek 60 hafta veya daha uzun süre tedavi edildi.
Entezit ile ilişkili artrit
HUMIRA'nın güvenliliği ve etkililiği, orta dereceli artrit ile ilişkili enteziti olan 46 pediyatrik hastada (6 ila 17 yaş) çok merkezli, randomize, çift kör bir çalışmada değerlendirilmiştir. alan, maksimum 40 mg'a kadar, veya 12 hafta boyunca iki haftada bir plasebo Çift kör dönemi, hastaların HUMIRA 24 mg / m2 vücut yüzey alanı aldığı açık etiketli bir çalışma dönemi izledi. 192 hafta boyunca iki haftada bir maksimum 40 mg subkutan olarak Birincil sonlanım noktası, başlangıçtan 12. haftaya kadar aktif artritli eklem sayısındaki değişim yüzdesiydi (deformiteye bağlı olmayan şişme veya hareket kaybı artı ağrılı eklemler ve/veya hassasiyet) ve ortalama %-62.6'lık bir düşüşle elde edildi (ortalama yüzde değişim - %88,9), plasebo grubundaki hastalarda ise -%11,6 (medyan yüzde değişim - %50,0). Artritli aktif eklem sayısındaki iyileşme, çalışmanın açık etiketli süresi boyunca 52. haftaya kadar korunmuştur. İstatistiksel olarak anlamlı olmasa da, çoğu hasta, entezit bölgelerinin sayısı, ağrılılık gibi ikincil sonlanım noktasında klinik iyileşme göstermiştir. eklem sayısı (TJC), şişmiş eklem sayısı (SJC), Pediatrik ACR 50 yanıtı ve Pediatrik ACR 70 yanıtı.
Yetişkin romatoid artrit
Humira, romatoid artritteki tüm klinik çalışmalarda 3.000'den fazla hastada değerlendirilmiştir.Humira'nın etkililiği ve güvenliği beş randomize, çift kör, iyi kontrollü çalışmada değerlendirilmiştir. Bazı hastalar 120 aya kadar tedavi görmüştür.
RA çalışması I, haftada 12.5 ila 25 mg (metotreksata karşı toleranssızsa 10 mg) arasında değişen dozlarda metotreksat dahil en az bir DMARD'a dirençli orta ila şiddetli romatoid artriti olan ve metotreksat dozu devam eden 18 yaş ve üzeri 271 hastada yürütülmüştür. haftada 10-25 mg sabit. 24 hafta boyunca iki haftada bir Humira 20, 40 veya 80 mg veya plasebo verildi.
AR II Çalışması, en az bir DMARD ilacına yetersiz yanıt veren orta ila şiddetli romatoid artritli ≥ 18 yaş 544 hastayı inceledi. 20 veya 40 mg Humira dozları, iki haftada bir plasebo ile birlikte subkutan enjeksiyon yoluyla iki haftada bir veya 26 hafta boyunca her hafta verildi; plasebo her hafta aynı süre boyunca verildi. Diğer DMARD'ların kullanımına izin verilmedi.
AR III çalışmasına, orta ila şiddetli aktif romatoid artritli, 12.5 ila 25 mg arasında değişen dozlarda metotreksat tedavisine yetersiz yanıt veren veya her hafta 10 mg metotreksata intoleransı olan, 18 yaş ve üzeri 619 hasta dahil edilmiştir. Bu çalışmada 3 grup oluşturulmuştur. İlki, 52 hafta boyunca her hafta plasebo enjeksiyonları aldı. İkincisi 52 hafta boyunca haftada 20 mg Humira alırken, üçüncüsü iki haftada bir 40 mg Humira ve iki haftada bir plasebo enjeksiyonları aldı. İlk 52 haftanın tamamlanmasının ardından 457 hasta, Humira / MTX'in 10 yıla kadar iki haftada bir 40 mg'lık bir dozda uygulandığı açık etiketli bir uzatma fazına alındı.
AR IV çalışması, ilk olarak ≥ 18 yaşında orta ila şiddetli aktif romatoid artritli 636 hastada Humira'nın güvenliğini değerlendirdi. Çalışma popülasyonu, hem DMARD ile hiç tedavi edilmemiş hastalardan hem de minimum 28 gün boyunca stabil olması koşuluyla önceden mevcut anti-romatizmal tedaviye devam eden hastalardan oluşuyordu. Bu tedaviler metotreksat, leflunomid, hidroksiklorokin, sülfasalazin ve/veya altın tuzlarını içerir Hastalar 24 hafta boyunca iki haftada bir HUMIRA 40 mg veya plasebo almak üzere randomize edilmiştir.
AR çalışması V, daha önce metotreksat ile tedavi edilmemiş ve orta ila şiddetli erken aktif romatoid artriti (ortalama hastalık süresi 9 aydan az) olan 799 yetişkin hastayı değerlendirdi. Bu çalışma, iki haftada bir metotreksat ile kombinasyon tedavisinde verilen HUMIRA 40 mg'ın, iki haftada bir monoterapi olarak verilen Humira 40 mg'ın ve tek başına metotreksatın hastalığın belirti ve semptomlarını ve romatoid artritin neden olduğu eklem hasarının ilerleme indeksini azaltmadaki etkinliğini değerlendirdi. 104 hafta boyunca.
AR çalışmaları I, II, III'ün birincil son noktası ve AR IV'ün ikincil son noktaları, 24 veya 26. haftada bir ACR 20 yanıtına ulaşan hastaların oranını değerlendirmekti. AR V çalışmasının birincil amacı, 52. haftada bir ACR 50 yanıtına ulaşan hastaların yüzdesi. Ek olarak, AR çalışmaları III ve V, 52. haftada hastalık progresyonunun inhibisyonunu (radyografik muayeneler yoluyla) gösterme ana amacına sahipti. AR çalışması III'ün de birincil amacı vardı. yaşam kalitesinin arttığını göstermektir.
ACR yanıtı
ACR 20, 50 ve 70 yanıtlarına ulaşan Humira ile tedavi edilen hastaların yüzdeleri, AR çalışmaları I, II ve III'te karşılaştırılabilirdi.Her iki haftada bir 40 mg ile tedaviye ilişkin sonuçlar Tablo 5'te özetlenmiştir.
RA çalışmaları I-IV'te ACR yanıtının tanımlanması için değerlendirilen tüm parametreler (ağrılı ve şiş eklem sayısı, doktor ve hasta tarafından hastalık aktivitesinin değerlendirilmesi, hasta tarafından ağrının değerlendirilmesi, sakatlık indeksi - HAQ) ve CRP değerleri (mg / dL) plaseboya kıyasla 24 veya 26 haftada düzeldi AR III çalışmasında, bu gelişmeler 52 hafta boyunca korundu.
AR III çalışmasının açık etiketli uzatma aşamasında, ACR yanıtı yaşayan çoğu hasta tedaviye 10 yıl devam ettiklerinde yanıtı korumuştur. Toplam 207 hastanın 114'ü 5 yıl boyunca iki haftada bir 40 mg HUMIRA almaya devam etti. Bunlardan 86 hastada (%75.4) ACR 20 yanıtı vardı; 72 hastada (%63.2) ACR 50 yanıtı vardı; ve 41 hastada (%36) ACR 70 yanıtı vardı Toplam 207 hastanın 81'i 10 yıl boyunca iki haftada bir HUMIRA 40 mg ile tedaviye devam etti. Bunlardan 64 hastada (%79.0) ACR 20 yanıtı vardı; 56 hastada (%69.1) ACR 50 yanıtı vardı; ve 43 hastada (%53.1) ACR 70 yanıtı vardı.
AR IV çalışmasında, geleneksel tedaviyle kombinasyon halinde HUMIRA ile tedavi edilen hastaların ACR 20 yanıtı, geleneksel ilaçlarla kombine edilmiş plasebo ile tedavi edilen hastalardan istatistiksel olarak anlamlı derecede daha iyiydi (p
RA çalışmaları I-IV'te, HUMIRA ile tedavi edilen hastalar, tedaviye başladıktan 1-2 hafta sonra plaseboya göre istatistiksel olarak anlamlı derecede daha yüksek ACR 20 ve 50 yanıtları elde etmiştir.
RA çalışması V'de, daha önce metotreksat ile tedavi edilmemiş erken romatoid artritli hastalarda, 52. haftada Humira / metotreksat kombinasyon tedavisi metotreksat monoterapisine ve HUMIRA monoterapisine göre daha hızlı ve anlamlı derecede daha fazla ACR yanıtı ile sonuçlanmıştır ve bu yanıtlar 104 hafta boyunca devam etmiştir ( bkz. Tablo 6).
52. haftada, HUMIRA / metotreksat kombinasyon tedavisi alan hastaların %42.9'u klinik remisyona ulaşmıştır (DAS28).
radyolojik yanıt
Humira ile tedavi edilen hastaların ortalama hastalık süresinin yaklaşık 11 yıl olduğu AR çalışması III'te, yapısal hasar radyografik olarak değerlendirildi ve modifiye Total Sharp Skoru (TSS) ve ilgili bileşenlerde, erozyon ve eklem boşluğu daralmasında bir değişiklik olarak ifade edildi ( JSN) indeksleri Humira / MTX ile tedavi edilen hastalar, 6 ve 12 ayda tek başına MTX alan hastalardan önemli ölçüde daha az radyolojik progresyon gösterdi (bkz. Tablo 7).
AR çalışması III'ün açık etiketli uzantısında, yapısal hasarın ilerleme hızındaki azalma, bir hasta alt grubunda 8 ve 10 yıl boyunca korunur.8 yılda, başlangıçta her biri 40 mg HUMIRA ile tedavi edilen 207 hastanın 81'i diğer haftalar Bunlar arasında, 48 hasta, mTSS'de başlangıca göre 0,5 veya daha az bir değişiklikle tanımlanan yapısal hasarda ilerleme göstermedi.10 yılda, iki haftada bir 40 mg HUMIRA ile tedavi edilen 207 hastanın 79'u, bunlardan 40'ı mTSS'de taban çizgisinden 0,5 veya daha az bir değişiklikle tanımlanan yapısal hasarın ilerlemesini göstermez.
Tablo 7
AR III çalışmasında 12 ay sonra ortalama radyografik değişiklik
metotreksat yapmak
b Metotreksat ve Humira arasındaki indeks değişikliklerindeki farklılıklar için %95 güven aralığı.
c Sıra analizine dayalıdır.
d Ortak Alan Daraltma (eklem boşluğunun azaltılması).
AR çalışması V'de, yapısal eklem hasarı radyografik olarak değerlendirildi ve modifiye Toplam Keskin Skordaki değişiklik açısından ifade edildi (bkz. Tablo 8).
52 hafta ve 104 haftalık tedaviden sonra, ilerleme göstermeyen hastaların oranı (modifiye Total Sharp Skorunda başlangıca göre değişiklik ≤ 0,5), metotreksat monoterapisine kıyasla Humira / metotreksat kombinasyon tedavisi ile (sırasıyla %63.8 ve %61,2) anlamlı olarak daha yüksekti. (sırasıyla %37.4 ve %33.5, p
Yaşam kalitesi ve fiziksel fonksiyon
Yaşam kalitesi ve fiziksel işlev, Sağlık Değerlendirme Anketi (HAQ) aracılığıyla elde edilen sakatlık indeksi ile dört orijinal, yeterli ve iyi kontrollü çalışmada değerlendirildi ve 52. haftadaki AR çalışması III'ün birincil son noktalarından biriydi. Dört çalışmadaki Humira rejimleri, plaseboya kıyasla başlangıç ve 6. ay arasında HAQ sakatlık indeksinde istatistiksel olarak anlamlı iyileşmeler gösterdi ve AR çalışması III'te aynı sonuç 52. haftada gözlemlendi. Short tarafından değerlendirilen genel sağlık durumu analizi Dört çalışmadaki Form Sağlık Anketi (SF -36), tüm Humira doz rejimleri için bu sonuçları istatistiksel olarak anlamlı sonuçlarla desteklemektedir. dönüşümlü. Kronik hastalık tedavisine (FACIT) ilişkin fonksiyonel değerlendirme endeksleri tarafından gösterildiği gibi yorgunluk hissinde istatistiksel olarak anlamlı bir azalma, değerlendirildiği üç çalışmanın hepsinde (çalışma AR I, III, IV) bulundu.
AR III çalışmasında, fiziksel işlevde iyileşme elde eden ve tedaviye devam eden deneklerin çoğu, 520 hafta (120 ay) açık etiketli tedavi boyunca iyileşmeyi sürdürmüştür. Yaşam kalitesindeki iyileşme 156. haftaya (36 ay) kadar ölçülmüştür ve iyileşme zamanla korunmuştur.
AR çalışması V'de, HAQ ve SF 36'nın fiziksel bileşeni temelinde değerlendirilen sakatlık indeksi üstün bir gelişme gösterdi (p
Pediatrik hastalarda Crohn hastalığı
Humira, ağırlığa bağlı doza bağlı indüksiyon ve idame tedavisinin etkililiğini ve güvenliğini değerlendirmek için tasarlanmış çok merkezli, randomize, çift kör bir klinik çalışmada test edilmiştir (30. Denekler, bir kortikosteroid ve/veya bir immünomodülatör dahil olmak üzere geleneksel tedavide başarısız olmuş olmalıdır). ) CD için ve denekler daha önce yanıt kaybetmiş veya infliximab'a karşı toleranssız olabilir.
Tüm denekler, başlangıçtaki vücut ağırlıklarına dayalı bir dozla açık etiketli indüksiyon tedavisi almıştır: ≥ 40 kg ağırlığındaki denekler için 0. haftada 160 mg ve 2. haftada 80 mg ve kilolu denekler için 80 mg ve 40 mg.
4. haftada, vücut ağırlıklarına bağlı olarak denekler Tablo 9'da gösterildiği gibi Düşük Doz veya Standart Doz idame rejimlerine 1:1 oranında randomize edilmiştir.
Etkinlik sonuçları
Çalışmanın birincil sonlanım noktası, PCDAI skoru ≤ 10 ile tanımlanan 26. haftada klinik remisyon olmuştur.
Klinik remisyon ve klinik yanıt oranları (başlangıca göre en az 15 puanlık PCDAI puan azalması olarak tanımlanır) Tablo 10'da gösterilmiştir. Kortikosteroid veya immünomodülatörün kesilme oranları Tablo 11'de gösterilmektedir.
Her iki tedavi grubu için Vücut Kitle İndeksinde ve başlangıçtan 26. ve 52. Haftaya kadar büyüme hızında istatistiksel olarak anlamlı artışlar (iyileştirmeler) gözlendi.
Her iki tedavi grubunda da yaşam kalitesi parametrelerinde (IMPACT III dahil) başlangıca göre istatistiksel ve klinik olarak anlamlı iyileşmeler gözlendi.
Yetişkinlerde Crohn hastalığı
Humira'nın güvenliliği ve etkililiği, orta ila şiddetli derecede aktif Crohn Hastalığı (Crohn Hastalığı Aktivite İndeksi (CDAI) ≥ 220 ve ≤ 450) olan 1500'den fazla hastada randomize, çift kör, plasebo kontrollü çalışmalarda değerlendirilmiştir. Sabit dozlarda aminosalisilatlar, kortikosteroidler ve/veya immünomodülatör ajanların birlikte uygulanmasına izin verildi ve hastaların %80'i bu ilaçlardan en az birini almaya devam etti.
Klinik remisyon indüksiyonu (CDAI olarak tanımlanır)
Klinik remisyonun sürdürülmesi CD III (CHARM) çalışmasında değerlendirildi. CD çalışması III'te 854 hasta 0. haftada 80 mg ve 2. haftada 40 mg açık etiketli HUMIRA almıştır. 4. haftada, hastalar iki haftada bir 40 mg, haftada bir 40 mg veya plasebo alacak şekilde randomize edilmiştir; çalışmanın toplam süresi 56 haftadır. 4. haftada yeterli klinik yanıt (CDAI düşüşü ≥ 70) sergileyen hastalar katmanlara ayrıldı ve 4. haftada yeterli klinik yanıt göstermeyen hastalardan ayrı olarak analiz edildi. 8. haftadan sonra kortikosteroid dozunun kademeli olarak azaltılması.
Klinik remisyon indüksiyon oranları ve CD çalışması I ve CD çalışması II'den alınan yanıt Tablo 12'de gösterilmektedir.
8. haftada 160/80 mg ve 80/40 mg indüksiyon doz grubunda benzer remisyon oranları gözlendi ve 160/80 mg doz grubunda advers olaylar daha sık meydana geldi.
CD çalışması III'te 4. haftada hastaların %58'i (499/854) yeterli bir klinik yanıt yaşadı ve birincil analizde değerlendirildi 4. haftada yeterli klinik yanıt elde edilen hastaların %48'i daha önce diğer TNF antagonist ilaçlarla terapi Remisyonu sürdürme ve klinik yanıt için yüzdeler Tablo 13'te gösterilmektedir.
56. haftada, plaseboya kıyasla adalimumab ile hastaneye yatışlar ve hastalıkla ilgili cerrahiler istatistiksel olarak anlamlı ölçüde azaldı.
4. haftada yeterli yanıt vermeyen hastalardan, HUMIRA idame tedavisi ile tedavi edilen hastaların %43'ü, plasebo ile tedavi edilen hastaların %30'u ile karşılaştırıldığında, 12. haftada yeterli yanıt elde etmiştir. Bu sonuçlar, 4. haftada yeterli yanıt göstermeyen bazı hastaların 12. haftaya kadar devam eden idame tedavisinden fayda gördüğünü göstermektedir. Tedavinin 12 haftanın üzerinde devam etmesi, önemli ölçüde daha yüksek sayıda yanıta yol açmamıştır (bkz. bölüm 4.2).
CD çalışması I'den 117/276 hasta ve CD çalışmaları II ve III'ten 272/777 hasta en az 3 yıl açık etiketli adalimumab tedavisi için takip edildi. Sırasıyla 88 ve 189 hasta klinik remisyon sağlamaya devam etti. Klinik yanıt (CR-100) sırasıyla 102 ve 233 hastada korunmuştur.
Yaşam kalitesi
Çalışma CD I ve CD II'de, plaseboya kıyasla HUMIRA 80/40 mg ve 160/80 mg'a randomize edilen hastalarda hastalığa özgü inflamatuar bağırsak hastalığı anketi (IBDQ) toplam skorunda istatistiksel olarak anlamlı iyileşme 4. haftada elde edildi ve Çalışma D III'te 26. ve 56. haftaların yanı sıra plasebo grubuna kıyasla Humira tedavi grupları arasında
immünojenisite
Anti-adalimumab antikorlarının oluşumu, adalimumabın artan klirensi ve azalmış etkinliği ile ilişkilidir. Anti-adalimumab antikorlarının varlığı ile advers olayların başlangıcı arasında belirgin bir ilişki yoktur.
4-17 yaş arası poliartiküler jüvenil idiyopatik artrit hastalarında, adalimumab ile tedavi edilen hastaların %15,8'inde (27/171) anti-adalimumab antikorları tespit edilmiştir. HUMIRA ile metotreksat verilmeyen hastalarda, adalimumab metotreksat ile birlikte kullanıldığında insidans %25.6 (22/86) iken %5.9 (5/85) olmuştur.
Entezit ile ilişkili artritli hastalarda, adalimumab ile tedavi edilen hastaların %10,9'unda (5/46) anti-adalimumab antikorları tespit edilmiştir. HUMIRA ile birlikte metotreksat verilmeyen hastalarda, insidans %13.6 (3/22), adalimumab metotreksat ile kombinasyon halinde kullanıldığında %8.3 (2/24) idi.
Romatoid artrit çalışmalarında hastalar 6 ila 12 aylık dönem boyunca çeşitli zaman aralıklarında adalimumab antikorları açısından taranmıştır.Pivotal klinik çalışmalarda, adalimumab ile tedavi edilen hastaların %5.5'inde (58/1053) adalimumab antikorları saptanmıştır. plasebo ile tedavi edilen hastaların %0.5'i (2/370) ile birlikte metotreksat verilmeyen hastalarda, insidans %12.4 iken, adalimumab metotreksat ile kombinasyon halinde kullanıldığında bu oran %0.6'dır.
İmmünojenisite testleri ürüne özel olduğundan, diğer ürünlerle antikor miktarlarının karşılaştırılması uygun değildir.
05.2 Farmakokinetik özellikler
Emilim ve dağıtım
4 ila 17 yaşları arasındaki poliartiküler jüvenil idiyopatik artritli (JIA) hastalara iki haftada bir 24 mg / m2 (maksimum 40 mg'a kadar) subkutan uygulamadan sonra, serum adalimumab konsantrasyonunun ortalama minimum denge değeri (20. haftadan itibaren ölçülen değerler) adalimumab ile birlikte metotreksat kullanılmadan ve metotreksat ile birlikte uygulanan 10.9 ± 5.2 μg/mL (47 , %7 CV) ile 5.6 ± 5.6 μg / mL (%102 CV) idi.
Yaşları 2 ila 2 arasında değişen poliartiküler JİA'lı hastalarda, adalimumabın ortalama çukur denge serum konsantrasyonu, adalimumab ile birlikte metotreksat kullanımı olmaksızın 6.0 ± 6.1 mcg / mL (%101 CV) ve 7.9 ± 5.6 mcg / mL (%71.2 CV) olmuştur. metotreksat ile birlikte uygulandığında.
Entezit ile ilişkili artriti olan 6-17 yaş arası hastalara iki haftada bir 24 mg/m2 (maksimum 40 mg'a kadar) subkutan uygulamayı takiben, kararlı durumda adalimumab serum konsantrasyonlarının ortalama minimum değeri (ölçülen değerler ) 24. haftada) metotreksat ile birlikte kullanılmadan adalimumab ile 8.8 ± 6.6 mcg / mL ve metotreksat ile birlikte uygulandığında 11.8 ± 4.3 mcg / mL idi.
Orta ila şiddetli CD'si olan pediyatrik hastalarda, açık etiketli adalimumabın indüksiyon dozu, 40 kg'da vücut ağırlığı kesme değerine bağlı olarak 0. ve 2. haftalarda sırasıyla 160/80 mg veya 80/40 mg olmuştur. 4. haftada, hastalar standart Doz (iki haftada bir 40/20 mg) veya Düşük Doz (iki haftada bir 20/10 mg) tedavi grubuna vücut ağırlığına göre 1:1 oranında randomize edilmiştir. 4. haftada ulaşılan adalimumab dip seviyelerinin ortalama (± SD) serum konsantrasyonları, hastalar ≥ 40 kg (160/80 mg) için 15.7 ± 6.6 mg / mL ve hastalar için 10.6 ± 6.1 mg / mL idi.
Randomize tedavilerine devam eden hastalar için, 52. haftada adalimumabın ortalama (± SD) dip konsantrasyonları, standart doz grubu için 9,5 ± 5,6 mg/mL ve Düşük Doz grubu için 3,5 ± 2,2 mg/mL idi. 52 hafta boyunca iki haftada bir adalimumab tedavisi almaya devam eden hastalarda ortalama dip konsantrasyonları korunmuştur. Dozu alternatif haftadan haftalık rejime yükselten hastalar için 52. haftada ortalama (± SD) adalimumab serum konsantrasyonları 15.3 ± 11.4 mcg / mL (haftada 40/20 mg) ve 6.7 ± 3.5 mcg / idi. mL (haftada 20/10 mg).
yetişkinler
Tek bir 40 mg dozun subkutan uygulamasını takiben, adalimumabın absorpsiyon ve dağılımı yavaştı ve uygulamadan yaklaşık 5 gün sonra doruk serum konsantrasyonları meydana geldi. 0.25 ila 10 mg/kg'lık tek intravenöz dozlardan sonra, konsantrasyonlar dozla orantılıydı.0.5 mg/kg'lık (≈40 mg) dozlardan sonra, klirens 11 ila 15 mL/saat arasında değişiyordu, dağılım hacmi (Vss) değişiyordu. 5 ila 6 litre arasındaydı ve son fazın ortalama yarı ömrü yaklaşık iki haftaydı. Çeşitli romatoid artrit hastalarında sinovyal sıvıdaki adalimumab konsantrasyonları, serumdakilerin %31-96'sı arasında değişmiştir.
Romatoid artritli (RA) yetişkin hastalarda iki haftada bir 40 mg adalimumabın subkutan uygulamasını takiben, dip konsantrasyonlar ortalama yaklaşık 5 mg/ml (eş zamanlı metotreksat olmadan) ve 8-9 mg/ml (metotreksat ile kombinasyon halinde) olmuştur. 2 haftada bir veya haftada bir 20, 40 ve 80 mg'lık subkutan dozları takiben dengedeki adalimumab seviyeleri, neredeyse doza bağlı bir şekilde arttı.
Eliminasyon
1.300'den fazla RA hastasından oluşan bir numune üzerinde yapılan popülasyon farmakokinetik analizleri, vücut ağırlığı arttıkça adalimumab klerensinde belirgin bir artışa doğru bir eğilim göstermiştir.Vücut ağırlığı için düzeltmeden sonra, cinsiyet ve yaş farklılıklarının adalimumab klirensi üzerinde minimal etkiye sahip olduğu bulunmuştur. serbest adalimumab (anti-adalimumab antikorlarına bağlı olmayan - AAA) ölçülebilir AAA titreleri olan hastalarda daha düşüktü Humira, böbrek yetmezliği veya karaciğer yetmezliği olan hastalarda çalışılmamıştır.
Karaciğer veya böbrek yetmezliği
HUMIRA, karaciğer veya böbrek yetmezliği olan hastalarda çalışılmamıştır.
05.3 Klinik öncesi güvenlik verileri
Klinik olmayan veriler, tek doz toksisite, tekrarlanan doz toksisitesi ve genotoksisite çalışmalarına dayalı olarak insanlar için özel bir tehlike ortaya koymamaktadır.
Sinomolojik maymunlarda 0, 30 ve 100 mg/kg (9-17 maymun/grup) dozlarında bir embriyo-fetal gelişim/perinatal gelişim toksisite çalışması yapılmıştır; bu çalışma, adalimumabın neden olduğu herhangi bir fetal zarar ortaya koymadı.Kemirgenlerde TNF'ye sınırlı çapraz reaktiviteye sahip bir antikor için uygun modellerin bulunmaması ve kemirgenlerde nötralize edici antikorların geliştirilmesi nedeniyle kanserojenlik testi ve standart doğurganlık ve doğum sonrası toksisite değerlendirmeleri yapılmamıştır.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
mannitol
Sitrik asit monohidrat
Sodyum sitrat
Sodyum monobazik fosfat dihidrat
disodyum fosfat dihidrat
Sodyum klorit
polisorbat 80
Sodyum hidroksit
Enjeksiyonlar için su.
06.2 Uyumsuzluk
Uyumluluk çalışmaları bulunmadığından, bu tıbbi ürün diğer tıbbi ürünlerle karıştırılmamalıdır.
06.3 Geçerlilik süresi
24 ay
06.4 Depolama için özel önlemler
Buzdolabında (2°C - 8°C) saklayınız. Dondurmayın. İlacı ışıktan korumak için flakonu kartonda saklayınız.
06.5 İç ambalajın yapısı ve paketin içeriği
HUMIRA 40 mg enjeksiyonluk çözelti, tek dozluk bir flakonda (tip I cam), kauçuk tıpalarla kapatılmış, bir alüminyum tabaka ile kaplanmış ve bir geçmeli kapak içinde bulunur.
Her biri aşağıdakileri içeren 2 kutudan oluşan 1 paket:
1 flakon (0,8 ml steril solüsyon), 1 boş steril şırınga, 1 iğne, 1 flakon adaptörü ve 2 alkollü bez.
06.6 Kullanım ve kullanım talimatları
HUMIRA 40 mg enjeksiyonluk solüsyon koruyucu içermez. Kullanılmayan ilaçlar ve bu ilaçtan kaynaklanan atıklar yerel yönetmeliklere uygun olarak atılmalıdır.
07.0 PAZARLAMA YETKİ SAHİBİ
bakire
SL6 4XE
Birleşik Krallık
08.0 PAZARLAMA YETKİ NUMARASI
EU / 1/03/256/001 40 mg enjeksiyonluk solüsyon 1 flakon 0.8 ml + 1 şırınga + subkutan kullanım için 2 swab 035946019 / E
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
İlk izin tarihi: 8 Eylül 2003
En son yenileme tarihi: 8 Eylül 2008
10.0 METİN REVİZYON TARİHİ
09/2014