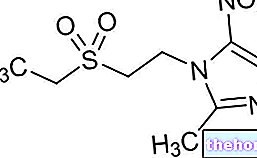
Aktif maddeler: Sitagliptin
Xelevia 25 mg film kaplı tablet
Paket boyutları için Xelevia prospektüsleri mevcuttur:- Xelevia 25 mg film kaplı tablet
- Xelevia 50 mg film kaplı tabletler
- Xelevia 100 mg film kaplı tabletler
Xelevia neden kullanılır? Bu ne için?
Xelevia, tip 2 diyabetli erişkin hastalarda kan şekeri düzeylerini düşüren dipeptidil peptidaz-4 (DPP-4) inhibitörleri adı verilen bir ilaç sınıfına ait olan sitagliptin etkin maddesini içerir.
Bu ilaç, yemekten sonra üretilen insülin seviyelerini artırmaya yardımcı olur ve vücut tarafından üretilen şeker miktarını azaltır.
Doktorunuz bu ilacı tip 2 diyabet nedeniyle çok yüksek olan kan şekeri seviyenizi düşürmenize yardımcı olması için reçete etmiştir.Bu ilaç tek başına veya kan şekerini düşüren diğer ilaçlarla (insülin, metformin, sülfonilüre veya glitazonlar) birlikte kullanılabilir. bir diyet ve egzersiz programı ile birlikte diyabetinizi tedavi etmek için alıyor olabilirsiniz.
Tip 2 diyabet nedir?
Tip 2 diyabet, vücudun yeterince insülin üretmediği ve vücut tarafından üretilen insülinin gerektiği gibi çalışmadığı bir hastalıktır.Vücut ayrıca çok fazla şeker üretebilir. Bu olduğunda, kanda şeker (glikoz) birikir.Bu, kalp hastalığı, böbrek hastalığı, körlük ve ampütasyon gibi ciddi tıbbi sorunlara yol açabilir.
Kontrendikasyonlar Xelevia ne zaman kullanılmamalıdır?
Xelevia'yı almayın
- Sitagliptine veya bu ilacın içerdiği diğer maddelerden herhangi birine karşı alerjiniz varsa.
Kullanım Önlemleri Xelevia'yı almadan önce bilmeniz gerekenler
Xelevia ile tedavi edilen hastalarda pankreas iltihabı (pankreatit) vakaları bildirilmiştir.
Aşağıdakilere sahipseniz veya olduysanız doktorunuza söyleyiniz:
- pankreas hastalığı (pankreatit gibi)
- kanda safra taşı, alkol bağımlılığı veya çok yüksek trigliserit (bir yağ türü) seviyeleri. Bu tıbbi durumlar pankreatit geliştirme riskinizi artırabilir
- tip 1 diyabet
- diyabetik ketoasidoz (yüksek kan şekeri, hızlı kilo kaybı, bulantı veya kusma ile birlikte diyabetin bir komplikasyonu)
- geçmiş veya mevcut böbrek problemleri
- Xelevia'ya karşı alerjik bir reaksiyon.
Bu ilacın düşük kan şekerine (hipoglisemi) neden olması olası değildir, çünkü kan şekeriniz düştüğünde çalışmaz. Bununla birlikte, bu ilaç bir sülfonilüre veya insülin ile birlikte alındığında (hipoglisemi) meydana gelebilir. Doktorunuz sülfonilüre veya insülin dozunu azaltabilir.
Çocuklar ve ergenler
18 yaşın altındaki çocuklar ve ergenler bu ilacı kullanmamalıdır. Çocuklarda ve 18 yaşın altındaki adolesanlarda bu ilacın kullanımının güvenli ve etkili olup olmadığı bilinmemektedir.
Etkileşimler Hangi ilaçlar veya yiyecekler Xelevia'nın etkisini değiştirebilir
Başka ilaçlar alıyorsanız, yakın zamanda aldıysanız veya alma ihtimaliniz varsa doktorunuza veya eczacınıza söyleyiniz.
Özellikle digoksin (düzensiz kalp atışı ve diğer kalp problemlerini tedavi etmek için kullanılan bir ilaç) alıyorsanız doktorunuza söyleyiniz. Xelevia ile birlikte alındığında kanınızdaki digoksin seviyesinin kontrol edilmesi gerekebilir.
Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme
Hamileyseniz veya emziriyorsanız, hamile olabileceğinizi düşünüyorsanız veya bebek sahibi olmayı planlıyorsanız, bu ilacı almadan önce doktorunuza veya eczacınıza danışınız. Hamilelik sırasında bu ilacı kullanmamalısınız.
Bu ilacın anne sütüne geçip geçmediği bilinmemektedir. Emziriyorsanız veya emzirmeniz gerektiğini düşünüyorsanız bu ilacı almamalısınız.
Araç ve makine kullanma
Bu ilacın araç ve makine kullanma yeteneği üzerinde etkisi yoktur veya ihmal edilebilir düzeydedir. Bununla birlikte, araç ve makine kullanma yeteneğinizi etkileyebilecek baş dönmesi ve uyuklama bildirilmiştir.
Bu ilacı sülfonilüreler adı verilen diğer ilaçlarla veya insülinle birlikte almak, araç kullanma, makine kullanma veya koruyucu bariyerler olmadan çalışma yeteneğinizi etkileyebilecek hipoglisemiye neden olabilir.
Doz, Yöntem ve Uygulama Süresi Xelevia nasıl kullanılır: Pozoloji
Bu ilacı her zaman tam olarak doktorunuzun size söylediği şekilde alınız. Şüpheniz varsa, doktorunuza veya eczacınıza danışın.
Önerilen olağan doz:
- bir adet 100 mg film kaplı tablet
- günde bir kez
- ağızla
Böbrek problemleriniz varsa doktorunuz daha düşük dozlar (25 mg veya 50 mg gibi) reçete edebilir.
Bu ilacı yiyecek ve içecekle birlikte veya ayrı olarak alabilirsiniz.
Doktorunuz bu ilacı tek başına veya kan şekeri seviyenizi düşüren diğer ilaçlarla birlikte reçete edebilir.
Diyet ve egzersiz vücudunuzun kan şekerini daha iyi kullanmasına yardımcı olabilir. Xelevia'yı alırken doktorunuz tarafından önerilen diyet ve egzersiz programına devam etmeniz önemlidir.
Xelevia'yı kullanmayı unutursanız
Bir dozu unutursanız, hatırladığınız anda onu alınız. Bir sonraki dozun zamanı gelene kadar hatırlamıyorsanız, unuttuğunuz dozu atlayın ve normal dozunuza devam edin.
Bu ilacın çift dozunu almayın.
Xelevia'yı kullanmayı bırakırsanız
Kan şekeri seviyenizi izlemeye devam edebilmeniz için bu ilacı doktorunuz reçete ettiği sürece almaya devam edin. İlk önce doktorunuzla konuşmadan bu ilacı almayı bırakmamalısınız.
Bu ilacın kullanımıyla ilgili başka sorularınız varsa, doktorunuza veya eczacınıza sorunuz.
Aşırı doz Xelevia'yı çok fazla aldıysanız ne yapmalısınız?
Bu ilacın reçete edilen dozundan fazlasını alırsanız, derhal doktorunuza başvurunuz.
Yan Etkiler Xelevia'nın yan etkileri nelerdir?
Tüm ilaçlar gibi, bu ilaç da yan etkilere neden olabilir, ancak bu yan etkiler herkeste görülmez.
Aşağıdaki ciddi yan etkilerden herhangi birini fark ederseniz Xelevia'yı kullanmayı DURDURUN ve hemen bir doktora başvurun:
- Mide bulantısı ve kusma ile birlikte veya bunlar olmaksızın sırta kadar uzanabilen şiddetli ve kalıcı karın ağrısı (mide bölgesi), bunlar pankreas iltihabının (pankreatit) belirtileri olabilir.
Deride döküntü, kurdeşen, kabarcıklar / deride soyulma ve yüzde, dudaklarda, dilde ve boğazda nefes alma veya yutma güçlüğüne neden olabilecek şişme gibi şiddetli bir alerjik reaksiyonunuz varsa (sıklığı bilinmiyor), bu ilaçla tedaviyi durdurun. ve derhal doktorunuzla temasa geçiniz. Doktorunuz alerjik reaksiyonunuzu tedavi etmek için bir ilaç ve diyabetiniz için farklı bir ilaç reçete edebilir.
Bazı hastalarda metformine sitagliptin eklendikten sonra aşağıdaki yan etkiler görülmüştür:
- Yaygın (10 kişiden 1'ini etkileyebilir): Düşük kan şekeri, mide bulantısı, gaz, kusma
- Yaygın olmayan (100 kişiden 1'ini etkileyebilir): mide ağrısı, ishal, kabızlık, uyku hali
Bazı hastalar kombinasyon tedavisinin bir parçası olarak sitagliptin ve metformini birlikte başlatırken farklı tiplerde mide ağrısı bildirmiştir (sıklık yaygındır).
Bazı hastalarda sülfonilüre ve metformin ile kombinasyon halinde sitagliptin alırken aşağıdaki yan etkiler görülmüştür:
- Çok yaygın (10 kişiden 1'inden fazlasını etkileyebilir): Düşük kan şekeri
- Yaygın: kabızlık
Bazı hastalarda sitagliptin ve pioglitazon alırken aşağıdaki yan etkiler görülmüştür:
- Yaygın: Gaz, ellerde veya bacaklarda şişme
Sitagliptin'i pioglitazon ve metformin ile birlikte kullanırken bazı hastalarda aşağıdaki yan etkiler görülmüştür:
- Yaygın: Ellerin veya bacakların şişmesi
İnsülin ile kombinasyon halinde sitagliptin (metforminli veya metforminsiz) alırken bazı hastalarda aşağıdaki yan etkiler görülmüştür:
- Yaygın: grip
- Yaygın olmayan: ağız kuruluğu
Bazı hastalar, klinik çalışmalarda tek başına sitagliptin alırken veya tek başına ve/veya diğer diyabet ilaçları ile onay sonrası kullanım sırasında aşağıdaki yan etkileri yaşamıştır:
- Yaygın: Düşük kan şekeri, baş ağrısı, üst solunum yolu enfeksiyonu, burun akıntısı veya tıkanıklığı ve boğaz ağrısı, osteoartrit, kollarda veya bacaklarda ağrı
- Yaygın olmayan: Baş dönmesi, kabızlık, kaşıntı
- Sıklığı bilinmiyor: böbrek sorunları (bazen diyaliz gerektirir), kusma, eklem ağrısı, kas ağrısı, sırt ağrısı, interstisyel akciğer hastalığı
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuzla, eczacınızla veya hemşirenizle konuşun.Bu broşürde listelenmeyen olası yan etkiler de buna dahildir.Yan etkileri Ek V'de listelenen ulusal raporlama sistemi aracılığıyla da doğrudan bildirebilirsiniz. Yardımcı olabileceğiniz yan etkiler Bu ilacın güvenliği hakkında daha fazla bilgi sağlayın.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
Blister ve karton üzerinde belirtilen "EXP" tarihinden sonra bu ilacı kullanmayınız. Son kullanma tarihi, o ayın son gününü ifade eder.
Bu ilaç herhangi bir özel saklama koşulu gerektirmez.
Herhangi bir ilacı atık su veya evsel atık yoluyla atmayın.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorun.Bu, çevrenin korunmasına yardımcı olacaktır.
Diğer bilgiler
Xelevia'nın içeriği
- Aktif bileşen sitagliptindir. Her film kaplı tablet (tablet), 25 mg sitagliptine eşdeğer sitagliptin fosfat monohidrat içerir.
- Diğer bileşenler şunlardır: tablet çekirdeğinde: mikrokristal selüloz (E460), susuz kalsiyum hidrojen fosfat (E341), kroskarmeloz sodyum (E468), magnezyum stearat (E470b) ve sodyum stearil fumarat. Tablet kaplaması şunları içerir: poli (vinil alkol), makrogol 3350, talk (E553b), titanyum dioksit (E171), kırmızı demir oksit (E172) ve sarı demir oksit (E172).
Xelevia'nın görünüşü ve paketin içeriği
Bir tarafında "221" yazan yuvarlak, pembe film kaplı tabletler.
Opak kabarcıklar (PVC / PE / PVDC ve alüminyum).
Delikli birim doz blisterlerde 14, 28, 30, 56, 84, 90 veya 98 film kaplı tablet ve 50 x 1 film kaplı tabletten oluşan paketler.
Tüm paket boyutları pazarlanmayabilir.
sona erme "> Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
FİLM KAPLI XELEVIA 25 MG TABLETLER
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Her tablet 25 mg sitagliptine eşdeğer sitagliptin fosfat monohidrat içerir.
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakın.
03.0 FARMASÖTİK FORM
Film kaplı tablet (tablet).
Bir tarafında "221" yazılı yuvarlak, pembe film kaplı tablet.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Tip 2 diabetes mellituslu yetişkin hastalarda Xelevia'nın glisemik kontrolü iyileştirdiği endikedir:
monoterapide
• tek başına diyet ve egzersizle yeterince kontrol edilemeyen ve kontrendikasyonlar veya intolerans nedeniyle metforminin uygun olmadığı hastalarda.
ile kombinasyon halinde ikili oral tedavide
• diyet ve egzersiz artı metformin tek başına yeterli kan şekeri kontrolü sağlamadığında metformin.
• Diyet ve egzersiz artı maksimum tolere edilen sülfonilüre dozu tek başına yeterli glisemik kontrol sağlamadığında ve kontrendikasyonlar veya intolerans nedeniyle metformin uygun olmadığında bir sülfonilüre.
• bir PPAR agonisti kullanımı uygun olduğunda bir peroksizom proliferatörü ile aktive olan reseptör gama (PPAR ??) agonisti (örneğin, bir tiazolidindion) ve diyet ve egzersiz artı PPAR agonisti olduğunda? tek başlarına yeterli kan şekeri kontrolü sağlamazlar.
ile kombinasyon halinde üçlü oral tedavide
• Diyet ve egzersiz ile bu ilaçlarla ikili tedavi yeterli glisemik kontrol sağlamadığında bir sülfonilüre ve metformin.
• bir PPAR agonisti mi? ve bir PPAR agonisti kullanımı uygun olduğunda ve diyet ve egzersiz artı bu ilaçlarla ikili tedavi yeterli glisemik kontrol sağlamadığında metformin.
Xelevia, diyet ve egzersizin yanı sıra stabil bir insülin dozu yeterli glisemik kontrol sağlamadığında insüline (metforminli veya metforminsiz) ek tedavi olarak da endikedir.
04.2 Pozoloji ve uygulama yöntemi
Dozaj
Doz günde bir kez 100 mg sitagliptindir. Metformin ve/veya bir PPAR agonisti ile kombinasyon halinde kullanıldığında, metformin ve/veya PPAR agonisti dozu korunmalıdır ve Xelevia eş zamanlı olarak uygulanmalıdır.
Xelevia bir sülfonilüre veya insülin ile kombinasyon halinde kullanıldığında, hipoglisemi riskini azaltmak için daha düşük bir sülfonilüre veya insülin dozu düşünülebilir (bkz. bölüm 4.4).
Bir Xelevia dozu atlanırsa, hasta hatırladığı anda alınmalıdır.
Aynı gün çift doz alınmamalıdır.
Özel popülasyonlar
Böbrek hasarı
Sitagliptin'in başka bir antidiyabetik tıbbi ürünle birlikte kullanımı düşünüldüğünde, böbrek yetmezliği olan hastalarda kullanım şekli kontrol edilmelidir.
Hafif böbrek yetmezliği olan hastalarda (kreatinin klerensi [CrCl] ≥ 50 mL/dak), doz ayarlaması gerekli değildir.
Orta derecede böbrek yetmezliği olan hastalar için (CrCl ≥ 30 ila
Şiddetli böbrek yetmezliği (CrCl hemodiyalizi veya periton diyalizi) olan hastalar için Xelevia dozu günde bir kez 25 mg'dır. Tedavi, diyalizin zamanlamasına bakılmaksızın uygulanabilir.
Böbrek fonksiyonuna dayalı bir doz ayarlaması olduğundan, Xelevia ile tedaviye başlamadan önce ve sonrasında periyodik olarak böbrek fonksiyonunun değerlendirilmesi önerilir.
Karaciğer yetmezliği
Hafif ila orta derecede karaciğer yetmezliği olan hastalarda doz ayarlaması gerekli değildir. Xelevia, şiddetli karaciğer yetmezliği olan hastalarda çalışılmamıştır ve dikkatli olunmalıdır (bkz. bölüm 5.2).
Bununla birlikte, sitagliptin esas olarak böbrek yoluyla elimine edildiğinden, ciddi karaciğer yetmezliğinin sitagliptinin farmakokinetiğini etkilemesi beklenmez.
Yaşlılar
Yaşa göre doz ayarlaması gerekli değildir.
Pediatrik popülasyon
18 yaşından küçük çocuklarda ve adolesanlarda sitagliptinin güvenliliği ve etkililiği. Veri mevcut değildir.
Uygulama yöntemi
Xelevia yemekle birlikte veya yemeksiz alınabilir.
04.3 Kontrendikasyonlar
Etkin maddeye veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık (bkz. bölüm 4.4 ve 4.8).
04.4 Özel uyarılar ve uygun kullanım önlemleri
genellik
Xelevia, tip I diyabetli hastalarda veya diyabetik ketoasidoz tedavisinde kullanılmamalıdır.
akut pankreatit
Dipeptidil peptidaz 4 (DPP-4) inhibitörlerinin kullanımı, akut pankreatit gelişme riski ile ilişkilendirilmiştir. Hastalar, akut pankreatitin karakteristik semptomu hakkında bilgilendirilmelidir: şiddetli, kalıcı karın ağrısı Pankreatitte düzelme gözlenmiştir. sitagliptin tedavisi (destek tedavisi olsun veya olmasın), ancak çok seyrek olarak nekrotizan veya hemorajik pankreatit ve/veya ölüm vakaları bildirilmiştir. Pankreatit şüphesi varsa, Xelevia ve diğer potansiyel olarak şüpheli tıbbi ürünlerle tedavi kesilmelidir; akut pankreatit teşhisi doğrulanırsa, Xelevia tedavisi yeniden başlatılmamalıdır. Pankreatit öyküsü olan hastalarda dikkatli olunmalıdır.
Diğer antihiperglisemik ilaçlarla birlikte kullanıldığında hipoglisemi
Xelevia'nın monoterapi olarak ve hipoglisemiye neden olduğu bilinmeyen tıbbi ürünlerle (örn. metformin ve/veya bir PPAR agonisti?) kombinasyon tedavisinin bir parçası olarak yapılan klinik çalışmalarda, sitagliptin ile bildirilen hipoglisemi insidansı, plasebo alan hastalardaki insidansa benzerdi. Sitagliptin, insülin veya bir sülfonilüre ile kombinasyon halinde kullanıldığında hipoglisemi gözlenmiştir. Bu nedenle, hipoglisemi riskini azaltmak için daha düşük dozda sülfonilüre veya insülin düşünülebilir (bkz. bölüm 4.2).
Böbrek hasarı
Sitagliptin böbrek yoluyla atılır. Normal böbrek fonksiyonu olan hastalardakine benzer plazma sitagliptin konsantrasyonları elde etmek için, orta ve şiddetli böbrek yetmezliği olan hastalarda ve hemodiyaliz veya periton diyalizi gerektiren ESRD hastalarında daha düşük dozlar önerilir (bkz. bölüm 4.2 ve 5.2).
Sitagliptin'in başka bir antidiyabetik tıbbi ürünle birlikte kullanımı düşünüldüğünde, böbrek yetmezliği olan hastalarda kullanım şekli kontrol edilmelidir.
aşırı duyarlılık reaksiyonları
Pazarlama sonrası raporlarda, sitagliptin ile tedavi edilen hastalarda ciddi aşırı duyarlılık reaksiyonları bildirilmiştir. Bu reaksiyonlar anafilaksi, anjiyoödem ve Stevens-Johnson sendromu dahil eksfolyatif cilt bozukluklarını içerir. Bu reaksiyonların başlangıcı, tedavinin başlamasından sonraki ilk 3 ay içinde meydana geldi ve bazı raporlar ilk dozdan sonra meydana geldi.
Aşırı duyarlılık reaksiyonundan şüpheleniliyorsa Xelevia tedavisi kesilmelidir. Olayın diğer olası nedenleri araştırılmalı ve diyabet için alternatif tedavi başlatılmalıdır.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Diğer tıbbi ürünlerin sitagliptin üzerindeki etkileri
Aşağıda açıklanan klinik veriler, eşzamanlı tıbbi ürünlerle klinik olarak anlamlı etkileşim riskinin sınırlı olduğunu göstermektedir.
Eğitim laboratuvar ortamında sitagliptinin sınırlı metabolizmasından sorumlu ana enzimin, CYP2C8'in katkısıyla CYP3A4 olduğunu belirtti. Normal böbrek fonksiyonu olan hastalarda, CYP3A4 dahil olmak üzere metabolizmanın sitagliptin klerensinde sınırlı bir rolü vardır. Şiddetli böbrek yetmezliği veya son dönem böbrek hastalığı (SDBY) bağlamında sitagliptinin eliminasyonunda metabolizma daha önemli bir rol oynayabilir.Bu nedenle güçlü CYP3A4 inhibitörlerinin (örn. ketokonazol, itrakonazol, ritonavir, klaritromisin) değişiklik göstermesi olasıdır. Şiddetli böbrek yetmezliği veya son dönem böbrek yetmezliği olan hastalarda sitagliptinin farmakokinetiği Güçlü CYP3A4 inhibitörlerinin böbrek yetmezliğindeki etkileri bir klinik çalışmada belirlenmemiştir.
Ulaştırma çalışmaları laboratuvar ortamında sitagliptinin p-glikoprotein ve organik anyon taşıyıcı 3 (OAT3) için bir substrat olduğunu gösterdi. OAT3 aracılı sitagliptin taşınması inhibe edildi laboratuvar ortamında Probenesid, klinik olarak anlamlı etkileşimlerin riskinin sınırlı olduğu kabul edilse de. OAT3 inhibitörlerinin eşzamanlı uygulaması değerlendirilmemiştir. canlıda.
metformin: Günde iki kez 50 mg sitagliptin ile 1000 mg çoklu metformin dozlarının birlikte uygulanması, tip 2 diyabetli hastalarda sitagliptinin farmakokinetiğini önemli ölçüde değiştirmedi.
siklosporin: Güçlü bir p-glikoprotein inhibitörü olan siklosporinin sitagliptinin farmakokinetiği üzerindeki etkisini değerlendirmek için bir çalışma yapılmıştır. Sitagliptinin Cmax'ı sırasıyla yaklaşık %29 ve %68 Sitagliptinin farmakokinetiğindeki bu değişiklikler klinik olarak anlamlı kabul edilmemiştir Sitagliptinin renal klerensi önemli ölçüde değişmemiştir Bu nedenle diğer p-glikoprotein inhibitörleri ile ilgili herhangi bir etkileşim beklenmemektedir.
Sitagliptinin diğer tıbbi ürünler üzerindeki etkileri
Digoksin: Sitagliptin, plazma digoksin konsantrasyonları üzerinde sınırlı bir etkiye sahipti. 10 gün boyunca günde 100 mg sitagliptin ile birlikte 0.25 mg digoksin uygulamasını takiben, digoksinin plazma EAA'sı ortalama %11 arttı ve plazma Cmaks'ı ortalama %18 arttı. Digoksin doz ayarlaması önerilmez. Bununla birlikte, sitagliptin ve digoksin birlikte uygulandığında digoksin toksisitesi riski taşıyan hastalarda digoksin toksisitesi izlenmelidir.
Veri laboratuvar ortamında sitagliptinin CYP450 izoenzimlerini inhibe etmediğini veya indüklemediğini öne sürmektedir. Klinik çalışmalarda sitagliptin, metformin, gliburid, simvastatin, rosiglitazon, varfarin veya oral kontraseptiflerin farmakokinetiğini önemli ölçüde değiştirmedi ve kanıt sağladı. canlıda CYP3A4, CYP2C8, CYP2C9 substratları ve organik katyon taşıyıcı (OCT) ile etkileşimlere neden olma eğilimi düşüktür. Sitagliptin, p-glikoproteinin zayıf bir inhibitörü olabilir canlıda.
04.6 Hamilelik ve emzirme
Gebelik
Hamile kadınlarda sitagliptin kullanımına ilişkin yeterli veri yoktur Hayvan çalışmaları yüksek dozlarda üreme toksisitesi göstermiştir (bkz. Bölüm 5.3) İnsanlar için potansiyel risk bilinmemektedir. İnsan verilerinin olmaması nedeniyle, Xelevia hamilelik sırasında kullanılmamalıdır.
Besleme zamanı
Sitagliptinin insan sütüne geçip geçmediği bilinmemektedir. Hayvan çalışmaları sitagliptin'in anne sütüne geçtiğini göstermiştir. Xelevia emzirme döneminde kullanılmamalıdır.
Doğurganlık
Hayvan verileri, sitagliptin tedavisinin erkek ve dişi doğurganlığı üzerinde bir etkisi olduğunu önermemektedir. İnsan verisi eksikliği var.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
Xelevia'nın araç ve makine kullanma yeteneği üzerinde etkisi yoktur veya ihmal edilebilir düzeydedir.
Ancak, araç veya makine kullanırken baş dönmesi ve uyku halinin rapor edildiği akılda tutulmalıdır.
Ek olarak, Xelevia bir sülfonilüre veya insülin ile birlikte kullanıldığında, hastalar hipoglisemi riski konusunda bilgilendirilmelidir.
04.8 İstenmeyen etkiler
Güvenlik profilinin özeti
Pankreatit ve aşırı duyarlılık reaksiyonları dahil ciddi advers reaksiyonlar bildirilmiştir.
Sülfonilüre (%4.7 - 13.8) ve insülin (%9.6) ile ilişkili olarak hipoglisemi bildirilmiştir (bkz. bölüm 4.4).
Advers reaksiyon tablosu
Advers reaksiyonlar aşağıda (Tablo 1) sistem organ sınıfı ve sıklığına göre listelenmiştir. Sıklıklar şu şekilde tanımlanmıştır: çok yaygın (≥ 1/10); yaygın (≥ 1/100,
Tablo 1. Sitagliptin monoterapisinin plasebo kontrollü klinik çalışmalarından ve pazarlama sonrası deneyimden tanımlanan advers reaksiyonların sıklığı
* Pazarlama sonrası gözetimde tanımlanan advers reaksiyonlar.
† Bölüm 4.4'e bakın.
‡ Aşağıya bakınız TECOS Kardiyovasküler Güvenlik Çalışması.
Seçilmiş advers reaksiyonların tanımı
Yukarıda açıklanan ilaca bağlı advers deneyimlere ek olarak, tıbbi ürünle nedensel ilişkiden bağımsız olarak bildirilen ve vakaların en az %5'inde ve en yaygın olarak sitagliptin ile tedavi edilen hastalarda meydana gelen advers deneyimler arasında üst solunum yolu enfeksiyonu ve nazofarenjit yer almaktadır. Sitagliptin ile tedavi edilen hastalarda daha sık meydana gelen (%5 düzeyine ulaşmayan, ancak kontrol grubuna kıyasla sitagliptin ile >%0.5 daha yüksek bir insidansla meydana gelen) tıbbi ürünle nedensel ilişkiden bağımsız olarak bildirilen ek advers deneyimler ) osteoartrit ve ekstremitelerde ağrıyı içeriyordu.
Sitagliptin'in diğer antidiyabetik tıbbi ürünlerle yapılan kombinasyon çalışmalarında, sitagliptin monoterapisi çalışmalarından daha sık olarak bazı advers reaksiyonlar gözlenmiştir. metformin), bulantı ve kusma (metformin ile yaygın), gaz (metformin veya pioglitazon ile yaygın), kabızlık (sülfonilüre ve metformin kombinasyonu ile yaygın), periferik ödem (pioglitazon veya pioglitazon ve metformin kombinasyonu ile yaygın) somnolans ve ishal (metformin ile yaygın olmayan) ve ağız kuruluğu (insülin ile yaygın olmayan (metforminli veya metforminsiz)).
TECOS Kardiyovasküler Güvenlik Çalışması
Sitagliptin ile Kardiyovasküler Sonuçları Değerlendirme Çalışması (TECOS) çalışmasına günde 100 mg (veya başlangıç eGFR ≥30 ve 2 ise günde 50 mg) sitagliptin ile tedavi edilen 7.332 hasta ve niyet popülasyonunda plasebo ile tedavi edilen 7.339 hasta dahil edilmiştir. -davranmak. Her iki tedavi de genellikle HbA1c ve KV risk faktörleri için bölgesel standart değerler elde etmek için kullanılan tedaviye eklendi.Sitagliptin ile tedavi edilen hastalarda ciddi advers olayların genel insidansı, tedavi edilen hastalardakine benzerdi.plasebo ile
Tedavi amaçlı popülasyonda, başlangıçta insülin ve/veya sülfonilüre kullanan hastalarda, şiddetli hipoglisemi insidansı sitagliptin ile tedavi edilen hastalarda %2.7 ve plasebo ile tedavi edilen hastalarda %2.5; insülin kullanmayan hastalarda ve/veya bir bazal sülfonilüre, şiddetli hipoglisemi insidansı sitagliptin ile tedavi edilen hastalarda %1.0 ve plasebo ile tedavi edilen hastalarda %0.7 olmuştur. Doğrulanmış pankreatit olayları tanılarının insidansı, sitagliptin ile tedavi edilen hastalarda %0.3 ve plasebo ile tedavi edilen hastalarda %0.2 idi.
Şüpheli advers reaksiyonların raporlanması
İlacın ruhsatlandırılmasından sonra meydana gelen şüpheli advers reaksiyonların raporlanması, tıbbi ürünün fayda/risk oranının sürekli olarak izlenmesine olanak sağladığı için önemlidir.Sağlık profesyonellerinden, herhangi bir şüpheli advers reaksiyonu İtalyan İlaç Kurumu aracılığıyla bildirmeleri istenir. , web sitesi: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Doz aşımı
Sağlıklı gönüllülerde yapılan kontrollü klinik çalışmalarda, 800 mg'a kadar tek doz sitagliptin uygulandı. Bir çalışmada 800 mg sitagliptin dozunda, klinik olarak anlamlı kabul edilmeyen QTc'de minimal artışlar gözlenmiştir. Klinik çalışmalarda 800 mg'ın üzerindeki dozlarla ilgili deneyim yoktur. 10 güne kadar olan periyotlar için günde 600 mg'a kadar sitagliptin ve 28 güne kadar olan periyotlar için günde 400 mg'a kadar sitagliptin dozları ile yapılan çok dozlu Faz I çalışmalarında doza bağlı advers reaksiyonlar gözlenmemiştir.
Doz aşımı durumunda, yaygın destekleyici önlemlerin kullanılması mantıklıdır, örneğin: emilmeyen materyali gastrointestinal sistemden uzaklaştırın, klinik izleme yapın (elektrokardiyografi dahil) ve gerekirse destekleyici bakım uygulayın.
Sitagliptinin diyaliz edilebilirliği mütevazıdır. Klinik çalışmalarda, 3-4 saatlik bir hemodiyaliz seansında dozun yaklaşık %13,5'i uzaklaştırılmıştır. Klinik olarak uygun görüldüğü takdirde uzun süreli hemodiyaliz düşünülebilir Sitagliptinin periton diyalizi ile diyalize uygunluğu bilinmemektedir.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: diyabette kullanılan ilaçlar, dipeptidil peptidaz 4 (DPP-4) inhibitörleri.
ATC kodu: A10BH01.
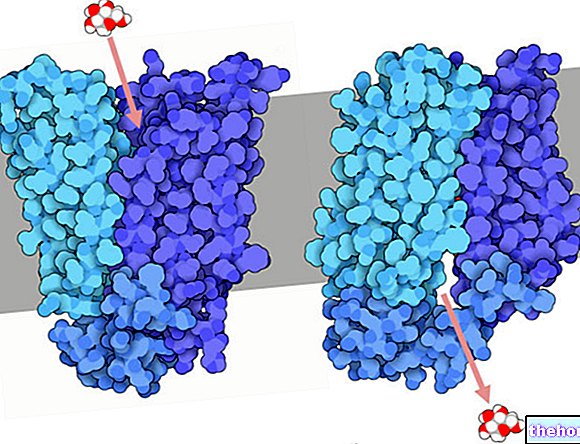
Hareket mekanizması
Xelevia aPPAR?, dipeptidil peptidaz 4 (DPP-4) inhibitörleri olarak adlandırılan bir oral antihiperglisemik ilaç sınıfını içerir. Bu tıbbi ürünle gözlemlenen glisemik kontroldeki iyileşmeye "artmış aktif inkretin seviyeleri" aracılık edebilir. İnkretinler, glukagon benzeri peptit-1 (GLP-1) ve glukoza bağımlı insülinotropik polipeptit (GIP) içeren hormonlar, gün içinde bağırsaktan salınır ve öğünlere tepki olarak seviyeleri yükselir. Incretinler, glikoz homeostazının fizyolojik düzenlenmesinde rol oynayan endojen bir sistemin parçasıdır.Kan glikozu normal veya yükseldiğinde, GLP-1 ve GIP, hücre içi sinyal yolları yoluyla pankreas beta hücreleri tarafından insülin sentezini ve salınımını arttırır.siklik AMP dahil. Tip 2 diyabetli hayvan modellerinde GLP-1 veya DPP-4 inhibitörleri ile tedavinin, glukoza beta hücre tepkisini iyileştirdiği ve insülin biyosentezini ve salınımını uyardığı gösterilmiştir. Daha yüksek insülin seviyeleri ile doku glikoz alımı artar GLP-1 ayrıca pankreas alfa hücreleri tarafından glukagon salgılanmasını azaltır Düşük glukagon konsantrasyonları, daha yüksek insülin seviyeleri ile birlikte hepatik glikoz üretiminin azalmasına neden olur ve bu da kanda bir azalmaya neden olur GLP-1 ve GIP'nin etkileri glikoza bağlıdır, bu nedenle kan şekeri düşük olduğunda, insülin salınımı ve glukagon salgılanmasının baskılanması için herhangi bir uyarı gözlenmez Hem GLP-1 hem de GIP için, glukoz yükseldiğinde insülin salınımının uyarılması artar normal konsantrasyonların üstünde Ayrıca, GLP-1 glukagonun hipoglisemiye normal tepkisini etkilemez. GLP-1 ve GIP'nin aktivitesi, inkretinleri hızla inaktif metabolitlere hidrolize eden DPP-4 enzimi tarafından sınırlandırılır. Sitagliptin, DPP-4 ile inkretinlerin hidrolizini önler, böylece GLP-1 ve GIP'nin aktif formlarının plazma konsantrasyonlarını arttırır.Aktif inkretin seviyelerinin arttırılması sitagliptin insülin salınımını arttırır ve glikoz şeklinde glukagon seviyelerini azaltır.Tip 2 hastalarında Hiperglisemili diyabet, insülin ve glukagon seviyelerindeki bu değişiklikler hemoglobin A1c'nin (HbA1c) azalmasına ve açlık ve kan şekeri konsantrasyonlarının düşmesine neden olur. prandium sonrası. Sitagliptinin glukoza bağımlı mekanizması, glukoz seviyeleri düşük olduğunda bile insülin sekresyonunu artıran ve tip 2 diyabetli hastalarda ve normal kişilerde hipoglisemiye yol açabilen sülfonilürelerin mekanizmasından farklıdır. DPP-4 enzimidir ve terapötik konsantrasyonlarda yakından ilişkili DPP-8 veya DPP-9 enzimlerinin aktivitesini inhibe etmez.
Sağlıklı gönüllülerde yapılan 2 günlük bir çalışmada, tek başına sitagliptin aktif GLP-1 konsantrasyonlarını arttırırken, tek başına metformin aktif ve toplam GLP-1 konsantrasyonlarını benzer şekilde arttırmıştır. Sitagliptin ve metforminin birlikte uygulanması, aktif GLP-1 konsantrasyonları üzerinde ilave bir etkiye sahipti. Sitagliptin, ancak metformin değil, aktif GIP konsantrasyonlarını arttırdı.
Klinik etkinlik ve güvenlik
Genel olarak sitagliptin, monoterapi veya kombinasyon tedavisi olarak verildiğinde glisemik kontrolü iyileştirmiştir (bkz. Tablo 2).
Tek başına sitagliptinin etkililiğini ve güvenliğini değerlendirmek için iki çalışma yapılmıştır. Günde bir kez 100 mg sitagliptin monoterapisi ile tedavi, biri 18 hafta süren ve diğeri olmak üzere iki çalışmada plaseboya kıyasla HbA1c, açlık plazma glukozu (AKG) ve 2 saatlik tokluk glukozunda (2 saatlik PPG) önemli iyileşmeler sağlamıştır. 24 hafta HOMA-a (Homeostasis Model Assessment-?), proinsülin/insülin oranı ve sık örnekleme ile öğün tolerans testine beta hücre yanıtı ölçümleri dahil olmak üzere beta hücre fonksiyonunun vekil belirteçlerinde iyileşme gözlemlendi. sitagliptin ile tedavi edilen hastalarda gözlenen hipoglisemi, plaseboya benzerdi. Plasebo ile tedavi edilen hastalarda görülen hafif bir azalma ile karşılaştırıldığında, iki çalışmada vücut ağırlığı sitagliptin tedavisi ile başlangıca göre artmamıştır.
Günde bir kez 100 mg sitagliptin, biri metformin ile ve diğeri pioglitazon ile kombinasyon halinde olmak üzere, 24 haftalık iki ek sitagliptin çalışmasında plaseboya kıyasla glisemik parametrelerde önemli iyileşmeler sağlamıştır. Vücut ağırlığında başlangıca göre değişiklik, plaseboya kıyasla sitagliptin ile tedavi edilen hastalarda benzerdi.Bu çalışmalarda, sitagliptin veya plasebo ile tedavi edilen hastalarda hipogliseminin "bir" benzer insidansı rapor edilmiştir.
24 haftalık plasebo kontrollü bir çalışma, tek başına glimepirid'e veya metformin ile kombinasyon halinde glimepirid'e eklenen sitagliptinin (günde bir kez 100 mg) etkililiğini ve güvenliğini değerlendirmek için tasarlanmıştır. glisemik parametrelerde iyileştirmeler. Sitagliptin ile tedavi edilen hastalar, plasebo verilenlere kıyasla vücut ağırlığında mütevazı bir artışa sahipti.
Pioglitazon ve metformin kombinasyonuna eklenen sitagliptinin (günde bir kez 100 mg) etkililiğini ve güvenliğini değerlendirmek için 26 haftalık plasebo kontrollü bir çalışma tasarlanmıştır. Sitagliptin'in pioglitazon ve metformine eklenmesi, glisemik parametrelerde önemli iyileşmeler sağladı.Vücut ağırlığındaki başlangıca göre değişiklik, sitagliptin ile tedavi edilen hastalarda ve plasebo ile tedavi edilen hastalarda benzerdi.Plasebo ile tedavi edilen hastalarda hipoglisemi insidansı da benzerdi • sitagliptin veya plasebo ile tedavi edilen hastalar.
İnsüline eklenen sitagliptinin (günde bir kez 100 mg) (en az 10 hafta boyunca stabil bir dozda) metforminle (en az 1.500 mg) etkililiğini ve güvenliğini değerlendirmek için 24 haftalık plasebo kontrollü bir çalışma tasarlanmıştır. Premiks insülin alan hastalarda ortalama günlük doz 70.9 U/gün, premiks olmayan (orta etkili / uzun etkili) insülin alan hastalarda ise ortalama günlük doz 44.3 U/gün idi. İnsüline sitagliptin eklenmesi, glisemik parametrelerde önemli gelişmelere neden oldu. Her iki grupta da vücut ağırlığında başlangıca göre anlamlı bir değişiklik olmadı.
Başlangıç kombinasyon tedavisi faktöriyel çalışmasından 24 haftalık, plasebo kontrollü bir çalışmada, sitagliptin metformin (günde iki kez 500 mg veya 1.000 mg) ile kombinasyon halinde günde iki kez 50 mg, her bir monoterapiye kıyasla glisemik parametrelerde önemli iyileşmeler sağlamıştır. sitagliptin ve metformin kombinasyonu ile tek başına metformin veya plasebo ile gözlemlenene benzerdi; sitagliptin monoterapisi ile tedavi edilen hastalarda başlangıca göre herhangi bir değişiklik gözlenmemiştir. Tedavi grupları arasında hipoglisemi insidansı benzerdi.
Tablo 2: Plasebo Kontrollü Monoterapi ve Kombinasyon Tedavisi Çalışmalarında HbA1c Sonuçları *
* Tedavi edilen tüm hasta popülasyonu (tedavi niyeti analizi).
† En küçük kareler, önceki hipoglisemik tedavi ve başlangıç değeri için ayarlanmış anlamına gelir.
‡ P
§ 18 haftada HbA1c (%). 24 haftada HbA1c (%).
# HbA1c (%) 26 haftada.
¶ En küçük kareler, 1. Ziyarette metformin kullanımı (evet / hayır), 1. Ziyarette [önceden karıştırılmış veya ön karıştırılmamış (orta etkili veya uzun etkili)] insülin kullanımı ve taban çizgisi için ayarlanmış anlamına gelir. metformin ve insülin) anlamlı değildi (p> 0.10).
Diyetle yeterli glisemik kontrolü olmayan hastalarda günde bir kez 100 mg sitagliptinin (N = 528) metforminle (N = 522) etkililiğini ve güvenliğini değerlendirmek için 24 haftalık aktif kontrollü bir çalışma (metformin) tasarlanmıştır. egzersiz yapan ve antihiperglisemik tedavi görmeyen (en az 4 ay tedavi görmemiş) Metforminin ortalama dozu günde yaklaşık 1.900 mg idi. Metformin için -%0.57 (protokol başına analiz) Sitagliptin ile tedavi edilen hastalarda ilaca bağlı olduğu düşünülen gastrointestinal advers reaksiyonların genel insidansı, metformin ile tedavi edilen hastalarda %12.6'ya kıyasla 2. , %7 idi. Hipoglisemi insidansı tedavi grupları arasında önemli ölçüde farklı değildi (sitagliptin, %1.3; metformin, %1.9) Vücut ağırlığı her iki grupta da başlangıca göre azaldı (sitagliptin, -0.6 kg; metformin -1.9 kg).
Metformin monoterapisinde yetersiz glisemik kontrolü olan hastalarda günde bir kez 100 mg sitagliptin veya glipizid (bir sülfonilüre) eklenmesinin etkinlik ve güvenliğini karşılaştıran bir çalışmada sitagliptin, HbA1c'yi azaltmada glipizide benzerdi. Karşılaştırma grubunda kullanılan ortalama glipizid dozu 10 mg/gün olmuştur ve hastaların yaklaşık %40'ı çalışma boyunca ≤ 5 mg/gün glipizid dozuna ihtiyaç duymuştur. Bununla birlikte, sitagliptin grubundaki hastalar, glipizid grubuna göre etkinlik eksikliği nedeniyle daha fazla devamsızlık yaşadı. Sitagliptin ile tedavi edilen hastalarda, glipizid (-1.5 vs +1.1 kg). Bu çalışmada, insülin sentez ve salım etkinliğinin bir belirteci olan proinsülin/insülin oranı sitagliptin ile düzelirken, glipizid tedavisi ile kötüleşirken, hipoglisemi insidansı sitagliptin grubunda (%4.9) glipizid grubuna göre anlamlı derecede düşüktü. (%32.0).
660 hastayı içeren 24 haftalık, plasebo kontrollü bir çalışma, insülin tedavisinin yoğunlaştırılması sırasında metformin ile veya metforminsiz (en az 1.500 mg) insülin glarjinine eklenen sitagliptinin (günde bir kez 100 mg) insülin koruyucu etkililiğini ve güvenliğini değerlendirmek için tasarlanmıştır. Başlangıç HbA1c %8,74 ve başlangıç insülin dozu 37 IU/gün idi. Hastalara parmak ucuyla ölçülen açlık glukoz değerlerine göre insülin glarjin dozunu titre etmeleri talimatı verildi. 24. haftada günlük insülin dozu artışı sitagliptin ile tedavi edilen hastalarda 19 IU/gün ve plasebo ile tedavi edilen hastalarda 24 IU/gün olmuştur Sitagliptin ve insülin (metforminli veya metforminsiz) ile tedavi edilen hastalarda HbA1c'deki azalma - Plasebo ve insülin (metforminli veya metforminsiz) ile tedavi edilen hastalarda %1.31'e karşı -%0.87, fark -%0.45 [%95 GA: -0.60, -0.29] Sitagliptin ile tedavi edilen hastalarda hipoglisemi insidansı %25.2 idi. ve insülin (metforminli veya metforminsiz) ve plasebo ve insülin (metforminli veya metforminsiz) ile tedavi edilen hastalarda %36.8. Fark esas olarak, 3 veya daha fazla hipoglisemi atağı yaşayan plasebo grubundaki hastaların daha yüksek yüzdesinden kaynaklanıyordu (%9.4'e karşı %19.1). Şiddetli hipoglisemi insidansında bir fark yoktu.
Orta ila şiddetli böbrek yetmezliği olan hastalarda günde bir kez 25 veya 50 mg sitagliptin ile günde 2.5 ila 20 mg glipizid'i karşılaştıran bir çalışma yapılmıştır. Bu çalışma, kronik böbrek yetmezliği olan 423 hastayı içeriyordu (tahmini glomerüler filtrasyon hızı
Diyalizde olan 129 SDBY hastasında günde bir kez 25 mg sitagliptin ve günde 2.5 ila 20 mg glipizid'i karşılaştıran başka bir çalışma yapılmıştır. 54 hafta sonra, başlangıca göre HbA1c'deki ortalama azalma sitagliptin ile -%0.72 ve glipizid ile -%0.87 idi. Bu çalışmada, günde bir kez 25 mg sitagliptinin etkililik ve güvenlilik profili, böbrek fonksiyonu normal olan hastalarda yapılan diğer monoterapi çalışmalarında gözlenene genel olarak benzerdi. Tedavi grupları arasında hipoglisemi insidansı önemli ölçüde farklı değildi (sitagliptin, %6.3; glipizid, %10.8).
Tip 2 diyabetli ve kronik böbrek yetmezliği (kreatinin klerensi) olan 91 hastayı içeren başka bir çalışmada
TECOS, HbA1c değerleri ≥6,5 ila %8,0 arasında değişen ve yerleşik KV hastalığı olan ve günde 100 mg sitagliptin (7,332) ile tedavi edilen tedavi amaçlı popülasyondaki 14,671 hastada yapılan randomize bir çalışmadır (veya başlangıçta günde 50 mg). eGFR ≥30 ve 2) veya genellikle HbA1c ve KV risk faktörleri için bölgesel standart değerlere ulaşmak için kullanılan tedaviye plasebo (7.339) eklendi. ≥75 yaş ve böbrek yetmezliği olan 3.324 hasta (eGFR 2).
Çalışma boyunca, sitagliptin ve plasebo grupları arasında HbA1c'deki tahmini genel ortalama (SD) fark %0.29, %95 GA (-0.32, -0.27) idi; P
Birincil kardiyovasküler son nokta, erken başlangıçlı kardiyovasküler ölüm, ölümcül olmayan miyokard enfarktüsü, ölümcül olmayan inme veya stabil olmayan anjina nedeniyle hastaneye yatışın bir bileşimiydi.İkincil kardiyovasküler son noktalar arasında erken başlangıçlı kardiyovasküler ölüm, ölümcül olmayan miyokard enfarktüsü veya ölümcül inme, birleşik birincil son noktanın bireysel bileşenlerinin başlangıcı; herhangi bir nedenle ölüm; ve konjestif kalp yetmezliği nedeniyle hastaneye yatışlar.
Ortalama üç yıllık bir takipten sonra, sitagliptin, genellikle kullanılan tedaviye eklendiğinde, tip diyabetli hastalarda genellikle sitagliptin olmadan kullanılan tedaviye kıyasla majör advers kardiyovasküler olay riskini veya kalp yetmezliği nedeniyle hastaneye yatış riskini artırmadı. 2 (Tablo 3).
Tablo 3. Kompozit kardiyovasküler sonuçların oranları ve ana ikincil sonuçların oranları
* 100 hasta-yılı başına insidans oranı 100 x (toplam hasta-yıl takip için uygun maruziyet süresi boyunca ≥1 olaya sahip toplam hasta sayısı) olarak hesaplanmıştır.
† Bölgesel olarak katmanlara ayrılmış bir Cox modeline dayalıdır. Bileşik uç noktalar için, p-değeri, tehlike oranının 1,3'ten az olduğunu göstermek için bir aşağı olmama testine karşılık gelir. Diğer tüm son noktalar için p değeri, risk oranlarındaki farklılıklar için bir teste karşılık gelir.
‡ Kalp yetmezliği nedeniyle hastaneye yatış analizi, başlangıçta kalp yetmezliğinin anamnestik öyküsüne göre ayarlandı.
Pediatrik popülasyon
Avrupa İlaç Ajansı, tip 2 diyabetli pediyatrik popülasyonun bir veya daha fazla alt grubunda Xelevia ile yapılan çalışmaların sonuçlarını sunma yükümlülüğünü ertelemiştir (pediatrik kullanım hakkında bilgi için bkz. bölüm 4.2).
05.2 Farmakokinetik özellikler
absorpsiyon
Sağlıklı gönüllülere 100 mg'lık bir dozun oral yoldan uygulanmasından sonra, sitagliptin hızla emildi ve doruk plazma konsantrasyonları (medyan Tmaks) dozdan 1 ila 4 saat sonra, sitagliptinin ortalama plazma AUC'si 8, 52 M • saat, Cmaks 950 nM idi. Sitagliptinin mutlak biyoyararlanımı yaklaşık %87'dir.Yüksek yağlı bir öğünün sitagliptin ile birlikte uygulanmasının farmakokinetik üzerinde hiçbir etkisi olmadığından, Xelevia yemeklerden bağımsız olarak uygulanabilir.
Sitagliptinin plazma AUC'si dozla orantılı bir şekilde arttı Cmax ve C24h için doz orantılılığı belirlenmedi (Cmax doz orantılılığından daha fazla arttı ve C24h doz orantılılığına göre daha az arttı).
Dağıtım
Sağlıklı gönüllülere tek bir 100 mg intravenöz sitagliptin dozunu takiben ortalama kararlı durum dağılım hacmi yaklaşık 198 litredir. Plazma proteinlerine geri dönüşümlü bir şekilde bağlanan sitagliptin fraksiyonu düşüktür (%38).
biyotransformasyon
Sitagliptin esas olarak idrar yoluyla değişmeden elimine edilir ve metabolizma minör bir metabolik yoldur. Sitagliptinin yaklaşık %79'u idrarla değişmeden atılır.
Oral [14C] sitagliptin dozunu takiben, radyoaktivitenin yaklaşık %16'sı sitagliptin metabolitleri olarak atıldı. Sitagliptinin altı metabolitinin izleri bulunmuştur ve sitagliptinin plazma DPP-4 inhibitör aktivitesine katkıda bulunması beklenmemektedir. laboratuvar ortamında sitagliptinin sınırlı metabolizmasından birincil olarak sorumlu olan enzimin, CYP2C8'in katkısıyla CYP3A4 olduğunu belirtti.
Veri laboratuvar ortamında sitagliptinin CYP3A4, 2C8, 2C9, 2D6, 1A2, 2C19 veya 2B6 CYP izozimlerinin bir inhibitörü olmadığını ve CYP3A4 ve CYP1A2'nin bir indükleyicisi olmadığını göstermiştir.
Eliminasyon
[14C] sitagliptin'in sağlıklı gönüllülere oral yoldan verilmesini takiben, tatbik edilen radyoaktivitenin yaklaşık %100'ü, uygulamadan sonraki bir hafta içinde dışkıda (%13) veya idrarda (%87) elimine edilmiştir. 100 mg oral sitagliptin dozundan sonra terminal aPPAR t1 / 2 yaklaşık 12.4 saat olmuştur. Sitagliptin, çoklu dozlarda yalnızca minimal düzeyde birikir. Renal klirens yaklaşık 350 mL/dk idi.
Sitagliptin eliminasyonu esas olarak renal atılım yoluyla gerçekleşir ve aktif tübüler sekresyon içerir. Sitagliptin, sitagliptinin renal eliminasyonunda rol oynayabilen insan organik anyon taşıyıcısı 3 (hOAT-3) için bir substrattır.Sitagliptinin taşınmasında hOAT-3'ün klinik önemi belirlenmemiştir. sitagliptinin renal eliminasyonuna aracılık etmede de rol oynayabilen p-glikoprotein. Bununla birlikte, bir p-glikoprotein inhibitörü olan siklosporin, sitagliptinin renal klerensini azaltmamıştır. Sitagliptin, OCT2 veya OAT1 veya PEPT1 / 2 taşıyıcıları için bir substrat değildir. Laboratuvar ortamında, sitagliptin, terapötik olarak ilgili plazma konsantrasyonlarında OAT3 (IC50 = 160 μM) veya p-glikoprotein (250 μM'ye kadar) aracılı taşımayı inhibe etmedi. Klinik bir çalışmada sitagliptin, plazma digoksin konsantrasyonları üzerinde sınırlı bir etkiye sahipti ve sitagliptinin zayıf bir p-glikoprotein inhibitörü olabileceğini gösterdi.
Hastaların özellikleri
Sitagliptinin farmakokinetiği, sağlıklı gönüllülerde ve tip 2 diyabetli hastalarda genel olarak benzerdi.
Böbrek hasarı
Normal sağlıklı kontrol gönüllülerine kıyasla değişen derecelerde kronik böbrek yetmezliği olan hastalarda azaltılmış sitagliptin dozunun (50 mg) farmakokinetiğini değerlendirmek için açık etiketli tek dozlu bir çalışma yürütülmüştür. Çalışma, kreatinin klerensine göre hafif olarak sınıflandırılan böbrek yetmezliği olan hastaları içermiştir (50 ila
Hafif böbrek yetmezliği olan hastalarda, normal sağlıklı kontrol deneklerine kıyasla sitagliptin plazma konsantrasyonlarında klinik olarak anlamlı artışlar olmamıştır. Orta derecede böbrek yetmezliği olan hastalarda sitagliptin plazma EAA'sında yaklaşık 2 kat artış gözlendi ve hemodiyalizde şiddetli böbrek yetmezliği ve ESDR'si olan hastalarda sağlıklı kontrol deneklerine kıyasla plazma EAA'sında yaklaşık 4 kat artış gözlendi. Sitagliptin hemodiyaliz yoluyla sınırlı bir ölçüde uzaklaştırılmıştır (dozdan 4 saat sonra başlayan 3 ila 4 saatlik bir hemodiyaliz seansında %13.5) Sitagliptin plazma konsantrasyonlarını normal böbrek fonksiyonu olan hastalarda bulunanlara benzer şekilde elde etmek için, aşağıdaki dozlarda daha düşük dozlar önerilir: orta ve şiddetli böbrek yetmezliği olan hastaların yanı sıra diyaliz gerektiren SDBY olan hastalarda (bkz. bölüm 4.2).
Karaciğer yetmezliği
Hafif veya orta derecede karaciğer yetmezliği olan hastalarda (Child-Pugh skoru ≤ 9) Xelevia için doz ayarlaması gerekli değildir. Şiddetli karaciğer yetmezliği olan hastalarda klinik deneyim yoktur (Child-Pugh skoru > 9) Bununla birlikte, sitagliptin esas olarak böbrekler yoluyla elimine edildiğinden, ciddi karaciğer yetmezliğinin sitagliptin farmakokinetiğini etkilemesi beklenmemektedir.
Yaşlılar
Yaşa bağlı olarak doz ayarlaması gerekli değildir. 80 yılda bir Faz I ve Faz II popülasyon farmakokinetik analizinden elde edilen verilere göre yaşın sitagliptinin farmakokinetiği üzerinde klinik olarak anlamlı bir etkisi yoktur. gençlerde.
Pediatrik popülasyon
Pediyatrik hastalarda Xelevia ile herhangi bir çalışma yapılmamıştır.
Hastaların diğer özellikleri
Cinsiyet, ırk veya vücut kitle indeksine (BMI) göre doz ayarlaması gerekli değildir. Bu özelliklerin, bir Faz I bileşik farmakokinetik analizinden elde edilen verilere ve bir Faz I ve Faz II popülasyon farmakokinetik analizinden elde edilen verilere dayalı olarak sitagliptin farmakokinetiği üzerinde klinik olarak anlamlı bir etkisi olmamıştır.
05.3 Klinik öncesi güvenlik verileri
Kemirgenlerde, insan maruziyetinin 58 katına eşit sistemik maruziyet değerlerinde böbrek ve karaciğer toksisitesi gözlenirken, insan maruziyetinin 19 katında hiçbir etki düzeyi bulunmadı. Sıçanlarda, insan klinik maruziyetinin 67 katına eşit maruziyet seviyelerinde kesici diş anormallikleri gözlemlendi; 14 haftalık bir sıçan çalışmasına dayalı olarak bu olay için etkisiz seviye 58 kat olmuştur. Bu verilerin insanlarla ilgisi bilinmemektedir.Köpeklerde, klinik maruziyet seviyesinin yaklaşık 23 katı maruziyet seviyelerinde, bazıları ağızdan nefes alma, tükürük salgısı, beyaz köpük gibi nöral toksisiteyi düşündüren tedavi ile ilgili geçici fiziksel belirtiler gözlemlenmiştir. kusma, ataksi, titreme, aktivite azalması ve/veya eğik duruş. İnsanlardaki sistemik maruziyet düzeyinin yaklaşık 23 katına eşdeğer dozlarda, histolojik olarak çok hafif ila hafif iskelet kası dejenerasyonu da gözlenmiştir.Klinik maruziyet düzeyinin 6 katına eşit bir maruziyette bu olaylar için hiçbir etki düzeyi bulunmamıştır.
Sitagliptin preklinik çalışmalarda genotoksisite göstermedi. Sitagliptin farelerde kanserojen değildi. Sıçanlarda, insan maruziyetinin 58 katına eşit sistemik maruziyet seviyelerinde hepatik adenom ve karsinom insidansında bir artış olmuştur.
Geniş güvenlik marjı nedeniyle (bu seviyede etkisi olmayan 19 kat), bu neoplastik lezyonlar, insanlarda maruz kalma koşullarıyla ilgili olarak kabul edilmez.
Çiftleşme öncesinde ve sırasında sitagliptin ile tedavi edilen erkek ve dişi sıçanlarda doğurganlık üzerinde herhangi bir olumsuz etki gözlenmemiştir.
Sıçanlarda yapılan doğum öncesi/sonrası gelişim çalışmalarında sitagliptin herhangi bir yan etki göstermedi.
Üreme toksisitesi çalışmaları, insan maruziyet düzeylerinden 29 kat daha yüksek sistemik maruziyet düzeylerinde sıçanların yavrularında fetal kaburga malformasyonları (yok, hipoplastik ve dalgalı kaburgalar) insidansında tedaviye bağlı hafif bir artış göstermiştir. Tavşanlarda, insan maruziyet düzeylerinin 29 katından daha fazla maruziyet düzeylerinde anne toksisitesi gözlenmiştir.Geniş güvenlik sınırları nedeniyle, bu bulgular insanlarda ilgili üreme risklerinin varlığına işaret etmemektedir. Sitagliptin, emziren sıçanların sütünde kayda değer miktarlarda salgılanır (süt / plazma oranı: 4: 1).
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
Tablet çekirdeği:
mikrokristalin selüloz (E460),
kalsiyum hidrojen fosfat susuz (E341),
kroskarmeloz sodyum (E468),
magnezyum stearat (E470b),
sodyum stearil fumarat
Tablet kaplama:
polivinil alkol),
makrogol 3350,
talk (E553b),
titanyum dioksit (E171),
kırmızı demir oksit (E172),
sarı demir oksit (E172)
06.2 Uyumsuzluk
İlgili değil.
06.3 Geçerlilik süresi
3 yıl
06.4 Depolama için özel önlemler
Bu ilaç herhangi bir özel saklama koşulu gerektirmez.
06.5 İç ambalajın yapısı ve paketin içeriği
Opak kabarcıklar (PVC / PE / PVDC ve alüminyum). Delikli birim doz blisterlerde 14, 28, 30, 56, 84, 90 veya 98 film kaplı tablet ve 50 x 1 film kaplı tabletten oluşan paketler.
Tüm paket boyutları pazarlanmayabilir.
06.6 Kullanım ve kullanım talimatları
Kullanılmayan ilaçlar ve bu ilaçtan elde edilen atıklar yerel yönetmeliklere uygun olarak atılmalıdır.
07.0 PAZARLAMA YETKİ SAHİBİ
Merck Sharp & Dohme Ltd.
Hertford Yolu, Hoddesdon
Hertfordshire EN11 9BU
Birleşik Krallık
08.0 PAZARLAMA YETKİ NUMARASI
AB / 1/07/382/001
037794017
AB / 1/07/382/002
037794029
AB / 1/07/382/003
037794031
AB / 1/07/382/004
037794043
AB / 1/07/382/005
037794056
AB / 1/07/382/006
037794068
AB / 1/07/382/019
037794195
AB / 1/07/382/020
037794207
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
İlk izin tarihi: 21 Mart 2007
En son yenileme tarihi: 20 Ocak 2012
10.0 METİN REVİZYON TARİHİ
28 Ocak 2016