Aktif maddeler: Octreotid
Sandostatin 0.05 mg / ml enjeksiyonluk çözelti veya infüzyonluk çözelti için konsantre
Sandostatin 0.1 mg / ml enjeksiyonluk çözelti veya infüzyonluk çözelti için konsantre
Sandostatin 0,5 mg / ml enjeksiyonluk çözelti veya infüzyonluk çözelti için konsantre
Sandostatin 1 mg / 5 ml enjeksiyonluk çözelti veya infüzyonluk çözelti için konsantre
Sandostatin paket ekleri, paket boyutları için mevcuttur: - Sandostatin LAR 10 mg / 2.5 ml enjeksiyonluk süspansiyon için toz ve solvent, Sandostatin LAR 20 mg / 2.5 ml enjeksiyonluk süspansiyon için toz ve solvent, Sandostatin LAR 30 mg / 2.5 ml enjeksiyonluk süspansiyon için toz ve solvent
- Sandostatin 0,05 mg/ml enjeksiyonluk çözelti veya infüzyonluk konsantre, Sandostatin 0,1 mg/ml enjeksiyonluk çözelti veya infüzyonluk konsantre, Sandostatin 0,5 mg/ml enjeksiyonluk çözelti veya infüzyonluk konsantre, Sandostatin 1 mg / 5 ml enjeksiyonluk çözelti veya infüzyonluk çözelti konsantresi
Sandostatin neden kullanılır? Bu ne için?
Sandostatin, sentetik bir somatostatin analog bileşiğidir. Somatostatin normalde insan vücudunda bulunur ve büyüme hormonu gibi belirli hormonların salınımını engeller.Sandostatinin somatostatine göre avantajları, daha güçlü olması ve etkisinin daha uzun sürmesidir.
Sandostatin kullanılır
- akromegali, vücudun çok fazla büyüme hormonu ürettiği bir durum.Normalde, büyüme hormonu dokuların, organların ve kemiklerin büyümesini kontrol eder. Aşırı miktarda bulunduğunda özellikle el ve ayaklarda kemik ve doku boyutlarında artışa neden olur. Sandostatin, baş ağrısı, aşırı terleme, el ve ayaklarda uyuşma, yorgunluk ve eklem ağrısı gibi akromegali semptomlarını büyük ölçüde azaltır.
- Gastrointestinal sistemin belirli tümörleri ile ilişkili semptomları hafifletmek için (örn. karsinoid tümörler, VIPomalar, glukagonomalar, gastrinomlar, insülinomalar). Bu koşullarda mide, bağırsaklar veya pankreasta bazı spesifik hormonların ve diğer ilgili maddelerin aşırı üretimi vardır.
Bu aşırı üretim vücudun doğal hormonal dengesini değiştirir ve sıcak basması, ishal, hipotansiyon, deri döküntüleri ve kilo kaybı gibi çeşitli semptomlara neden olur. Sandostatin tedavisi bu semptomların kontrol altına alınmasına yardımcı olur.
- Pankreas cerrahisinden kaynaklanan komplikasyonları önlemek için. Sandostatin ile tedavi, ameliyattan sonra komplikasyon (örn. karın apsesi, pankreas iltihabı) olasılığını azaltmaya yardımcı olur.
- sirozlu (kronik karaciğer hastalığı) hastalarda kanamayı durdurmak ve rüptüre gastroözofageal varislerden tekrar kanamaya karşı korunmak için. Sandostatin tedavisi kanamayı kontrol etmeye ve kan nakli ihtiyacını azaltmaya yardımcı olur.
- Aşırı miktarda tiroid uyarıcı hormon (TSH) üreten hipofiz adenomlarını tedavi etmek için.
- diğer tedaviler (ameliyat veya radyoterapi) endike olmadığında veya etkili olmadığında;
- radyoterapi sonrası, radyoterapinin maksimum etkinliğe ulaşması için gerekli olan süreyi kapsayacak şekilde
Kontrendikasyonlar Sandostatin ne zaman kullanılmamalıdır?
SANDOSTATİN'i aşağıdaki durumlarda KULLANMAYINIZ
- Oktreotide veya bu ilacın içerdiği diğer maddelerden herhangi birine karşı alerjiniz varsa
Kullanım Önlemleri Sandostatin almadan önce bilmeniz gerekenler
SANDOSTATİN'i almadan önce doktorunuzla konuşun:
- Safra taşınız olduğunu biliyorsanız veya geçmişte olduysa; SANDOSTATİN'in uzun süreli kullanımı taş oluşumuna neden olabileceğinden doktorunuza söyleyiniz. Doktorunuz sizden safra kesesinin periyodik kontrollerini yaptırmanızı isteyebilir.
- Kan şekeri seviyenizle ilgili çok yüksek (diyabet) veya çok düşük (hipoglisemi) sorunlarınız olduğunu biliyorsanız. SANDOSTATİN gastroözofageal varis kanamasını tedavi etmek için kullanıldığında, kan şekeri seviyeleri izlenmelidir.
- Daha önce B12 vitamini eksikliği atakları geçirdiyseniz, doktorunuz sizden periyodik olarak B12 vitamini seviyenizi kontrol etmenizi isteyebilir.
Testler ve kontroller
SANDOSTATİN tedavisini uzun süre alıyorsanız, doktorunuz sizden tiroid fonksiyonunuzu periyodik olarak kontrol etmenizi isteyebilir.
Doktorunuz karaciğer fonksiyonunuzu kontrol edecektir.
Çocuklar
Çocuklarda Sandostatin kullanımı ile ilgili deneyimler sınırlıdır.
Etkileşimler Hangi ilaçlar veya yiyecekler Sandostatin'in etkisini değiştirebilir?
Başka ilaçlar alıyorsanız, yakın zamanda aldıysanız veya alma ihtimaliniz varsa doktorunuza veya eczacınıza söyleyiniz. NS
Sandostatin tedavisi sırasında genellikle diğer ilaçları almaya devam edebilirsiniz. Bununla birlikte, Sandostatin'in simetidin, siklosporin, bromokriptin, kinidin ve terfenadin gibi bazı ilaçlarla etkileşime girdiği bildirilmiştir.
Kan basıncını kontrol etmek için ilaçlar (beta blokerler veya kalsiyum kanal blokerleri gibi) veya su ve elektrolit dengesini kontrol etmek için ilaçlar alıyorsanız, doktorunuz dozunuzu ayarlamaya karar verebilir.
Şeker hastasıysanız, doktorunuz insülin dozunuzu ayarlamaya karar verebilir.Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme
Hamileyseniz veya emziriyorsanız, hamile olabileceğinizi düşünüyorsanız veya bebek sahibi olmayı planlıyorsanız, bu ilacı almadan önce doktorunuza danışınız.
Sandostatin sadece hamilelik sırasında açıkça gerekliyse kullanılabilir.
Çocuk doğurma potansiyeli olan hastalar tedavi sırasında yeterli kontrasepsiyon kullanmalıdır.
SANDOSTATİN tedavisi sırasında hastalar emzirmemelidir. Sandostatin'in insan sütüne geçip geçmediği bilinmemektedir.
Araç ve makine kullanma
SANDOSTATİN'in araç veya makine kullanma yeteneği üzerinde etkisi yoktur veya ihmal edilebilir düzeydedir. Bununla birlikte, SANDOSTATİN ile tedavi sırasında, güvenli bir şekilde araç ve makine kullanma yeteneğini azaltabilecek baş ağrısı ve yorgunluk gibi bazı yan etkiler ortaya çıkabilir.
Doz, Uygulama Yöntemi ve Zamanı Sandostatin nasıl kullanılır: Pozoloji
Bu ilacı her zaman tam olarak doktorunuzun veya eczacınızın size söylediği şekilde alınız. emin değilseniz, doktorunuza veya eczacınıza danışınız. Tedavi edilen duruma bağlı olarak SANDOSTATİN şu şekilde uygulanabilir:
- deri altı enjeksiyon (deri altına) veya
- intravenöz infüzyon (damar içine).
Sirozlu (kronik karaciğer hastalığı) bir hastaysanız, doktorunuzun idame dozunuzu ayarlaması gerekebilir. Doktorunuz veya hemşireniz Sandostatin'in deri altına nasıl enjekte edileceğini size açıklayacaktır ancak damar içine infüzyon her zaman bir sağlık uzmanı tarafından yapılmalıdır.
- Derialtı enjeksyonu
Deri altı enjeksiyon için en uygun yerler kollar, uyluklar ve karındır.
Belirli bir bölgeyi tahriş etmemek için her deri altı enjeksiyon için yeni bir yer seçin. Enjeksiyona kendi başlarına devam edecek hastalar, doktorlarından veya hemşirelerinden kesin talimatlar almalıdır.
İlacı buzdolabında saklayacaksanız, kullanmadan önce oda sıcaklığına getirmeniz tavsiye edilir. Bu, enjeksiyon bölgesi ağrısı riskini azaltır. Elde tutularak oda sıcaklığına getirilebilir ancak ısıtılması gerekmez.
Deri altındaki enjeksiyon bölgesinde çok az insan ağrı hisseder.Bu ağrı genellikle sadece kısa bir süre sürer.Bu oluşursa, enjeksiyon bölgesine birkaç saniye sonra hafifçe masaj yaparak rahatlayabilir.
Sandostatin flakonunu kullanmadan önce partikül veya renk varyasyonlarını kontrol edin. Olağandışı bir şey fark ederseniz kullanmayın.
Kontaminasyonu önlemek için çok dozlu flakonların tıpası 10 defadan fazla delinmemelidir.
Doz aşımı Çok fazla SANDOSTATİN aldıysanız ne yapmalısınız?
Kullanmanız gerekenden daha fazla Sandostatin kullandıysanız
Sandostatin doz aşımından sonra yaşamı tehdit eden herhangi bir reaksiyon bildirilmemiştir.
Doz aşımı belirtileri şunlardır: düzensiz kalp atışı, düşük tansiyon, kalp durması, beyne giden oksijenin azalması, üst midede şiddetli ağrı, sarı cilt ve gözler, mide bulantısı, iştahsızlık, ishal, halsizlik, yorgunluk, enerji eksikliği, kilo kaybı, şişkinlik, halsizlik ve kanda yüksek düzeyde laktik asit.
Doz aşımı belirtileriniz olduğunu düşünüyorsanız hemen doktorunuza söyleyiniz.
SANDOSTATİN'i kullanmayı unutursanız
Hatırlar hatırlamaz bir doz alın ve ardından tedaviye her zamanki gibi devam edin. Bir dozun atlanmasının belirli bir sonucu olmayacaktır, ancak normale dönene kadar semptomların geçici olarak geri dönmesine neden olabilir.
Unutulan bir dozu telafi etmek için çift doz Sandostatin enjekte etmeyin.
SANDOSTATİN'i kullanmayı bırakırsanız
SANDOSTATİN tedavisi kesilirse semptomlar tekrarlayabilir. Bu nedenle, doktorunuz söylemedikçe SANDOSTATİN almayı bırakmayınız.
Bu ilacın kullanımıyla ilgili başka sorularınız varsa, doktorunuza, eczacınıza veya hemşirenize sorunuz.
Yan Etkiler Sandostatin'in yan etkileri nelerdir?
Tüm ilaçlar gibi, bu ilaç da yan etkilere neden olabilir, ancak bu yan etkiler herkeste görülmez.
Bazı yan etkiler ciddi olabilir. Aşağıdakilerden herhangi biri meydana gelirse derhal doktorunuza söyleyiniz:
Çok yaygın (10 kullanıcıdan 1'inden fazlasını etkileyebilir):
- Ani sırt ağrısına neden olabilen safra taşları.
- Yüksek kan şekeri seviyeleri.
Yaygın (10 kullanıcıdan 1'ini etkileyebilir):
- Tiroid bezinin aktivitesinde azalma (hipotiroidizm), kalp hızında, iştahta veya kiloda değişiklikler, yorgunluk, üşüme veya boynun önünde şişlik hissi.
- Tiroid fonksiyon testlerinde değişiklikler.
- Safra kesesi iltihabı (kolesistit); Semptomlar, sağ üst karında ağrı, ateş, mide bulantısı, ciltte ve gözlerde sararma (sarılık) içerebilir.
- Düşük kan şekeri.
- Bozulmuş glikoz toleransı.
- Yavaş kalp atışı.
Yaygın olmayan (100 kullanıcıdan 1'ini etkileyebilir):
- Susuzluk, düşük idrar çıkışı, koyu renkli idrar, kırmızı ve kuru cilt.
- Hızlı nabız.
Diğer ciddi yan etkiler
- Deri döküntüsü dahil aşırı duyarlılık (alerji) reaksiyonları.
- Nefes almada güçlük veya baş dönmesine neden olan bir tür alerjik reaksiyon (anafilaksi).
- Pankreas iltihabı (pankreatit) semptomları arasında üst karın bölgesinde ani ağrı, bulantı, kusma, ishal sayılabilir.
- Karaciğer iltihabı (hepatit); Semptomlar ciltte ve gözlerde sararma (sarılık), bulantı, kusma, iştahsızlık, genel olarak iyi hissetmeme, kaşıntı, açık renkli idrar içerebilir.
- Düzensiz kalp atışı.
Yukarıda açıklanan yan etkilerden herhangi birini fark ederseniz derhal doktorunuza söyleyiniz.
Diğer yan etkiler:
Aşağıda listelenen yan etkilerden herhangi birini fark ederseniz doktorunuza, eczacınıza veya hemşirenize söyleyiniz.Bunlar genellikle hafif şiddettedir ve tedaviye devam edildiğinde kaybolma eğilimindedir.
Çok yaygın (10 kullanıcıdan 1'inden fazlasını etkileyebilir):
- İshal.
- Karın ağrısı.
- Mide bulantısı.
- Kabızlık.
- Şişkinlik.
- Baş ağrısı.
- Enjeksiyon bölgesinde lokal ağrı.
Yaygın (10 kullanıcıdan 1'ini etkileyebilir):
- Yemekten sonra mide rahatsızlığı (dispepsi).
- öğürdü.
- Mide dolgunluğu hissi.
- Yağlı dışkı.
- Yumuşak tabureler.
- açıklığa kavuşturdum.
- Baş dönmesi
- İştah kaybı.
- Karaciğer fonksiyon testlerinde değişiklik.
- Saç kaybı
- Nefes darlığı.
- zayıflık.
Bu yan etkilerden herhangi biri meydana gelirse, lütfen doktorunuza, hemşirenize veya eczacınıza söyleyiniz.
Deri altındaki enjeksiyon bölgesinde çok az insan ağrı hisseder.Bu ağrı genellikle sadece kısa bir süre sürer.Bu meydana gelirse, enjeksiyon bölgesine birkaç saniye hafifçe masaj yaparak rahatlayabilir.
SANDOSTATİN'i subkutan enjeksiyonla alıyorsanız, gastrointestinal yan etki riskini azaltmaya yardımcı olabileceğinden öğünlere yakın enjeksiyonlardan kaçının.Bu nedenle öğün aralarında veya yatmadan önce enjekte edilmesi önerilir.
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuzla, eczacınızla veya hemşirenizle konuşun.Bu broşürde listelenmeyen olası yan etkiler de buna dahildir.Yan etkileri doğrudan ulusal raporlama sistemi aracılığıyla da bildirebilirsiniz. .agenziaitalianadelfarmaco.gov.it / it / sorumluluk sahibi
Yan etkileri bildirerek, bu ilacın güvenliği hakkında daha fazla bilgi sağlamaya yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
Uzun süreli saklama için hem ampuller hem de şişeler 2° ile 8°C arasında bir sıcaklıkta tutulmalıdır. Işıktan korumak için orijinal ambalajında saklayınız.
0,05 - 0,1 - 0,5 mg / ml enjeksiyonluk çözelti veya infüzyonluk çözelti için konsantre:
Günlük kullanım sırasında <30°C sıcaklıkta 2 hafta süreyle saklayınız.
1 mg / 5 ml enjeksiyonluk çözelti veya infüzyonluk çözelti konsantresi:
Günlük kullanım sırasında <25 °C sıcaklıkta 2 hafta süreyle saklayınız.
Şişe: dondurmayın. Bu ilacı "EXP" sonrasında paketin üzerinde belirtilen son kullanma tarihinden sonra kullanmayınız. Son kullanma tarihi, o ayın son gününü ifade eder.
Herhangi bir ilacı atık su veya evsel atık yoluyla atmayın.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorun.Bu, çevrenin korunmasına yardımcı olacaktır.
Sandostatin ne içerir?
Sandostatin 0,05 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon):
Aktif bileşen 0.05 mg oktreotiddir.
Diğer bileşenler şunlardır: laktik asit, mannitol, sodyum bikarbonat, enjeksiyonluk su.
Sandostatin 0.1 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon):
Aktif bileşen 0.1 mg oktreotiddir.
Diğer bileşenler şunlardır: laktik asit, mannitol, sodyum bikarbonat, enjeksiyonluk su.
Sandostatin 0,5 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon):
Aktif bileşen 0,5 mg oktreotiddir.
Diğer bileşenler şunlardır: laktik asit, mannitol, sodyum bikarbonat, enjeksiyonluk su.
Sandostatin 1 mg / 5 ml (0,2 mg/ml) çok dozlu flakonlar, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon):
Aktif bileşen oktreotid 1 mg'dır.
Diğer bileşenler şunlardır: laktik asit, fenol, manitol, sodyum bikarbonat, enjeksiyonluk su.
Sandostatin'in neye benzediğinin ve paketin içeriğinin açıklaması
Sandostatin 0.05 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): 5 ampul 1 ml
Sandostatin 0.1 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): 5 ampul 1 ml
Sandostatin 0,5 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): 3 ampul 1 ml
Sandostatin multidoz flakonları 1 mg / 5 ml (0,2 mg/ml), enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon): 1 şişe 5 ml
Çözüm: çözelti berrak ve renksizdir
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
ŞİŞE SANDOSTATİN, ENJEKSİYON ÇÖZELTİ (DERİN KULLANIM) VEYA İNFÜZYON ÇÖZELTİ İÇİN KONSANTRE (İNTRAVENÖZ İNFÜZYON)
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Sandostatin 0.05 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon)
Bir şişe şunları içerir:
Aktif madde: 0.05 mg oktreotid.
Sandostatin 0.1 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon)
Bir şişe şunları içerir:
Aktif madde: 0.1 mg oktreotid.
Sandostatin 0.5mg / 1ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon)
Aktif madde: 0,5 mg oktreotid.
Sandostatin 1 mg / 5 ml (0,2 mg/ml) çok dozlu flakonlar, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon)
Bir şişe şunları içerir:
Aktif madde: oktreotid 1 mg.
Bu tıbbi ürün doz başına 1 mmol'den (23 mg) daha az sodyum içerir, yani esasında "sodyum içermez".
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakın.
03.0 FARMASÖTİK FORM
Enjeksiyonluk çözelti veya infüzyonluk çözelti konsantresi
Çözelti berrak ve renksizdir.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Cerrahi tedavi veya radyoterapi ile yeterince kontrol edilemeyen akromegali hastalarında büyüme hormonu (GH) ve IGF-1'in plazma seviyelerinin semptomatik kontrolü ve azaltılması.Sandostatin ayrıca ameliyatın kontrendike olduğu veya başka bir şekilde kabul edilmeyen veya radyoterapi için bekleyen akromegali hastalarda endikedir. maksimum etkinliğe ulaşmak için.
Karsinoid sendrom özelliklerine sahip karsinoid tümörler gibi fonksiyonel gastro-entero-pankreatik (GEP) endokrin tümörlerle ilişkili semptomların tedavisi (bkz. bölüm 5.1).
Sandostatin bir antikanser tedavisi değildir ve bu hastalarda tedavi edici değildir.
Pankreas cerrahisinden kaynaklanan komplikasyonların önlenmesi.
Sirotik hastalarda kanamayı durdurmak ve gastroözofageal varislerin neden olduğu yeniden kanamaya karşı korunmak için acil tedavi. Sandostatin, endoskopik skleroterapi gibi spesifik bir tedavi ile birlikte kullanılmalıdır.
TSH salgılayan hipofiz adenomlarının tedavisi:
• ameliyat ve/veya radyoterapi sonrası salgı normale dönmediğinde;
• ameliyatın uygun olmadığı hastalarda;
• ışınlanmış hastalarda, radyoterapi etkinliğe ulaşana kadar.
04.2 Pozoloji ve uygulama yöntemi
Dozaj
akromegali
Deri altından her 8 ila 12 saatte bir 0,05 - 0,1 mg Sandostatin ile başlayın.
Herhangi bir pozolojik değişiklik, GH ve IGF-1'in plazma konsantrasyonlarının aylık kontrolleri temelinde belirlenmelidir (referans değer: GH
SANDOSTATİN tedavisine başlandıktan sonraki 3 ay içinde GH düzeylerinde tutarlı bir azalma ve klinik semptomlarda iyileşme sağlanamazsa, tedavi kesilmelidir.
Gastro-entero-pankreatik endokrin tümörler
Günde bir veya iki kez subkutan olarak 0,05 mg Sandostatin ile başlayın.
Klinik yanıt, tümör tarafından üretilen hormon seviyeleri üzerindeki etki (karsinoid tümörler durumunda, idrardaki 5-hidroksiindolasetik asit konsantrasyonları) ve tolere edilebilirlik, dozaj
kademeli olarak günde 3 kez 0.1 - 0.2 mg'a yükseltilebilir. Bazı istisnai durumlarda daha yüksek dozlara başvurmak gerekir. Bakım dozları bireysel hastaya göre ayarlanmalıdır.
Karsinoid tümörlerde, tolere edilen maksimum dozda SANDOSTATİN ile tedaviye başlandıktan sonraki 1 hafta içinde herhangi bir fayda sağlanamazsa tedavi kesilmelidir.
Pankreas ameliyatından kaynaklanan komplikasyonlar
laparotomiden en az 1 saat önce ameliyat gününden başlayarak, ardışık 7 gün boyunca günde 3 kez deri altından 0.1 mg.
Gastro-varis kanaması-yemek borusu
5 gün boyunca sürekli intravenöz (i.v.) infüzyon olarak 25 mcg/saat. Sandostatin salin içinde seyreltilerek uygulanabilir.
Gastroözofageal varis kanaması olan sirotik hastalarda, SANDOSTATİN 5 gün boyunca 50 mcg/saat'e kadar sürekli intravenöz infüzyonda iyi tolere edilmiştir.
TSH salgılayan hipofiz adenomlarının tedavisi
Genellikle en etkili doz, deri altı enjeksiyon yoluyla günde üç kez 100 mikrogramdır. Doz, TSH ve tiroid hormonlarının yanıtlarına göre ayarlanabilir. Etkinliği değerlendirmek için en az 5 günlük tedavi gerekecektir.
Yaşlı hastalarda kullanım
Sandostatin ile tedavi edilen yaşlı hastalarda tolere edilebilirliğin azaldığına veya doz ayarlaması gerektiğine dair bir kanıt yoktur.
Çocuklarda kullanım
Çocuklarda Sandostatin kullanımı ile ilgili deneyimler sınırlıdır.
Karaciğer fonksiyon bozukluğu olan hastalarda kullanım
Karaciğer sirozu olan hastalarda, ilacın yarı ömrü artabilir ve idame doz ayarlaması gerekebilir.
Böbrek fonksiyon bozukluğu olan hastalarda kullanım
Bozulmuş böbrek fonksiyonu, subkutan uygulanan oktreotid için toplam maruziyeti (EAA) etkilememiştir, bu nedenle Sandostatin doz ayarlaması gerekli değildir.
04.3 Kontrendikasyonlar
Etkin maddeye veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
04.4 Özel uyarılar ve uygun kullanım önlemleri
Genel
GH salgılayan hipofiz tümörleri bazen ciddi komplikasyonlara (örneğin görme alanı değişiklikleri) neden olarak genişleyebildiğinden, tüm hastaların dikkatli bir şekilde izlenmesi önemlidir. Tümör genişlemesi durumunda, alternatif prosedürlerin olasılığı göz önünde bulundurulmalıdır.
Akromegali kadın hastalarda, azalan büyüme hormonu (GH) seviyelerinin terapötik faydaları ve insülin benzeri büyüme faktörü 1'in (IGF-1) normalleşmesi, doğurganlığı potansiyel olarak geri getirebilir. gerekirse oktreotid ile tedavi (ayrıca bkz. bölüm 4.6).
Oktreotid ile uzun süreli tedavi gören hastalarda tiroid fonksiyonu izlenmelidir.
Oktreotid tedavisi sırasında karaciğer fonksiyonu izlenmelidir.
Kardiyovasküler sistem ile ilgili olaylar
Yaygın bradikardi vakaları bildirilmiştir. Beta blokerler, kalsiyum kanal blokerleri veya su ve elektrolit dengesini kontrol eden ajanlar gibi ilaçların doz ayarlamaları gerekli olabilir (bkz. bölüm 4.5).
Safra kesesi ve ilgili olaylar
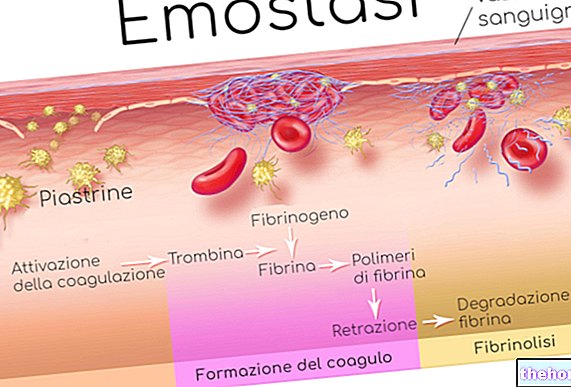
Oktreotid, kolesistokinin salgılanmasını engelleyerek safra kesesinin kontraktilitesinin azalmasına ve kum ve taş oluşumu riskinin artmasına neden olur.Safra taşı oluşum insidansının %15-30 arasında olduğu tahmin edilmektedir. Genel popülasyondaki insidans yaklaşık %5 - 20'dir.Ancak, SANDOSTATİN ile tedavi sırasında hem öncesinde hem de 6 ila 12 aylık aralıklarla safra kesesinin ultrason kontrolü önerilir.Safra taşları varsa, genellikle asemptomatiktir; eğer semptomatik iseler safra asitleri ile eritilerek veya ameliyatla tedavi edilebilir.
Gastroenteropankreatik endokrin tümörler (GEP)
GEP endokrin tümörlerinin tedavisi sırasında, şiddetli semptomların yeniden ortaya çıkmasıyla birlikte ani semptom kontrolünün kaybedildiği nadir vakalar olabilir. Tedavi durdurulursa semptomlar kötüleşebilir veya tekrarlayabilir.
Karbonhidrat metabolizması
Büyüme hormonu, glukagon ve insülin salınımı üzerindeki inhibitör etkisinden dolayı Sandostatin, glukoz metabolizmasının düzenlenmesini etkileyebilir. Postprandiyal glukoz toleransı bozulabilir ve bazı durumlarda kronik ilaç uygulamasının bir sonucu olarak kalıcı hiperglisemi indüklenebilir. Hipoglisemi de bildirilmiştir.
İnsülinoma hastalarında, oktreotidin büyüme hormonu ve glukagon sekresyonunu insüline göre daha fazla nispi inhibisyon potansiyeline sahip olması ve insülin üzerindeki inhibitör etki süresinin daha kısa olması nedeniyle, oktreotid hipogliseminin şiddetini artırabilir ve süresini uzatabilir. SANDOSTATİN tedavisinin başlangıcında ve dozajda herhangi bir değişiklik olduğunda yakından izlenmelidir. Daha kısa aralıklarla daha küçük dozlar verilerek kan şekerindeki aşırı değişiklikler kontrol altına alınabilir.
Tip I insüline bağımlı diabetes mellitus durumunda, SANDOSTATİN uygulamasıyla insülin gereksinimi azaltılabilir. Diyabetik olmayan hastalarda ve kısmen sağlam insülin rezervi olan Tip II diyabetli hastalarda SANDOSTATİN uygulaması, tokluk kan şekerinde artışa neden olabilir. Bu nedenle glukoz toleransının ve antidiyabetik tedavinin izlenmesi önerilir.
yemek borusu varisleri
Özofagus varislerine bağlı kanama ataklarını takiben, insüline bağımlı diyabet gelişme riski veya önceden diyabeti olan hastalarda insülin gereksinimi artabileceğinden, kan şekeri seviyeleri dikkatle izlenmelidir.
Enjeksiyon bölgesinde lokal reaksiyonlar
Başta erkek olmak üzere sıçanlarda yapılan 52 haftalık bir toksisite çalışmasında, deri altı enjeksiyon bölgesinde yalnızca en yüksek dozda (vücut yüzey alanına dayalı olarak maksimum insan dozunun yaklaşık 8 katı) sarkomlar gözlenmiştir. 52 haftalık bir köpek toksisite çalışmasında deri altı enjeksiyon bölgesinde hiçbir hiperplastik veya neoplastik lezyon meydana gelmemiştir. 15 yıla kadar SANDOSTATİN ile tedavi edilen hastalarda enjeksiyon bölgelerinde tümör oluşumuna ilişkin herhangi bir rapor bulunmamaktadır. Şu anda mevcut tüm bilgiler, sıçanlarda gözlemlenen bulguların türe özgü olduğunu ve ilacın insanlarda kullanımıyla ilgili olmadığını göstermektedir (bkz. bölüm 5.3).
Beslenme
Bazı hastalarda, oktreotid diyet yağının emilimini bozabilir.
Oktreotid alan bazı hastalarda B12 vitamini seviyelerinde tutarlı bir düşüş ve anormal Schilling testi sonuçları gözlenmiştir. Daha önce vitamin B12 eksikliği atakları geçirmiş hastalarda SANDOSTATİN tedavisi sırasında vitamin B12 düzeylerinin izlenmesi önerilir.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
SANDOSTATİN birlikte uygulandığında beta blokerler, kalsiyum kanal blokerleri veya sıvı ve elektrolit kontrol ajanları gibi ilaçların doz ayarlaması gerekebilir (bkz. bölüm 4.4).
Sandostatin birlikte uygulandığında insülin ve antidiyabetik ilaçların doz ayarlaması gerekebilir (bkz. bölüm 4.4).
Octreotidin, siklosporinin bağırsak emilimini azalttığı ve simetidininkini geciktirdiği gösterilmiştir.
Oktreotid ve bromokriptinin birlikte uygulanması, bromokriptinin biyoyararlanımını arttırır.
Sınırlı yayınlanmış veriler, somatostatin analoglarının, büyüme hormonu baskılanması nedeniyle sitokrom P450 enzimleri tarafından metabolize edildiği bilinen bileşiklerin metabolik klirensini azaltabileceğini göstermektedir.Octreotidin bu etkiye sahip olduğu göz ardı edilemeyeceğinden, bu nedenle göz ardı edilmelidir. esas olarak CYP3A4 tarafından metabolize edilen ve düşük terapötik indekse sahip diğer ilaçlar (örn. kinidin, terfenadin).
04.6 Hamilelik ve emzirme
Gebelik
Gebe kadınlarda (300'den az maruz kalan gebelik) oktretotid kullanımına ilişkin sınırlı veri vardır ve vakaların yaklaşık üçte birinde gebelik sonuçları bilinmemektedir. Çoğu kadın, gebeliğin ilk üç ayında, subkutan olarak uygulanan 100 ila 1200 mcg/gün SANDOSTATİN veya 10 ila 40 mg/ay SANDOSTATİN LAR arasında değişen dozlarda oktreotide maruz kalmıştır. Sonucu bilinen gebeliklerin %4'ü Bu vakalar için oktreotid ile nedensel bir ilişkiden şüphelenilmemiştir.
Hayvanlar üzerinde yapılan çalışmalar üreme toksisitesi açısından doğrudan veya dolaylı zararlı etkiler göstermemektedir (bkz. bölüm 5.3).
Önlem olarak hamilelik sırasında Sandostatin kullanmaktan kaçınılması tercih edilir (bkz. bölüm 4.4).
Besleme zamanı
Oktreotidin insan sütüne geçip geçmediği bilinmemektedir Hayvan çalışmaları oktreotidin insan sütüne geçtiğini göstermiştir. SANDOSTATİN tedavisi sırasında hastalar emzirmemelidir.
Doğurganlık
Oktreotidin insan doğurganlığı üzerinde bir etkisi olup olmadığı bilinmemektedir. Hamilelik ve emzirme döneminde tedavi edilen annelerden doğan erkeklerde, testislerin inişinde bir gecikme gözlemlenmiştir, ancak Octreotid, erkek ve dişi sıçanlarda günde 1 mg/kg vücut ağırlığına kadar olan dozlarda doğurganlığı bozmamıştır (bakınız paragraf 5.3).
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
SANDOSTATİN'in araç veya makine kullanma yeteneği üzerinde etkisi yoktur veya ihmal edilebilir düzeydedir. SANDOSTATİN kullanırken baş dönmesi, asteni/yorgunluk veya baş ağrısı yaşarlarsa, hastalara araç veya makine kullanırken dikkatli olmaları tavsiye edilmelidir.
04.8 İstenmeyen etkiler
Güvenlik profilinin özeti
Oktreotid tedavisi sırasında en sık bildirilen advers reaksiyonlar gastrointestinal bozukluklar, sinir sistemi bozuklukları, hepatobiliyer bozukluklar ve metabolizma ve beslenme bozukluklarını içerir.
Oktreotid ile yapılan klinik deneyler sırasında en sık bildirilen advers reaksiyonlar diyare, karın ağrısı, bulantı, gaz, baş ağrısı, kolelitiazis, hiperglisemi ve kabızlıktır. Yaygın olarak bildirilen diğer advers reaksiyonlar baş dönmesi, lokalize ağrı, safra çamuru, tiroid disfonksiyonu (örneğin tiroid hormonunda [TSH] azalma, toplam ve serbest T4 azalması), gevşek dışkı, bozulmuş glukoz toleransı, kusma, asteni ve hipoglisemidir.
Advers reaksiyon tablosu
Tablo 1'de listelenen aşağıdaki advers ilaç reaksiyonları, oktreotid ile yapılan klinik çalışmalar sırasında toplanmıştır:
Advers ilaç reaksiyonları (Tablo 1) sıklık kategorisine göre, en sık görülen reaksiyon ilk önce aşağıdaki düzen kullanılarak listelenmiştir: çok yaygın (≥1/10); yaygın (≥1 / 100,
Tablo 1 Klinik çalışmalarda bildirilen advers ilaç reaksiyonları
Pazarlama sonrası
Tablo 2'de sunulan spontan olarak bildirilen advers ilaç reaksiyonları gönüllü olarak rapor edilmiştir ve ilaca maruz kalma sıklığı veya nedensel bir ilişkiyi güvenilir bir şekilde belirlemek her zaman mümkün değildir.
Tablo 2 Spontan raporlardan elde edilen advers ilaç reaksiyonları
Seçilmiş advers reaksiyonların tanımı
Gastrointestinal bozukluklar
Nadir durumlarda, gastrointestinal sistemi etkileyen advers olaylar, ilerleyici abdominal distansiyon, epigastrik bölgede şiddetli ağrı, karın ağrısı ve abdominal defans reaksiyonu ile birlikte akut intestinal obstrüksiyon özellikleri gösterebilir.
Gastrointestinal advers olayların sıklığının, devam eden tedavi ile zamanla azaldığı bilinmektedir.
Gastrointestinal yan etkilerin ortaya çıkması, Sandostatin'in öğünler arasında deri altından uygulanmasıyla, yani öğünler arasında veya yatmadan önce enjekte edilmesiyle azaltılabilir.
Enjeksiyon bölgesi reaksiyonları
Deri altı enjeksiyon bölgesinde nadiren 15 dakikadan uzun süren kızarıklık ve şişme ile birlikte ağrı veya iğnelenme, karıncalanma veya yanma hissi Çözelti oda sıcaklığına ulaştığında enjekte edilerek veya hacim azaltılarak lokal rahatsızlık azaltılabilir. daha konsantre bir formülasyon kullanılarak enjekte edilebilir.
Metabolizma ve beslenme bozuklukları
Ölçülen fekal yağ atılımı artabilse de, oktreotid ile uzun süreli tedavinin malabsorpsiyondan kaynaklanan bir beslenme eksikliğine neden olduğuna dair bugüne kadar hiçbir kanıt yoktur.
pankreas enzimleri
Çok nadir vakalarda, subkutan SANDOSTATİN tedavisinin ilk saatleri veya günleri içinde akut pankreatit rapor edilmiş ve ilacın kesilmesiyle düzelmiştir. Ek olarak, deri altı Sandostatin ile uzun süreli tedavi gören hastalarda kolelitiazis kaynaklı pankreatit bildirilmiştir.
Kardiyak patolojiler
Hem akromegali hastalarında hem de karsinoid sendromlu hastalarda QT uzaması, eksenel sapma, erken repolarizasyon, düşük voltaj, R/S geçişi, erken R dalgası ilerlemesi ve spesifik olmayan ST dalgası değişiklikleri gibi elektrokardiyografik değişiklikler gözlenmiştir. Bu hastaların çoğunda altta yatan kalp hastalığı bulunduğundan, bu olaylar ile oktreotid asetat tedavisi arasındaki ilişki kurulmamıştır (bkz. bölüm 4.4).
Şüpheli advers reaksiyonların raporlanması
İlacın ruhsatlandırılmasından sonra meydana gelen şüpheli advers reaksiyonların raporlanması, tıbbi ürünün fayda/risk dengesinin sürekli olarak izlenmesine imkan verdiği için önemlidir. Sağlık profesyonellerinden şüpheli advers reaksiyonları ulusal raporlama sistemi aracılığıyla bildirmeleri istenmektedir. "adres: www .agenziafarmaco.gov.it/it/responsabili
04.9 Doz aşımı
Yetişkinlerde ve çocuklarda sınırlı sayıda kazara aşırı doz Sandostatin vakası bildirilmiştir. Erişkinlerde, sürekli infüzyon (100-250 mcg/saat) veya subkutan (günde üç kez 1.500 mcg) uygulanan dozlar 2.400 ila 6.000 mcg / gün arasında değişmektedir. Bildirilen advers olaylar aritmi, hipotansiyon, kalp durması, serebral hipoksi, pankreatit, karaciğer yağlanması, ishal, halsizlik, uyuşukluk, kilo kaybı, hepatomegali ve laktik asidozdur.
Çocuklarda dozlar, sürekli infüzyon (2.1-500 mcg/saat) veya subkutan (50-100 mcg) olarak verilen 50 ila 3.000 mcg/gün aralığındadır. Bildirilen tek advers olay hafif hiperglisemidir.
Bölünmüş dozlar halinde subkutan olarak 3000 ila 30.000 mcg/gün dozlarında SANDOSTATİN alan kanser hastalarında beklenmeyen advers olaylar bildirilmemiştir.
Doz aşımı durumunda tedavi semptomatiktir.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: somatostatin ve analogları.
ATC kodu: H01CB02.
Octreotid sentetik bir oktapeptid, doğal somatostatinin yapısal analoğudur, çok benzer farmakolojik aktiviteye sahip ancak önemli ölçüde daha uzun etki süresine sahiptir.Sistemde üretilen büyüme hormonu (GH) ve peptitlerin ve serotoninin salgılanmasındaki patolojik artışı engeller. entero-pankreatik endokrin (GEP).
Hayvanlarda oktreotidin, GH ve glukagon baskılanması için daha belirgin seçicilik ile somatostatinden daha güçlü bir GH, glukkon ve insülin salma inhibitörü olduğu gösterilmiştir.
Sağlıklı gönüllülerde Sandostatin'in şunları inhibe ettiği gösterilmiştir:
• arginin kaynaklı GH salınımı, egzersiz ve insülin kaynaklı hipoglisemi,
• insülin, glukagon, gastrin ve endokrin sistem GEP'inin diğer peptitlerinin tokluk sonrası salınımı ve arginin tarafından indüklenen insülin ve glukonun salınımı,
• TRH hormonu (tirotropin salgılayan hormon) tarafından indüklenen TSH (tirotropik hormon) salınımı.
Somatostatinden farklı olarak oktreotid, GH sekresyonunu inhibe etmede insülinden daha güçlüdür; uygulamasını takiben hormonların rebound hipersekresyonu (örn. akromegali hastalarında GH) izlenmez.
Akromegali hastalarında SANDOSTATİN plazma GH ve IGF-1 düzeylerini düşürür. Hastaların yaklaşık %90'ında GH'de yaklaşık %50 veya daha fazla azalma ve serum GH, baş ağrısı, cilt ve yumuşak doku ödemi, hiperhidroz, artralji, parestezide bir azalma meydana gelir. Büyük bir hipofiz adenomu olan hastalarda SANDOSTATİN ile tedavi tümör kütlesinde azalmaya neden olabilir.
Gastro-entero-pankreatik endokrin sisteminin işlevsel tümörleri olan hastalarda, çeşitli endokrin etkileri nedeniyle Sandostatin ile tedavi, bir dizi klinik semptomu değiştirir. Cerrahi, hepatik arter embolizasyonu ve çeşitli kemoterapileri (örn., streptozosin ve 5-florourasil) içerebilen önceki tedavilere rağmen tümörlerine atfedilen semptomları hala gösteren hastalarda klinik iyileşme ve semptomatik fayda görülür.
Sandostatin'in farklı kanser türlerindeki etkileri aşağıdaki gibidir:
karsinoid tümörler
Oktreotid uygulaması, özellikle sıcak basması ve ishal semptomlarının iyileşmesine neden olabilir. Çoğu durumda, buna plazma serotonininde bir azalma ve 5-hidroksiindolasetik asidin idrarla atılımında bir azalma eşlik eder.
VIPomi
Bu tümörlerin biyokimyasal özellikleri, vazoaktif bağırsak peptidinin (VIP) aşırı üretiminden oluşur. Çoğu durumda, SANDOSTATİN uygulaması, "bu duruma özgü tipik şiddetli sekretuar diyarenin zayıflaması ve bunun sonucunda yaşam kalitesinde iyileşme ile sonuçlanır. Buna hipokalemi gibi ilişkili elektrolit anormalliklerinde bir iyileşme eşlik eder" enteral ve parenteral elektrolit sıvı beslenmesinin askıya alınması. Bazı hastalarda bilgisayarlı tomografi, özellikle karaciğer metastazlarında tümör progresyonunda bir azalma veya duraklama, hatta azalma gösterir.Klinik iyileşmeye genellikle plazma VIP seviyelerinde normal değerlere ulaşabilen bir azalma eşlik eder.
glukagonomlar
Sandostatin uygulaması, çoğu durumda bu durumun özelliği olan nekrolitik göçmen döküntüde önemli bir iyileşme ile sonuçlanır. SANDOSTATİN'in sıklıkla meydana gelen hafif diabetes mellitus koşulları üzerindeki etkisi belirgin değildir ve genellikle insülin veya oral hipoglisemik ajan dozlarının azalmasına neden olmaz Sandostatin, bu durumdaki hastalarda diyarenin iyileşmesine ve dolayısıyla kilonun artmasına neden olur. Sandostatin uygulaması sıklıkla plazma glukagon seviyelerinde ani bir azalmaya yol açsa da, bu azalma, semptomatik iyileşmenin devam etmesine rağmen, genellikle uzun bir uygulama periyodu boyunca korunmaz.
Gastrinomalar / Zollinger-Ellison Sendromu
Proton pompa inhibitörü veya H2 reseptör inhibitörü tedavisi genellikle gastrik asit hipersekresyonunu kontrol eder.Ancak, aynı zamanda baskın bir semptom olan diyare, proton pompa inhibitörleri veya H2 reseptör inhibitörleri tarafından yeterince rahatlamayabilir.Sandostatin, gastrik asit hipersekresyonunu daha da azaltmaya ve iyileştirmeye yardımcı olabilir. bazı hastalarda yüksek gastrin seviyelerini baskılayarak ishal dahil semptomlar.
insülinomlar
Sandostatin uygulaması, kısa süreli (yaklaşık 2 saat) olabilen immünoreaktif insülinin plazma konsantrasyonlarında bir azalmaya neden olur. Operatif tümörleri olan hastalarda SANDOSTATİN, normogliseminin ameliyat öncesi seviyelerde düzeltilmesine ve korunmasına yardımcı olur. Ameliyat edilemeyen iyi huylu veya kötü huylu tümörleri olan hastalarda, dolaşımdaki insülin seviyelerinde sürekli azalma olmadan bile glisemik kontrol iyileştirilebilir.
Pankreas ameliyatından kaynaklanan komplikasyonlar
Pankreas cerrahisi geçiren hastalarda, SANDOSTATİN'in ameliyat sırasında ve sonrasında uygulanması, tipik ameliyat sonrası komplikasyonların (örneğin pankreas fistülleri, apse ve müteakip sepsis, akut postoperatif pankreatit) insidansını azaltır.
Gastroözofageal varis kanaması
Altta yatan siroz nedeniyle gastroözofageal varis kanaması olan hastalarda, SANDOSTATİN'in spesifik tedavilerle (örn. sklerozan tedavi) kombinasyon halinde uygulanması, hemorajinin ve erken yeniden kanamanın daha iyi kontrolü, transfüzyon ihtiyacının azalması ve doğumda sağkalımın artması ile ilişkilidir. 5. gün Sandostatin'in kesin etki şekli tam olarak bilinmemekle birlikte, Sandostatin'in vazoaktif hormonların (örn. VIP, glukagon) inhibisyonu yoluyla splanknik kan akışını azalttığı söylenebilir.
TSH salgılayan hipofiz adenomlarının tedavisi
Sandostatin tedavisinin etkileri prospektif olarak 21 hastada gözlendi ve yayınlanmış 37 vakadan oluşan bir seri ile birleştirildi. Değerlendirilebilir biyokimyasal verileri olan 42 hastanın %81'inde (n = 34) tatmin edici sonuçlar (TSH'de en az %50 azalma ve tiroid hormonlarında önemli azalma), %67'sinde (n = 28) TSH normalleşmesi ve tiroid hormonları Bu hastalarda, yanıt tedavi süresi boyunca korunmuştur (61 aya kadar, ortalama 15.7 ay).
Klinik semptomlarla ilgili olarak, klinik hipertiroidizmi olan 32 hastanın 19'unda belirgin bir iyileşme bildirilmiştir. 11 vakada (%41) %20'den fazla tümör hacminde azalma ve 4 vakada (%15) %50'den fazla azalma gözlendi.En erken azalma 14 günlük tedaviden sonra rapor edilmiştir.
05.2 "Farmakokinetik özellikler
absorpsiyon
Subkutan uygulamadan sonra SANDOSTATİN hızla ve tamamen emilir. Maksimum plazma konsantrasyonuna 30 dakika içinde ulaşılır.
Dağıtım
Dağılım hacmi 0.27 L/kg ve toplam klerens 160 mL/dk'dır. Plazma protein bağlanması yaklaşık %65'tir. Kırmızı kan hücrelerine bağlanan Sandostatin miktarı ihmal edilebilir düzeydedir.
Eliminasyon
Subkütan uygulamadan sonra eliminasyon yarı ömrü 100 dakikadır İntravenöz uygulamadan sonra eliminasyon bifaziktir, yarılanma ömürleri sırasıyla 10 ve 90 dakikadır. Peptitin çoğu feçes yoluyla atılırken, yaklaşık %32'si değişmeden idrar yoluyla atılır.
Özel hasta kategorileri
Bozulmuş böbrek fonksiyonu, subkutan enjeksiyon olarak verilen toplam oktreotid maruziyetini (EAA) etkilememiştir.
Karaciğer sirozu olan hastalarda eliminasyon kapasitesi azalabilir, ancak karaciğer yağlanması olan hastalarda azalmaz.
05.3 Klinik öncesi güvenlik verileri
Akut ve tekrarlanan doz toksisitesi, genotoksisite, kanserojen potansiyel ve üreme toksisitesi ile ilgili hayvan çalışmaları, insanlar için özel bir tehlike göstermemiştir.
Hayvanlarda yapılan üreme çalışmaları, 1 mg / kg / gün'e kadar dozlarda parenteral olarak uygulanan oktreotid nedeniyle teratojenik, embriyo / fetal veya diğer üreme etkilerine dair hiçbir kanıt göstermedi. Sıçan yavrularının fizyolojik büyümesinde gözlenen bazı gecikmeler geçicidir ve aşırı farmakodinamik aktiviteye bağlı "GH inhibisyonuna" bağlanabilir (bkz. bölüm 4.6).
Jüvenil sıçanlarda spesifik bir çalışma yapılmamıştır. Prenatal ve postnatal gelişim çalışmalarında, gebelik ve emzirme döneminde oktreotid alan annelerin F1 yavrularında büyüme ve olgunlaşmada azalma gözlenmiştir.Erkek F1 yavrularında testislerde gecikme gözlenmiş ancak bu erkek F1 yavrularının doğurganlıkları normal kalmıştır. yukarıda bahsedilen etkiler geçiciydi ve GH inhibisyonunun bir sonucu olarak kabul edildi.
Kanserojenite / kronik toksisite
1.25 mg/kg vücut ağırlığına kadar günlük dozlarda oktreotid asetat ile tedavi edilen sıçanlarda, 52, 104 ve 113/116 hafta sonra enjeksiyon bölgesinde ağırlıklı olarak birkaç erkek hayvanda fibrosarkomlar gözlendi. Kontrol sıçanlarında da lokal tümörler meydana geldi, ancak bu tümörlerin gelişimi, laktik asit / mannitol aracı ile takviye edilen enjeksiyon bölgelerinde uzun süreli tahriş edici etkiler tarafından üretilen düzensiz fibroplaziye bağlandı. Bu spesifik olmayan doku reaksiyonunun farelere özel olduğu ortaya çıktı. Neoplastik lezyonlar, 98 hafta boyunca 2 mg/kg'a kadar dozlarda günlük subkutan oktreotid enjeksiyonları ile tedavi edilen farelerde veya 52 hafta boyunca günlük subkutan ilaç dozları enjeksiyonları ile tedavi edilen köpeklerde gözlenmedi.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
Sandostatin 0.05 - 0.1 - 0.5 mg / 1 ml ampuller, enjeksiyon için çözelti (deri altı kullanımı) veya infüzyon çözeltisi için konsantre (intravenöz infüzyon)
Yardımcı maddeler: laktik asit, mannitol, sodyum bikarbonat, enjeksiyonluk su.
Sandostatin 1 mg / 5 ml (0,2 mg/ml) çok dozlu flakonlar, enjeksiyonluk çözelti (deri altı kullanımı) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon)
Yardımcı maddeler: laktik asit, fenol, mannitol, sodyum bikarbonat, enjeksiyonluk su.
06.2 Uyumsuzluk
Octreotid asetat, total parenteral beslenme (NPT) solüsyonlarında stabil değildir.
06.3 Geçerlilik süresi
Sandostatin 0,05 - 0,1 - 0,5 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon): 3 yıl.
Sandostatin 1 mg / 5 ml (0,2 mg/ml) çok dozlu flakonlar, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon): 4 yıl.
06.4 Depolama için özel önlemler
Uzun süreli saklama için hem ampuller hem de şişeler 2 °C ile 8 °C arasında bir sıcaklıkta tutulmalıdır. Işıktan uzak tutmak için orijinal ambalajında saklayın.
Sandostatin 0,05 - 0,1 - 0,5 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon):
Günlük kullanım sırasında 30°C'de 2 hafta süreyle saklayınız.
Sandostatin 1 mg / 5 ml (0,2 mg/ml) çok dozlu flakonlar, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon):
Günlük kullanım sırasında oda sıcaklığında saklayınız.
Şişe: dondurmayın.
SANDOSTATİN, ÇOCUKLARIN ERİŞİMİNDEN VE GÖRÜŞÜNDEN UZAK TUTULMALIDIR
06.5 İç ambalajın yapısı ve paketin içeriği
Sandostatin 0.05 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): 5 ampul 1 ml.
Sandostatin 0.1 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): 5 ampul 1 ml.
Sandostatin 0,5 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): 1 ml'lik 3 ampul.
Renksiz cam şişeler
Sandostatin 1 mg / 5 ml (0,2 mg/ml) çok dozlu flakonlar, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): 1 şişe 5 ml.
lastik tıpa ile kapatılmış renksiz cam şişe.
06.6 Kullanım ve kullanım talimatları
deri altı uygulama
Tıbbi veya hemşirelik personeli, subkutan enjeksiyonları kendileri yapmak isteyen hastalara uygun şekilde talimat vermelidir.
Daha iyi bir lokal tolere edilebilirlik için, çözeltinin oda sıcaklığında uygulanması ve kısa sürede, kapalı alanlarda tekrarlanan enjeksiyonlar yapılmaması tavsiye edilir.
Ampuller uygulamadan önce açılmalı ve kullanılmayan miktarlar atılmalıdır.
Mikrobiyolojik açıdan ürün hemen kullanılmalıdır.
Şişeler kullanılıyorsa, kontaminasyon fenomenini önlemek için aynı şişeden 10'dan fazla ilaç çekimi yapılmaması tavsiye edilir. Düşük dozlarda 0,5 ml'den az çekmeyin, sabit konsantrasyonlu tekli flakonlar kullanın.
İntravenöz infüzyon yoluyla uygulama
Parenteral uygulamaya yönelik ürünler, renk değişiklikleri ve partikül varlığı açısından uygulamadan önce görsel olarak incelenmelidir.
SANDOSTATİN'in intravenöz infüzyon yoluyla uygulanması durumunda, 0,5 mg'lık bir flakonun içeriği genellikle 60 ml fizyolojik salin içinde çözülmeli ve elde edilen çözelti bir infüzyon pompası kullanılarak uygulanmalıdır. öngörülen tedavi süresi için gerekli olan Sandostatin ayrıca daha düşük konsantrasyonlarda infüze edildi.
Şişeler: Bu, OPC (One Point Cut) ön kırma sistemine sahip bir şişedir. Ampulleri doğru şekilde açmak için kullanma talimatında verilen talimatları takip etmek gerekir.
Kullanılmayan ilaçlar ve bu ilaçtan kaynaklanan atıklar yerel yönetmeliklere uygun olarak atılmalıdır.
07.0 PAZARLAMA YETKİ SAHİBİ
Novartis Farma S.p.A.
Largo Umberto Boccioni, 1 - 21040 Origgio (VA)
08.0 PAZARLAMA YETKİ NUMARASI
Sandostatin 0,05 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): A.I.C. n. 027083017
Sandostatin 0.1 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): A.I.C. n. 027083029
Sandostatin 0,5 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti için konsantre (intravenöz infüzyon): A.I.C. n. 027083031
Sandostatin 1 mg / 5 ml (0,2 mg/ml) çok dozlu flakonlar, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon): A.I.C. n. 027083043
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
Sandostatin 0,05 - 0,1 - 0,5 mg / 1 ml ampuller, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon)
İlk yetkilendirme: 02.05.1989 / Yenileme: 01.06.2010
Sandostatin 1 mg / 5 ml (0,2 mg/ml) çok dozlu flakonlar, enjeksiyonluk çözelti (deri altı kullanım) veya infüzyonluk çözelti konsantresi (intravenöz infüzyon)
İlk yetkilendirme: 02.05.1989 / Yenileme: 01.06.2010
10.0 METİN REVİZYON TARİHİ
09/2015