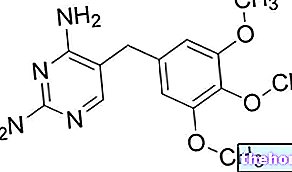
Aktif maddeler: Risperidon
Risperdal 25, 37.5 ve 50 mg intramüsküler kullanım için enjeksiyonluk uzun süreli salımlı süspansiyon için toz ve solvent
Paket boyutları için Risperdal paket ekleri mevcuttur:- Risperdal 1, 2, 3 ve 4 mg film kaplı tabletler, Risperdal 1 ve 2 mg ağızda dağılan tabletler, Risperdal 1 mg/ml oral damlalar, solüsyon
- Risperdal 25, 37.5 ve 50 mg intramüsküler kullanım için enjeksiyon için uzun süreli salımlı süspansiyon için toz ve solvent
Risperdal neden kullanılır? Bu ne için?
Risperdal Consta, "antipsikotikler" adı verilen bir ilaç grubuna dahildir.
Risperdal Consta, orada olmayan şeyleri görebileceğiniz, duyabileceğiniz veya hissedebileceğiniz, doğru olmayan şeylere inanabileceğiniz veya alışılmadık şekilde şüpheli veya kafanız karışmış hissedebileceğiniz bir durum olan şizofreninin idame tedavisi için kullanılır.
Risperdal Consta, halihazırda oral antipsikotiklerle (örneğin: tabletler, kapsüller) tedavi gören hastalar için tasarlanmıştır.
Risperdal, hastalığın semptomlarını hafifletmeye ve geri dönmesini durdurmaya yardımcı olabilir.
Kontrendikasyonlar Risperdal ne zaman kullanılmamalıdır?
Risperdal Consta'yı aşağıdaki durumlarda KULLANMAYINIZ
- Risperidon veya bu ilacın içerdiği diğer maddelerden herhangi birine karşı alerjiniz (aşırı duyarlılığınız) var.
Kullanım Önlemleri Risperdal kullanmadan önce dikkat edilmesi gerekenler
- Daha önce herhangi bir RISPERDAL formu almadıysanız, Risperdal Consta ile tedaviye başlamadan önce oral Risperdal ile başlamalısınız.
Aşağıdaki durumlarda Risperdal Consta'yı almadan önce doktorunuz veya eczacınız ile konuşunuz:
- Kalp sorunu var. Örnekler arasında düzensiz kalp ritmi veya düşük tansiyonunuz varsa veya tansiyon ilaçları alıyorsanız bulunur. Risperdal Consta kan basıncında düşüşe neden olabilir. Dozunuzun ayarlanması gerekebilir
- Yüksek tansiyon, kardiyovasküler bozukluklar veya beyin dolaşım bozuklukları gibi sizi felç riskine sokabilecek herhangi bir faktör biliyor musunuz?
- Dilinde, ağzında ve yüzünde istemsiz hareketler oldu.
- Semptomları ateş, kas sertliği, terleme veya bilinç düzeyinde azalma (Nöroleptik Malign Sendrom olarak da bilinir) içeren bir durumunuz olduysa
- Parkinson hastalığı veya bunaması var
- Geçmişte düşük seviyelerde beyaz kan hücreleriniz olduğunu biliyorsunuz (buna diğer ilaçlar neden olmuş olabilir veya olmayabilir).
- o şeker hastası
- epilepsi hastası
- O bir erkek ve uzun süreli veya ağrılı bir ereksiyon oldu.
- Vücut ısısını veya aşırı ısınmayı kontrol etmekte güçlük çekiyorsa
- böbrek problemleriniz var
- Karaciğer problemleriniz var
- Kanınızda anormal derecede yüksek bir prolaktin hormonu düzeyine sahipsiniz veya olası bir prolaktine bağımlı tümörünüz var
- Antipsikotik ilaçlar kan pıhtılarının oluşumuyla ilişkilendirildiğinden, sizin veya ailenizdeki bir başkasının kan pıhtısı (trombüs) öyküsü var.
Yukarıdaki koşullardan herhangi birinin sizin için geçerli olup olmadığından emin değilseniz, RISPERDAL'i kullanmadan önce doktorunuz veya eczacınız ile konuşunuz.
RISPERDAL ENJEKSİYONU alan hastalarda kandaki enfeksiyonlarla savaşmak için gerekli olan belirli bir tür beyaz kan hücresinin tehlikeli derecede düşük sayıları çok nadiren gözlendiğinden, doktorunuz beyaz kan hücresi sayımını kontrol edebilir.
Risperdal Consta kilo alımına neden olabilir. Önemli kilo alımı sağlığınızı olumsuz etkileyebilir. Doktorunuz kilonuzu düzenli olarak kontrol etmelidir.
Risperdal Consta alan hastalarda diabetes mellitus veya önceden var olan diabetes mellitusta kötüleşme gözlendiğinden, doktor yüksek kan şekeri düzeylerini kontrol etmelidir.
Daha önceden diabetes mellitusu olan hastalarda kan glukoz düzeyleri düzenli olarak izlenmelidir.
Merceğin bulanıklaşması (katarakt) nedeniyle bir "göz ameliyatı" sırasında, gözbebeği (gözünüzün ortasındaki siyah daire) gerektiği kadar büyüyemeyebilir. Ayrıca iris (gözün renkli kısmı) ameliyat sırasında sarkabilir ve bu da göze zarar verebilir. Göz ameliyatı olmayı planlıyorsanız, göz doktorunuza bu ilacı aldığınızı söyleyin.
Demanslı yaşlı
Risperdal Consta, demansı olan yaşlı hastalarda kullanılmak üzere tasarlanmamıştır.
Siz veya bakıcınız, zihinsel durumunuzda ani bir değişiklik veya "yüzde, kollarda veya bacaklarda, özellikle sadece bir tarafta ani zayıflık veya uyuşukluk veya kısa bir süre için bile olsa anlaşılmaz bir konuşma şekli fark ederseniz, Derhal tıbbi yardım almalısınız. Bunlar felç belirtileri olabilir.
Çocuklarda ve ergenlerde kullanım
Risperdal Consta, 18 yaşın altındaki hastalar tarafından alınmamalıdır.
Etkileşimler Hangi ilaçlar veya yiyecekler Risperdal'ın etkisini değiştirebilir?
Başka ilaçlar alıyorsanız, yakın zamanda aldıysanız veya alma ihtimaliniz varsa doktorunuza veya eczacınıza söyleyiniz. Aşağıdakilerden herhangi birini alıyorsanız doktorunuza veya eczacınıza söylemeniz özellikle önemlidir:
- Sakinleşmenize yardımcı olmak için beyninizde çalışan ilaçlar (benzodiazepinler) veya bazı ağrı kesici ilaçlar (opiatlar), alerji ilaçları (bazı antihistaminikler), çünkü risperidon tüm bu ilaçların yatıştırıcı etkilerini artırabilir.
- Sıtma ilaçları, kalp ritmi sorunları için ilaçlar, alerji ilaçları (antihistaminikler), bazı antidepresanlar veya zihinsel sorunlar için diğer ilaçlar gibi kalbinizin elektriksel aktivitesini değiştirebilen ilaçlar
- Yavaş kalp hızına neden olan ilaçlar Kanda düşük potasyuma neden olan ilaçlar (bazı diüretikler gibi)
- Artan kan basıncını tedavi etmek için ilaçlar.Risperdal Consta kan basıncında düşüşe neden olabilir
- Parkinson hastalığı ilaçları (levodopa gibi)
- Çok fazla sıvı birikmesine bağlı olarak (furosemid veya klorotiyazid gibi) kalp sorunları veya vücudun bazı kısımlarının şişmesi için kullanılan idrar söktürücü ilaçlar (diüretikler). Tek başına veya furosemid ile birlikte alınan Risperdal Consta demansı olan yaşlı hastalarda felç veya ölüm riskini artırabilir.
Aşağıdaki ilaçlar risperidonun etkisini azaltabilir:
- Rifampisin (bazı enfeksiyonların tedavisinde kullanılan bir ilaç)
- Karbamazepin, fenitoin (epilepsi ilaçları)
- Fenobarbital Bu tür ilaçları almaya başlarsanız veya bırakırsanız, farklı bir risperidon dozuna ihtiyacınız olabilir.
Aşağıdaki ilaçlar risperidonun etkisini artırabilir
- Kinidin (bazı kalp hastalıkları için kullanılır)
- Paroksetin, fluoksetin, trisiklik antidepresanlar gibi antidepresanlar
- Beta bloker olarak bilinen ilaçlar (yüksek tansiyon tedavisinde kullanılır)
- Fenotiyazinler (psikoz tedavisinde veya yatıştırıcı olarak kullanılan ilaçlar gibi)
- Simetidin, ranitidin (mide asidi blokerleri)
Bu tür ilaçları almaya başlar veya bırakırsanız, farklı bir risperidon dozuna ihtiyacınız olabilir.
Yukarıdaki koşullardan herhangi birinin sizin için geçerli olup olmadığından emin değilseniz, RISPERDAL'i kullanmadan önce doktorunuz veya eczacınız ile konuşunuz.
Yiyecek, içecek ve alkol ile Risperdal
Bu ilacı aç veya tok karnına içebilirsiniz. Risperdal Consta ile tedavi edilirken alkol almaktan kaçınmalısınız.
Uyarılar Şunları bilmek önemlidir:
Hamilelik, emzirme ve doğurganlık
- Hamileyseniz veya emziriyorsanız, hamile olabileceğinizi düşünüyorsanız veya bebek sahibi olmayı planlıyorsanız, bu ilacı almadan önce doktorunuza veya eczacınıza danışınız.
- Son trimesterde (gebeliklerinin son üç ayında) RISPERDAL kullanan annelerden doğan yenidoğan bebeklerde aşağıdaki belirtiler ortaya çıkabilir: titreme, kas sertliği ve/veya güçsüzlük, uyku hali, ajitasyon, solunum problemleri ve ilacı almada zorluk. Gıda. Bebeğiniz bu belirtilerden herhangi birini gösteriyorsa, doktorunuzla iletişime geçin.
- Risperdal Consta, doğurganlığı etkileyebilen 'prolaktin' adı verilen bir hormonun düzeylerini artırabilir (bkz. Olası yan etkiler).
Araç ve makine kullanma
Risperdal Consta ile tedavi sırasında baş dönmesi, yorgunluk ve görme sorunları meydana gelebilir. İlk önce doktorunuzla konuşmadan araç veya herhangi bir alet veya makine kullanmayınız.
Doz, Yöntem ve Uygulama Süresi Risperdal Nasıl Kullanılır: Pozoloji
Bu ilacı her zaman tam olarak doktorunuzun size söylediği şekilde alınız. Şüpheniz varsa, doktorunuza veya eczacınıza danışın. Risperdal Consta, bir sağlık uzmanı tarafından iki haftada bir kola veya kalçaya intramüsküler enjeksiyon olarak verilir. Enjeksiyonlar sağ ve sol taraflar arasında dönüşümlü olarak yapılmalı ve ürün intravenöz olarak uygulanmamalıdır.
Önerilen doz aşağıdaki gibidir:
yetişkinler
İlk doz
Son iki hafta içinde aldığınız günlük oral risperidon dozu (örn. tabletler) 4 mg veya daha azsa, başlangıç Risperdal Consta dozunuz 25 mg olmalıdır.
Son iki hafta içinde aldığınız günlük oral risperidon dozu (örn. tabletler) 4 mg'dan fazlaysa, size 37.5 mg'lık bir Risperdal Consta başlangıç dozu reçete edilebilir.
Halihazırda risperidon dışında başka oral antipsikotikler alıyorsanız, Risperdal Consta'nın başlangıç dozu, almakta olduğunuz tedaviye bağlı olacaktır. Doktorunuz Risperdal Enjektabl 25 mg veya 37.5 mg'ı seçecektir. Size 12.5 mg'lık daha düşük bir doz reçete edilebilir. Doktorunuz hangi Risperdal Consta dozunun sizin için uygun olduğuna karar verecektir.
Bakım dozu
- Olağan doz, enjeksiyon olarak iki haftada bir 25 mg'dır.
- Ayrıca 12.5 mg veya daha yüksek, 37.5 veya 50 mg gibi daha düşük bir doza ihtiyacınız olabilir. Doktorunuz hangi Risperdal Consta dozunun sizin için en iyi olduğuna karar verecektir.
- Doktorunuz, ilk enjeksiyondan sonraki ilk üç hafta boyunca oral RISPERDAL reçete edebilir.
Aşırı dozda Risperdal aldıysanız ne yapmalısınız?
Kullanmanız gerekenden daha fazla Risperdal Consta kullandıysanız
- Beklenenden fazla dozda Risperdal Consta alan hastalarda şu semptomlar görülmüştür: uyku hali, yorgunluk, anormal vücut hareketleri, ayakta durma ve yürüme sorunları, düşük kan basıncına bağlı baş dönmesi ve anormal kalp atışları. Kalbin anormal elektriksel iletimi ve nöbet vakaları bildirilmiştir.
- Derhal doktorunuza danışınız.
Risperdal Consta ile tedavinin kesilmesi
İlacın etkisini kaybeder. Belirtileriniz geri dönebileceğinden doktorunuz söylemedikçe bu ilacı almayı bırakmayın. Enjeksiyonları iki haftada bir yaptırmak için randevuları unutmadığınızdan emin olun. Randevunuza gelemeyecekseniz, "enjekte edilecek başka bir tarih" bulmak için hemen doktorunuzla temasa geçin.Bu ilacın kullanımıyla ilgili başka sorularınız varsa, doktorunuza veya eczacınıza sorun.
Yan Etkiler Risperdal'ın yan etkileri nelerdir?
Tüm ilaçlar gibi, bu ilaç da yan etkilere neden olabilir, ancak bu yan etkiler herkeste görülmez.
Aşağıdaki durumlarda derhal doktorunuza söyleyiniz:
- Damarlarınızda, özellikle bacaklarda kan pıhtıları (trombüs) olduğunu düşünüyorsunuz (belirtiler bacaklarda şişlik, ağrı ve kızarıklık içerir), kan damarları boyunca akciğerlere gidebilir, göğüs ağrısına ve nefes almada zorluğa neden olabilir. Bu belirtilerden herhangi birini fark ederseniz, derhal doktorunuza danışın.
- Demansınız var ve zihinsel durumunuzda ani bir değişiklik veya "yüzünüzde, kollarınızda veya bacaklarınızda, özellikle bir tarafta ani bir zayıflık veya uyuşukluk ya da kısa bir süre için bile olsa, diliniz anlaşılmazsa" fark ettiniz. felç belirtileri olabilir.
- Ateşiniz, kas sertliğiniz, terlemeniz veya bilinç düzeyinizde azalma (Nöroleptik Malign Sendrom adı verilen bir bozukluk) var. Acil tıbbi tedavi gerekebilir.
- Erkek ve uzamış veya ağrılı bir ereksiyon var.Bu duruma priapizm denir.Acil tıbbi tedavi gerekebilir.
- Dil, ağız ve yüzün istemsiz ritmik hareketleri vardır. Risperidon kesilmesi gerekebilir
- Ateş, ağız, yüz, dudak veya dilde şişme, nefes darlığı, kaşıntı, deri döküntüsü veya kan basıncında düşme ile karakterize şiddetli alerjik reaksiyonunuz varsa. Daha önce oral risperidonu tolere etmiş olmasına rağmen, Risperdal enjeksiyonlarını aldıktan sonra nadiren alerjik reaksiyonlar meydana gelir. Döküntü, boğazda şişme, kaşıntı veya solunum sorunları yaşarsanız, bunlar ciddi bir alerjik reaksiyonun belirtileri olabileceğinden derhal doktorunuza görünün.
Aşağıdaki yan etkiler ortaya çıkabilir:
Çok yaygın (10 kullanıcıda 1'den fazla kullanıcıyı etkiler):
- soğuk algınlığı belirtileri
- Uykuya dalmada veya uykuda kalmada zorluk
- depresyon, anksiyete
- Parkinsonizm: Bu durum şunları içerebilir: yavaş veya bozulmuş vücut hareketleri, kas sertliği veya gerginlik hissi (hareketleri sarsıntılı hale getirir) ve hatta bazen donup sonra yeniden başlayan bir hareket hissi. Parkinsonizmin diğer belirtileri arasında yavaş hareketlerle yürüme, istirahatte titreme,
Yaygın yan etkiler (100'de 1 ila 10 kullanıcıyı etkiler):
- Pnömoni, göğüs enfeksiyonu (bronşit), sinüzit
- İdrar yolu enfeksiyonu
- grip olmuş gibi hissetmek
- anemi
- Risperdal Consta, bir kan testinde bulunan 'prolaktin' adı verilen hormon düzeylerini artırabilir (belirtilere neden olabilir veya olmayabilir). Yüksek prolaktin düzeyi semptomları ortaya çıktığında, bunlar şunları içerebilir: (erkeklerde) göğüste şişme, ereksiyon sağlamada veya ereksiyonda veya diğer cinsel işlevlerde zorluk; (kadınlarda) göğüste rahatsızlık, göğüslerden süt kaybı, adet dönemlerinin olmaması veya diğer döneminizle ilgili sorunlar
- yüksek kan şekeri, kilo alımı, iştah artışı, kilo kaybı, iştah azalması
- uyku bozuklukları, sinirlilik, cinsel dürtüde azalma, ajitasyon, uykulu veya daha az uyanık hissetme
- Distoni: Bu, yavaş veya uzun süreli istemsiz kas kasılmasını içeren bir durumdur. Vücudun herhangi bir bölümünü tutabilse de (anormal duruşla sonuçlanır), distoni genellikle gözlerin, ağzın, dilin veya çenenin anormal hareketleri dahil olmak üzere yüz kaslarını içerir.
- Baş dönmesi
- Diskinezi: Bu, istemsiz kas hareketlerini içeren ve tekrarlayan, spastik veya bükülmüş hareketler veya seğirmeyi içerebilen bir durumdur.
- Titreme (sallama)
- Bulanık görme, göz enfeksiyonu veya konjonktivit
- Hızlı kalp atış hızı,
- düşük tansiyon, göğüs ağrısı, yüksek tansiyon
- nefes darlığı, boğaz ağrısı, öksürük, burun tıkanıklığı
- Karın ağrısı veya rahatsızlığı, kusma, bulantı, kabızlık, ishal, hazımsızlık, ağız kuruluğu, diş ağrısı
- erektil disfonksiyon
- adet kaybı
- memeden süt kaybı
- vücudun, kolların veya bacakların şişmesi, ateş, halsizlik, yorgunluk (yorgunluk)
- ağrı
- Kaşıntı, ağrı veya şişme dahil enjeksiyon bölgesi reaksiyonu
- Kanda artan transaminaz seviyeleri, kanda GGT artışı (gammaglutamiltransferaz adı verilen bir karaciğer enzimi), kanda karaciğer enzimlerinde artış
- düşmek
Yaygın olmayan yan etkiler (1000'de 1 ila 10 kullanıcıyı etkiler):
- solunum yolu enfeksiyonu, mesane enfeksiyonu, kulak enfeksiyonu, göz enfeksiyonu, bademcik iltihabı, tırnak mantarı enfeksiyonu, cilt enfeksiyonu
- enfeksiyon, cildin tek bir bölgesinin veya vücudun bir bölümünün enfeksiyonu, viral enfeksiyon, akarların neden olduğu cilt iltihabı, deri altı apsesi
- beyaz kan hücrelerinin sayısında azalma, trombositlerde azalma (kanamayı durdurmaya yardımcı olan kan hücreleri), kırmızı kan hücrelerinin sayısında azalma
- alerjik reaksiyon
- idrarda şeker, şeker hastalığı veya şeker hastalığının kötüleşmesi,
- yetersiz beslenme ve düşük vücut ağırlığı ile sonuçlanan iştah kaybı
- yüksek seviyelerde trigliserit (bir yağ), kanda artan kolesterol
- öfori (mani), kafa karışıklığı, orgazma ulaşamama, sinirlilik, kabus görme, geç diskinezi (yüzde, dilde veya vücudun diğer bölümlerinde kontrol edemediğiniz seğirme veya sarsıntı hareketleri) Ritmik istemsiz hareketler yaşarsanız hemen doktorunuza başvurun. dil, ağız ve yüzde Risperdal Consta'nın kesilmesi gerekli olabilir
- beyne giden ani kan kaybı (inme veya 'mini' inme),
- bilinç kaybı, bilinç düzeyinde azalma, bayılma
- Vücudun bir bölümünü acilen hareket ettirme ihtiyacı, denge bozuklukları, anormal koordinasyon, ayağa kalkarken baş dönmesi, dikkat bozukluğu, konuşma sorunları, tat kaybı veya anormal duyum, derinin ağrı ve dokunmaya karşı duyarlılığında azalma, karıncalanma, karıncalanma veya ciltte uyuşukluk hissi
- göz enfeksiyonu veya konjonktivit, göz kuruluğu, artan yırtılma, gözlerde kızarıklık
- dönme hissi (vertigo), kulaklarda çınlama, kulak ağrısı
- atriyal fibrilasyon (anormal kalp ritmi), kalbin üst ve alt kısımları arasındaki kalp iletiminde bir kesinti, kalbin anormal elektriksel iletimi, kalbin QT aralığının uzaması, yavaş kalp hızı, kalbin anormal elektriksel izlemesi (elektrokardiyogram) veya EKG), göğüste yarış veya zonklama hissi (çarpıntı)
- ayağa kalkarken düşük kan basıncı (sonuç olarak, Risperdal Consta alan bazı hastalar aniden ayağa kalkarken veya otururken baygınlık, baş dönmesi veya baygınlık hissedebilir)
- hızlı ve sığ solunum, solunum yolu tıkanıklığı, hırıltı, burun kanaması
- fekal inkontinans, yutma güçlüğü, aşırı gaz veya hava çıkışı
- kaşıntı, saç dökülmesi, egzama, kuru cilt, ciltte kızarıklık, ciltte renk değişikliği, akne, soyulma ve kaşıntılı kafa derisi veya cilt
- kandaki CPK'da (kreatin fosfokinaz) artış, kas hasarı olduğunda bazen salınan bir enzim
- eklem sertliği, eklem şişmesi, kas zayıflığı, boyun ağrısı
- sık idrara çıkma, idrar yapamama, idrar yaparken ağrı
- boşalma bozuklukları, adet gecikmesi, adet gecikmesi veya adet sorunları (kadınlarda), erkeklerde meme gelişimi, cinsel işlev bozukluğu, meme ağrısı, meme rahatsızlığı, vajinal akıntı
- yüz, ağız, göz veya dudakların şişmesi
- titreme, artan vücut ısısı
- yürüdüğün şekilde değiş
- susamış hissetmek, kendini iyi hissetmemek, göğüs ağrısı, kendini kötü hissetmek
- cildin sertleşmesi
- kanda karaciğer enzimlerinde artış
- prosedürel ağrı
Seyrek yan etkiler (10.000'de 1 ila 10 kullanıcıyı etkiler):
- enfeksiyonlarla savaşmaya yardımcı olan bazı beyaz kan hücrelerinde azalma,
- idrar hacmini kontrol eden hormonun uygunsuz salgılanması
- düşük kan şekeri
- aşırı su alımı
- duygu eksikliği
- nöroleptik malign sendrom (kafa karışıklığı, bilinç azalması veya kaybı, yüksek ateş ve şiddetli kas sertliği)
- düşük bilinç seviyesi
- kafa sallamak
- göz hareketi, göz döndürme, gözlerin ışığa aşırı duyarlılığı ile ilgili sorunlar
- Katarakt ameliyatı sırasında göz problemleri Katarakt ameliyatı sırasında Risperdal Consta aldıysanız veya aldıysanız intraoperatif floppy iris sendromu (IFIS) adı verilen bir durum oluşabilir. bu ilacı aldı.
- düzensiz kalp atışı
- enfeksiyonlarla savaşmak için gereken belirli tipte beyaz kan hücrelerinin tehlikeli derecede düşük olması, kanda eozinofillerin (özellikle beyaz kan hücreleri) artması, bacaklarda kan pıhtıları, akciğerlerde kan pıhtıları
- uyku sırasında solunum problemleri (uyku apnesi)
- gıda aspirasyonundan kaynaklanan zatürre, akciğer tıkanıklığı, akciğerlerde vızıltı sesleri, ses sorunları, solunum yolu bozukluğu
- pankreas iltihabı, kolon tıkanıklığı
- çok zorlandım
- ilaç döküntüsü
- kurdeşen, cilt kalınlaşması, kepek, cilt sorunu, cilt yaralanması
- kas liflerinin parçalanması ve kas ağrısı (rabdomiyoliz)
- anormal duruş
- göğüs büyütme, göğüslerden akıntı
- vücut ısısında azalma, rahatsızlık
- cilt ve gözlerin sararması (sarılık)
- Ateş, ağız, yüz, dudak veya dilde şişme, nefes darlığı, kaşıntı, deri döküntüsü ve bazen kan basıncında düşme ile karakterize şiddetli alerjik reaksiyon
- tehlikeli derecede aşırı su alımı
- artan insülin seviyeleri (kan şekeri seviyelerini kontrol eden bir hormon)
- beyindeki kan damarlarıyla ilgili sorunlar
- uyaranlara cevap verememe,
- kontrolsüz diyabet nedeniyle koma
- ani görme kaybı veya körlük
- glokom (göz küresinin içinde artan basınç), kapak kenarında kabuklanma
- sıcak basması, şişmiş dil,
- çatlamış dudaklar
- priapizm (cerrahi tedavi gerektirebilecek uzun süreli ve ağrılı bir ereksiyon)
- meme bezlerinin büyümesi
- vücut ısısında azalma, soğuk kollar ve bacaklar
- ilaç yoksunluğu sendromu
Çok seyrek yan etkiler (10.000'de 1'den az kullanıcıyı etkiler):
- Kontrolsüz diyabetin hayatı tehdit eden komplikasyonları
- boğazı tutabilen ve solunum güçlüğüne yol açabilen şişme ile birlikte şiddetli alerjik reaksiyon
- Tıkanmaya neden olan bağırsak kas hareketi eksikliği
Risperidona çok benzeyen paliperidon adı verilen başka bir ilacın kullanımıyla aşağıdaki yan etkiler görülmüştür, bu nedenle bu etkiler Risperdal ile de beklenebilir: ayağa kalkarken hızlı kalp atışı.
Yan etkilerden herhangi biri ciddileşirse veya bu kullanma talimatında belirtilmeyen herhangi bir yan etki fark ederseniz, lütfen doktorunuza veya eczacınıza söyleyiniz.
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuz, eczacınız veya hemşirenizle konuşun.Bu broşürde listelenmeyen olası yan etkiler de buna dahildir.Yan etkileri doğrudan https://www.aifa.gov adresindeki ulusal raporlama sistemi aracılığıyla da bildirebilirsiniz. .it/content/segnalazioni-reazioni-avverse. Yan etkileri bildirerek, bu ilacın güvenliği hakkında daha fazla bilgi sağlanmasına yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın. Karton üzerinde belirtilen son kullanma tarihinden sonra Risperdal Consta'yı kullanmayınız. Son kullanma tarihi, ayın son gününü ifade eder.
Ambalajın tamamını buzdolabında (2-8°C) saklayınız.Soğutma mümkün değilse, ürün uygulamadan önce en fazla 7 gün süreyle 25°C'yi aşmayan bir sıcaklıkta saklanabilir.
Orijinal ambalajında saklayın.
İlaçlar atık su veya evsel atıklar yoluyla atılmamalıdır.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorunuz.Bu çevrenin korunmasına yardımcı olacaktır.
Paket içeriği ve diğer bilgiler
Risperdal Consta'nın içeriği
Aktif madde risperidondur.
Her bir Risperdal tozu ve enjeksiyonluk uzun süreli salımlı süspansiyon için solvent paketi 25 mg, 37.5 mg veya 50 mg risperidon içerir.
Yardımcı maddeler şunlardır:
Toz: [poli- (d, 1-Laktid-ko-Glikolid)].
Çözücü (çözelti): polisorbat 20, karmeloz sodyum, disodyum hidrojen fosfat dihidrat, susuz sitrik asit, sodyum klorür, sodyum hidroksit, enjeksiyonluk su.
Risperdal Consta'nın görünüşü ve paketin içeriği
Enjeksiyon için uzatılmış salımlı süspansiyon için tozu içeren bir flakon (bu toz aktif madde olan risperidon içerir)
Enjeksiyonluk uzun süreli salımlı süspansiyon için toza eklenecek 2 ml berrak, renksiz sulu çözelti içeren bir kullanıma hazır şırınga.
Sulandırma için bir ALARISTM Smartsite® İğnesiz Flakon Erişim Cihazı.
Kas içi enjeksiyon için iki iğne (deltoid uygulama için Needle-Pro koruma cihazına sahip bir adet 1 inç (0,8 mm x 25 mm) 21G UTW güvenlik iğnesi ve kalçaya uygulama
SAĞLIK PROFESYONELLERİ İÇİN ÖNEMLİ BİLGİLER
İğnesiz flakon erişim cihazı için talimatlar
RISPERDAL enjektabl, başarılı bir uygulama sağlamak ve kit kullanımında zorluklardan kaçınmak için "Kullanım Talimatları"nın adımlarına özel dikkat gösterilmesini gerektirir.
Şişede bulunan risperdal enjeksiyon uzatılmış salımlı mikroküreler, yalnızca pakette sağlanan şırıngada bulunan solvent ile yeniden oluşturulmalıdır; sulandırılmış ürün, kalça (2 inç (50 mm) iğne) veya deltoid (1 inç (25 mm) iğne) içine uygulama için yalnızca paketteki uygun iğne ile uygulanmalıdır. Paketteki hiçbir bileşeni değiştirmeyin. Amaçlanan risperidon dozunun verilmesini sağlamak için flakonun tüm içeriği uygulanmalıdır. İçeriğin kısmen uygulanması, amaçlanan risperidon dozunun verilmesini garanti etmeyebilir.
Sulandırıldıktan sonra hemen uygulanması önerilir.
Enjeksiyonluk Risperdal paketini buzdolabından çıkarın ve sulandırmadan yaklaşık 30 dakika önce oda sıcaklığına getirin.
Paket içeriği:
- Enjeksiyon için uzatılmış salımlı süspansiyon için tozu içeren bir flakon (bu toz aktif madde olan risperidon içerir)
- Enjeksiyonluk uzun süreli salımlı süspansiyon için toza eklenecek 2 ml berrak, renksiz sulu çözelti içeren önceden doldurulmuş bir şırınga. 2 inç (50 mm) İĞNE 1 inç (25 mm) İĞNE
- Sulandırma için bir ALARIS ™ Smartsite İğnesiz Flakon Erişim Cihazı
- Kas içi enjeksiyon için iki iğne (deltoid uygulama için Needle-Pro koruma cihazlı bir adet 1 inç (0,8 mm x 25 mm) UTW 21G güvenli iğne ve İğneli bir adet 2 inç 20G TW güvenlik iğnesi (0 , 9 mm x 50 mm) Kalçaya uygulama için profesyonel koruma cihazı).
- Renkli plastik kapağı flakondan çıkarın. Gri lastik tapayı çıkarmayın. Gri kapağın üstünü alkollü bezle temizleyin ve kurumasını bekleyin.
- Blister folyoyu çıkarın ve SmartSite® flakon erişim cihazını beyaz luer kapak ile halka arasında tutarak çıkarın. Cihazın ucuna asla dokunmayın.
- SmartSite® cihazının flakona doğru yerleştirilmesi çok önemlidir, aksi takdirde seyreltici flakona aktarılırken sızabilir. Şişeyi sert bir yüzeye yerleştirin. Şişenin tabanını tutun. Uç, flakonun kauçuk tıpasının merkezinde olacak şekilde cihazı flakon üzerinde dikey olarak yönlendirin. Düz yönde aşağı itin
- Şişenin tabanını tutun ve şırınga ile cihazın bağlantı noktasını (mavi daire) alkollü bezle dezenfekte edin ve şırıngayı SmartSite® cihazına takmadan önce kurumasını bekleyin.
- Kullanıma hazır şırınganın 2 parçadan oluşan beyaz renkli bir ucu vardır: beyaz yaka ve düz beyaz kapak. Şırıngayı açmak için beyaz yakayı tutun ve düz beyaz kapağı çıkarın (BEYAZ KAPAĞI ÇEVİRMEYİN VEYA KESMEYİN).Beyaz kapağı iç lastik uçla birlikte çıkarın. Şırınga montaj işleminin tüm adımları için, şırıngayı yalnızca şırınganın ucunda bulunan beyaz yaka kısmından tutun. Beyaz kapaklı bileziği tutmak, beyaz kapaklı bileziğin çıkmasını önlemeye yardımcı olur ve şırınganın iyi bir şekilde bağlanmasını sağlar. montaj sırasında herhangi bir bileşeni zorlamak için. Bağlantıları zorlamak, bileşenlerin şırınga gövdesinden ayrılmasına neden olabilir.
- Şırınganın beyaz yakasını tutarak, şırınganın ucunu cihazın mavi dairesine sokun ve itin ve şırınganın SmartSite® cihazı ile bağlantısını sağlamak için saat yönünde çevirin (aşırı sıkmaktan kaçının). Dönmesini önlemek için bağlantı sırasında flakon erişim cihazının kapağını tutun. Şırıngayı ve SmartSite® cihazını hizalı tutun.
- Çözücü içeren şırınganın tüm içeriğini flakona enjekte edin.
- Homojen bir süspansiyon oluşmasını sağlamak için başparmağınızla pistona en az 10 saniye basarken flakonu kuvvetlice sallayın. Doğru karıştırıldığında, süspansiyon homojen, kalın ve süt renginde görünür. Sıvının içinde mikro küreler görünecek, ancak toz mikro küre kalmayacak.
- Flakonu tamamen çevirin ve süspansiyonun tüm içeriğini flakondan şırıngaya YAVAŞÇA çekin.Flaksiyonun deliklerdeki etiket kısmını çıkarın ve tanımlama için şırıngaya uygulayın.
- Beyaz yakayı tutarak şırıngayı SmartSite® flakon erişim cihazından çıkarın. Şişeyi ve cihazı uygun şekilde atın.
- İğne paketini açın ve kitte bulunanlardan uygun iğneyi seçin.İğneye enjektör bağlantı kısmından DOKUNMAYIN, sadece iğnenin şeffaf kılıfına.GLUTEAL içine enjeksiyon için 20G iğneyi seçin. 2 inç TW (0,9 mm x 50 mm) (ortada sarı renkli en uzun iğne) DELTOID enjeksiyonu için 1 inç UTW 21G iğneyi (0,8 mm x 25 mm) (ortada yeşil renkli daha kısa iğne) seçin.
- Kontaminasyonu önlemek için Needle-Pro'nun turuncu iğne korumasına dokunmamaya dikkat edin.Beyaz yakayı tutarak, turuncu Needle-Pro güvenlik cihazının luer bağlantısını şırıngaya saat yönünde hafif bir çevirerek bağlayın.
- Şırınganın beyaz bileziğini tutarken, iğnenin şeffaf kapağını kavrayın ve iğneyi, iğneye basarak ve saat yönünde çevirerek Needle-Pro güvenlik cihazının turuncu noktasına sıkıca yerleştirin. İğnenin konumlandırılması, bir sonraki adımı atarken iğne ile turuncu Needle-Pro güvenlik cihazı arasında güvenli bir bağlantının sağlanmasına yardımcı olacaktır.
- UYGULAMADAN ÖNCE, RISPERDAL ENJEKSİYONU TEKRAR ŞEKİLLENDİRİLMELİDİR, ÇÜNKÜ SULANDIRILMIŞ ÜRÜN ANLAMDA ÇÖKÜLECEKTİR. ŞIRINGA İÇERİSİNDEKİ MİKRO küreleri şiddetle SALLAYARAK DEVAM ETTİRİN
- Şırınganın beyaz yakasını hala tutarken şeffaf iğne muhafazasını çıkarın. Luer bağlantısı kopabileceğinden muhafazayı DÖNDÜRMEYİN.
- Hava kabarcıklarının üste çıkması için şırıngaya hafifçe vurun. Pistonu dikkatli ve yavaşça ileri doğru hareket ettirerek ve iğneyi dik tutarak şırıngadaki havayı çıkarın. Şırınganın tüm içeriğini hemen hastanın seçtiği kalça veya deltoid içine intramüsküler olarak enjekte edin.Kalça enjeksiyonu kalça bölgesinin üst dış kadranına yapılmalıdır.
İNTRAVENÖZ YOL İLE YÖNETMEYİN.
UYARI: Kirlenmiş bir iğneden kaynaklanan yaralanmayı önlemek için:
- Needle-Pro Güvenlik Cihazını iğneye itmek için boştaki elinizi KULLANMAYIN
- Needle-Pro Güvenlik Cihazını bilerek BIRAKMAYIN
- İğne bükülmüş veya hasarlıysa iğneyi düzeltmeye veya Needle-Pro güvenlik cihazını kancaya ÇALIŞMAYIN
- İğnenin cihazdan çıkmasına neden olabileceğinden, Needle-Pro güvenlik cihazını yanlış KULLANMAYIN
Enjeksiyon tamamlandığında iğneyi yalnızca bir elinizi kullanarak Needle-Pro turuncu güvenlik cihazının içine itin.
Turuncu Needle-Pro'yu düz bir yüzeye hafifçe iterek bu tek elle işlemi gerçekleştirin.TURUNCU İĞNE-PRO GÜVENLİK CİHAZINI İTTİRDİĞİNİZDE İĞNE TUTACAK ŞEKİLDE TUTACAKTIR. Atmadan önce iğnenin turuncu NeedlePro güvenlik cihazında tamamen kilitlendiğinden emin olun.İğneyi uygun şekilde atın. Ayrıca pakette bulunan diğer (kullanılmamış) iğneyi de atın.
Tekrar kullanmayın: tıbbi cihazların düzgün çalışması için belirli malzeme özellikleri gerekir. Bu özellikler yalnızca tek kullanım için doğrulanmıştır.Cihazı sonraki kullanım için yeniden kullanmaya yönelik herhangi bir girişim, cihazın bütünlüğünü olumsuz etkileyebilir veya çalışmasında bozulmaya neden olabilir.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
RISPERDAL TOZ VE ENJEKTE EDİLEN SÜSPANSİYON İÇİN ÇÖZÜCÜ, KASK İÇİ KULLANIM İÇİN UZUN SÜRELİ SERBEST BIRAKILMALI
(bundan böyle RISPERDAL enjekte edilebilir olarak anılacaktır)
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
1 flakon 25 mg, 37.5 mg veya 50 mg risperidon içerir.
1 ml sulandırılmış süspansiyon 12.5 mg, 18.75 mg veya 25 mg risperidon içerir.
Etkisi bilinen yardımcı maddeler: 1 ml sulandırılmış süspansiyon 3 mg sodyum içerir.
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakın.
03.0 FARMASÖTİK FORM
Enjeksiyonluk süspansiyon için uzun süreli salimli toz ve çözücü.
Toz ile şişe.
Beyaz / kirli beyaz serbest akan toz.
Sulandırma için solventli kullanıma hazır şırınga
Berrak ve renksiz sulu çözelti.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
RISPERDAL CONSTA, şu anda oral antipsikotiklerle stabilize olan hastalarda şizofreninin idame tedavisi için endikedir.
04.2 Pozoloji ve uygulama yöntemi
yetişkinler
İlk doz:
Çoğu hasta için önerilen doz, iki haftada bir kas içinden 25 mg'dır.
En az 2 hafta süreyle sabit doz oral risperidon kullanan hastalar için aşağıdaki dönüşüm programı dikkate alınmalıdır. 4 mg veya daha az dozda oral risperidon ile tedavi edilen hastalar 25 mg enjektabl RISPERDAL almalı, daha yüksek oral dozlarla tedavi edilen hastalar için ise 37.5 mg'lık daha yüksek RISPERDAL enjektabl dozu düşünülmelidir.
Oral risperidon almayan hastalarda, kas içi başlangıç dozu seçilirken önceki oral tedavi dozu dikkate alınmalıdır. Önerilen başlangıç dozu, iki haftada bir enjeksiyon için 25 mg RISPERDAL'dir. Kullanılan oral antipsikotiklerin daha yüksek dozlarını alan hastalarda, 37.5 mg'lık en yüksek RISPERDAL ENJEKSİYON dozu düşünülmelidir.
Enjektabl RISPERDAL'in ilk enjeksiyonunu takip eden üç haftalık gecikme evresinde oral risperidon veya önceki antipsikotik ile yeterli kapsama sağlanmalıdır (bkz. bölüm 5.2).
RISPERDAL ENJEKSİYON, ilk RISPERDAL ENJEKSİYONU enjeksiyonunu takiben 3 haftalık gecikme fazı sırasında oral risperidon veya önceki antipsikotik ile yeterli antipsikotik kapsama sağlanmadan şizofreninin akut alevlenmelerinde kullanılmamalıdır.
Bakım dozu:
Çoğu hasta için önerilen doz, iki haftada bir kas içinden 25 mg'dır. Bazı hastalar 37.5 ve 50 mg'lık daha yüksek dozlardan fayda görebilir. Bir dozdan daha yüksek bir doza geçiş, en az 4 hafta geçmeden yapılamaz. Bu doz ayarlamasının etkisi, daha yüksek doz ile ilk enjeksiyondan 3 hafta sonra önceden tahmin edilemez.Klinik çalışmalarda 75 mg doz ile ek bir fayda görülmemiştir.İki haftada bir 50 mg'ın üzerindeki dozlar gözlenmez. .
Yaşlılar
Doz ayarlaması gerekli değildir. Önerilen doz, iki haftada bir intramüsküler olarak 25 mg'dır. Oral risperidon almayan hastalar için önerilen doz, iki haftada bir enjeksiyon için 25 mg RISPERDAL'dir. En az 2 hafta süreyle sabit doz oral risperidon kullanan hastalar için aşağıdaki dönüşüm programı dikkate alınmalıdır. 4 mg veya daha az dozda oral risperidon ile tedavi edilen hastalar 25 mg enjektabl RISPERDAL almalı, daha yüksek oral dozlarla tedavi edilen hastalar için ise 37.5 mg'lık daha yüksek RISPERDAL enjektabl dozu düşünülmelidir.
İlk RISPERDAL enjeksiyon enjeksiyonunu takiben üç haftalık gecikme evresi boyunca yeterli antipsikotik kapsamı sağlanmalıdır (bkz. bölüm 5.2). Yaşlılarda RISPERDAL ENJEKSİYONU için klinik veriler sınırlıdır.RISPERDAL ENJEKSİYON yaşlılarda dikkatli kullanılmalıdır.
Karaciğer ve böbrek yetmezliği
RISPERDAL CONSTA, karaciğer ve böbrek fonksiyon bozukluğu olan hastalarda çalışılmamıştır.
Karaciğer veya böbrek yetmezliği olan hastalarda enjektabl RISPERDAL tedavisi gerekiyorsa, ilk hafta boyunca günde iki kez 0,5 mg oral risperidon başlangıç dozu önerilir. İkinci hafta günde iki kez 1 mg veya günde bir kez 2 mg verilebilir.En az 2 mg'lık toplam günlük oral doz iyi tolere edilirse, enjeksiyon için 25 mg RISPERDAL 2 haftada bir enjeksiyon yoluyla verilebilir.
İlk RISPERDAL enjeksiyon enjeksiyonunu takiben üç haftalık gecikme evresi boyunca yeterli antipsikotik kapsamı sağlanmalıdır (bkz. bölüm 5.2).
Pediyatrik hastalar
18 yaşın altındaki çocuklarda Risperdal Consta'nın güvenliliği ve etkililiği belirlenmemiştir.Veri mevcut değildir.
Uygulama yöntemi
RISPERDAL ENJEKSİYON, uygun güvenlik iğnesi kullanılarak deltoid veya kalçaya derin kas içi enjeksiyon yoluyla iki haftada bir uygulanmalıdır.Deltoid içine uygulama için, iki kol arasında dönüşümlü olarak 2.5 cm'lik iğne kullanın. Kalçaya uygulama için 5 cm'lik iğneyi iki kalça arasındaki enjeksiyonları değiştirerek kullanın.İntravenöz uygulamayın (bkz. bölüm 4.4 ve bölüm 6.6).
Uygulamadan önce tıbbi ürünün sulandırılmasıyla ilgili talimatlar için bölüm 6.6'ya bakınız.
04.3 Kontrendikasyonlar
Etkin maddeye veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
04.4 Özel uyarılar ve uygun kullanım önlemleri
Hiç risperidon almamış hastalar için, RISPERDAL enjektabl tedavisine başlamadan önce oral risperidon toleransının belirlenmesi önerilir (bkz. bölüm 4.2).
Demanslı yaşlı hastalar
RISPERDAL CONSTA, demansı olan yaşlı hastalarda çalışılmamıştır ve bu nedenle bu hasta grubunda kullanım için endike değildir.RISPERDAL CONSTA, demans ile ilişkili davranış bozukluklarının tedavisi için yetkilendirilmemiştir.
Demanslı Yaşlı Hastalarda Artan Mortalite
RISPERDAL dahil olmak üzere atipik antipsikotiklerle ilgili 17 kontrollü klinik çalışmanın meta-analizinde, atipik antipsikotiklerle tedavi edilen demansı olan yaşlı hastalarda plaseboya kıyasla mortalitede artış olmuştur. Bu popülasyonda oral RISPERDAL ile yapılan plasebo kontrollü klinik çalışmalarda, mortalite insidansı RISPERDAL ile tedavi edilen hastalarda %4,0 iken, plasebo alan hastalarda %3,1'dir. %95 kesin güven) 1,21 (0,7 - 2,1) idi. ortalama yaş (Aralık) ölen hastaların 86 yıl (Aralık 67-100).) İki büyük gözlemsel çalışmadan elde edilen veriler ayrıca, konvansiyonel antipsikotiklerle tedavi edilen demansı olan yaşlı hastalarda bile, tedavi edilmeyen hastalara kıyasla ölüm riskinin biraz arttığını göstermiştir. Riskin kesin büyüklüğünü gerçekten tahmin etmek için yeterli veri yoktur ve artan riskin nedeni bilinmemektedir.Gözlemsel çalışmalarda bulunan mortalite artışının bazılarından ziyade antipsikotik ilaçlara ne ölçüde atfedilebileceği açık değildir. hastalar.
Furosemidin eşzamanlı kullanımı
Demansı olan yaşlı hastalarda gerçekleştirilen oral RISPERDAL'in plasebo kontrollü klinik çalışmalarında, furosemid ile tedavi edilen hastalarda daha yüksek mortalite insidansı gözlenmiştir.
tek başına risperidon (%3.1; ortalama yaş 84, aralık 70-96) veya tek başına furosemid (%4.1; ortalama yaş 80, aralık) ile tedavi edilen hastalara kıyasla risperidon (%7.3; ortalama yaş 89, aralık 75-97) 67-90). Furosemid ve risperidon ile tedavi edilen hastalarda mortalite artışı, dört klinik çalışmanın ikisinde gözlenmiştir.Risperidonun diğer diüretiklerle (çoğunlukla düşük dozlarda kullanılan tiyazid diüretikleri) eşzamanlı kullanımı benzer gözlemlerle ilişkilendirilmemiştir.
Bu gözlemi açıklayacak hiçbir patofizyolojik mekanizma tanımlanmamıştır ve ölüm nedenleri için uyumlu bir model gözlemlenmemiştir. Bununla birlikte, kullanmaya karar vermeden önce dikkatli olunmalı ve bu kombinasyonun veya diğer güçlü diüretiklerle kombinasyonların riskleri ve faydaları göz önünde bulundurulmalıdır. Risperidon ile birlikte başka diüretikler alan hastalarda mortalite insidansında artış gözlenmemiştir.Tedaviden bağımsız olarak, dehidratasyon mortalite için genel bir risk faktörüdür ve bu nedenle demansı olan yaşlı hastalarda dikkatli bir şekilde kaçınılmalıdır.
Serebrovasküler Advers Olaylar (EACV)
Bazı atipik antipsikotiklerle tedavi edilen demans hastalarında yapılan randomize plasebo kontrollü klinik çalışmalarda serebrovasküler advers olay riskinde yaklaşık 3 kat artış gözlenmiştir. RISPERDAL ile öncelikle demanslı yaşlılarda (> 65 yaş) yürütülen altı plasebo kontrollü klinik çalışmanın havuzlanmış verileri, ACV'lerin (şiddetli ve ciddi olmayan, ilişkili) risperidon ile tedavi edilen hastaların %3.3'ünde (33/1009) meydana geldiğini göstermiştir. plasebo ile tedavi edilenlerin %1,2'sinde (8/712) Odds oranı (%95 kesin güven aralığı) 2,96 (1,34-7,50) idi. Bu artan riskin mekanizması bilinmemektedir. Diğer antipsikotikler veya diğer hasta popülasyonları için artan bir risk göz ardı edilemez. RISPERDAL CONSTA, inme risk faktörleri olan hastalarda dikkatli kullanılmalıdır.
Ortostatik hipotansiyon
Risperidonun alfa bloke edici aktivitesi ile ilgili olarak, özellikle tedavinin ilk aşamasında (ortostatik) hipotansiyon meydana gelebilir.Risperidon ve antihipertansif tedavinin birlikte kullanımı ile pazarlama sonrası aşamada klinik olarak anlamlı hipotansiyon gözlenmiştir. RISPERDAL, bilinen kardiyovasküler hastalığı (örn. kalp yetmezliği, miyokard enfarktüsü, iletim bozuklukları, dehidratasyon, hipovolemi veya serebrovasküler hastalık) olan hastalarda dikkatle uygulanmalıdır. Klinik olarak ilgili "ortostatik hipotansiyon"un devam etmesi durumunda, enjektabl RISPERDAL ile tedaviye devam etmenin uygunluğu yarar/risk oranı temelinde değerlendirilmelidir.
Lökopeni, nötropeni ve agranülositoz
Enjektabl RISPERDAL dahil olmak üzere antipsikotik ajanların kullanımı ile lökopeni, nötropeni ve agranülositoz olayları bildirilmiştir. Tedavinin ilk aylarında izlenir ve diğer nedensel faktörlerin yokluğunda klinik olarak anlamlı WBC azalmasının ilk belirtisinde enjekte edilebilir RISPERDAL enjektabl tedavisinin kesilmesi Klinik olarak anlamlı nötropenisi olan hastalar ateş veya diğer semptomlar veya enfeksiyon belirtileri açısından yakından izlenmeli ve derhal tedavi edilmelidir. Bu tür semptom veya belirtiler ortaya çıkarsa Şiddetli nötropenisi olan hastalar (mutlak nötrofil sayısı)
Tardif diskinezi / Ekstrapiramidal semptomlar (DT / EPS)
Dopamin reseptör antagonizması özelliklerine sahip tıbbi ürünler, ağırlıklı olarak dil ve/veya yüzde ritmik istemsiz hareketlerle karakterize olan geç diskinezinin indüklenmesiyle ilişkilendirilmiştir. Ekstrapiramidal semptomların başlaması, geç diskinezi için bir risk faktörüdür.Tardif diskinezi belirti ve semptomları ortaya çıkarsa, herhangi bir antipsikotik tedavinin kesilmesi olasılığı düşünülmelidir.
Nöroleptik malign sendrom (NMS)
Antipsikotik ilaçların uygulanmasıyla hipertermi, kas sertliği, otonom sinir sistemi kararsızlığı, bilinç değişikliği durumu ve yüksek serum kreatinofosfokinaz seviyeleri ile karakterize olan Nöroleptik Malign Sendrom bildirilmiştir.Ek belirtiler arasında miyoglobinüri (rabdomiyoliz) ve akut böbrek yetmezliği yer alabilir. Bu durumda, enjektabl RISPERDAL dahil tüm antipsikotikler kesilmelidir.
Parkinson hastalığı ve Lewy cisimli demans
Enjektabl RISPERDAL dahil antipsikotik ilaçları Parkinson hastalığı veya Lewy cisimcikli demansı (DLB) olan hastalara reçete etmeden önce, doktorlar fayda/risk oranını değerlendirmelidir. Parkinson hastalığı risperidon ile daha da kötüleşebilir. Her iki hasta grubu da Nöroleptik Malign Sendrom açısından yüksek risk altında olabileceği gibi antipsikotik ilaçlara daha duyarlı olabilir; bu hastalar klinik çalışmalardan çıkarıldı. Bu duyarlılıktaki artış, kafa karışıklığı, sedasyon, sık düşmelerle birlikte postural instabilite ve ekstrapiramidal semptomlarla kendini gösterebilir.
Hiperglisemi ve diabetes mellitus
Enjektabl RISPERDAL tedavisi sırasında hiperglisemi, diabetes mellitus ve önceden var olan diyabetin alevlenmesi bildirilmiştir.
Bazı durumlarda, predispozan bir faktör olabilecek daha önce kilo alımı bildirilmiştir. Ketoasidoz ile ilişki çok nadiren ve nadiren diyabetik koma ile bildirilmiştir.Antipsikotik kullanımı ile kılavuzlara göre yeterli klinik izleme önerilir. Enjektabl RISPERDAL dahil olmak üzere herhangi bir atipik antipsikotik ile tedavi edilen hastalar, hiperglisemi semptomları (polidipsi, poliüri, polifaji ve halsizlik gibi) açısından izlenmeli ve diabetes mellituslu hastalar kötüleşen glukoz kontrolü için düzenli olarak izlenmelidir.
Kilo almak.
RISPERDAL ENJEKSİYON kullanımı ile önemli kilo artışı bildirilmiştir.Ağırlık düzenli olarak izlenmelidir.
hiperprolaktinemi
Doku kültürü çalışmaları, insan meme kanserlerinde hücre büyümesinin prolaktin tarafından uyarılabileceğini düşündürmektedir.
Bugüne kadar klinik ve epidemiyolojik çalışmalarda antipsikotiklerin uygulanması ile açık bir ilişki gösterilmemiş olsa da, ilgili klinik öyküsü olan hastalarda dikkatli olunması önerilir. RISPERDAL CONSTA, önceden hiperprolaktinemisi olan hastalarda ve potansiyel olarak prolaktine bağımlı tümörü olan hastalarda dikkatli kullanılmalıdır.
QT aralığının uzaması
Pazarlama sonrası ortamda QT aralığı uzaması çok nadiren bildirilmiştir.Diğer antipsikotiklerde olduğu gibi, bilinen kardiyovasküler hastalığı, ailede QT aralığı uzaması öyküsü, bradikardi veya elektrolit dengesizlikleri (hipokalemi, hipomagnezemi) olan hastalara risperidon reçete edilirken dikkatli olunmalıdır. aritmojenik etki riskini ve QT uzamasına neden olduğu bilinen tıbbi ürünlerin birlikte kullanımı riskini artırabilir.
konvülsiyonlar
RISPERDAL CONSTA, nöbet öyküsü veya nöbet eşiğini düşürebilecek diğer durumları olan hastalarda dikkatli kullanılmalıdır.
priapizm
Alfa-adrenerjik reseptör bloke edici aktivitesi nedeniyle RISPERDAL CONSTA ile priapizm oluşabilir.
Vücut termoregülasyonu
Antipsikotik tıbbi ürünlerin vücudun çekirdek vücut ısısını düşürme kabiliyetini bozduğu rapor edilmiştir.Isı artışına katkıda bulunabilecek durumlarla karşılaşabilecek hastalara RISPERDAL ENJEKSİYON reçete edilirken dikkatli olunması önerilir.İç vücut, örneğin yoğun fiziksel aktivite, maruz kalma aşırı sıcağa, antikolinerjik aktiviteye sahip ilaçların birlikte uygulanmasına veya dehidrasyona yatkınlığa.
Venöz tromboembolizm
Antipsikotik ilaçlarla venöz tromboembolizm (VTE) vakaları bildirilmiştir. Antipsikotiklerle tedavi edilen hastalar sıklıkla VTE için edinilmiş risk faktörlerine sahiptir; bu nedenle VTE için tüm olası risk faktörleri, RISPERDAL enjektabl ile tedaviden önce ve tedavi sırasında tanımlanmalı ve önleyici tedbirler alınmalıdır.
İntraoperatif Disket İris Sendromu
Enjektabl RISPERDAL dahil olmak üzere alfa1a-adrenerjik antagonist etkisi olan tıbbi ürünlerle tedavi edilen hastalarda katarakt cerrahisi sırasında intraoperatif Floppy İris Sendromu (IFIS) gözlenmiştir (bkz. bölüm 4.8).
IFIS, operasyon sırasında ve sonrasında oküler komplikasyon riskini artırabilir. Alfa1a-adrenerjik antagonist etkisi olan tıbbi ürünlerin mevcut veya geçmişteki kullanımı ameliyattan önce oftalmik cerraha bildirilmelidir. Katarakt cerrahisinden önce alfa1 bloker tedavisinin kesilmesinin potansiyel faydası belirlenmemiştir ve antipsikotik tedaviyi bırakma riskine karşı tartılmalıdır.
antiemetik etki
Risperidon ile yapılan klinik öncesi çalışmalarda antiemetik bir etki gözlenmiştir. Bu etki, insanlarda ortaya çıkarsa, belirli ilaçların aşırı dozunun veya bağırsak tıkanıklığı, Reye sendromu ve beyin tümörü gibi durumların belirti ve semptomlarını maskeleyebilir.
Böbrek veya karaciğer yetmezliği
Oral risperidon çalışılmış olmasına rağmen, RISPERDAL CONSTA böbrek veya karaciğer yetmezliği olan hastalarda çalışılmamıştır. RISPERDAL ENJEKSİYON bu hasta grubunda dikkatle uygulanmalıdır (bkz. bölüm 4.2).
Yönetim
RISPERDAL INJECTION'ı yanlışlıkla bir kan damarına enjekte etmekten kaçınmak için çok dikkatli olun.
Yardımcı maddeler
Bu tıbbi ürün, doz başına 1 mmol'den (23 mg) daha az sodyum içerdiğinden, esasen sodyum içermez.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Enjektabl RISPERDAL'in eşzamanlı uygulanan diğer tıbbi ürünlerle etkileşimleri sistematik olarak değerlendirilmemiştir. Bu bölümde sağlanan ilaç etkileşim verileri, oral RISPERDAL ile yürütülen çalışmalara dayanmaktadır.
farmakodinamik etkileşimler
QT aralığının uzamasına neden olduğu bilinen ilaçlar
Diğer antipsikotiklerde olduğu gibi, risperidon, antiaritmikler (örn., kinidin, disopiramid, prokainamid, propafenon, amiodaron, sotalol), trisiklik antidepresanlar (örn., amitriptilin) gibi QT aralığının uzamasına neden olduğu bilinen ilaçlarla kombinasyon halinde reçete edilirken dikkatli olunması önerilir. tetrasiklik antidepresanlar (örneğin maprotilin), bazı antihistaminikler, diğer antipsikotikler, bazı antimalaryaller (örneğin kinin ve meflokin) ve elektrolit dengesizliklerine (hipokalemi, hipomagnezemi), bradikardi veya risperidon karaciğer metabolizmasını inhibe eden ilaçlarla birlikte. gösterge niteliğinde ve kapsamlı olmayan bir listedir.
Merkezi etkili uyuşturucu ve alkol
Risperidon, artan sedasyon riskinden dolayı özellikle alkol, opiatlar, antihistaminikler ve benzodiazepinler dahil olmak üzere diğer merkezi etkili maddelerle kombinasyon halinde dikkatli kullanılmalıdır.
Levodopa ve dopamin agonistleri
RISPERDAL CONSTA, levodopa ve diğer dopamin agonistlerinin etkisini antagonize edebilir.Bu kombinasyon özellikle Parkinson hastalığının son aşamasında gerekli görülürse, her tedavinin en düşük etkili dozu reçete edilmelidir.
Hipotansif etkisi olan ilaçlar
Risperidon ve antihipertansif tedavinin birlikte kullanımı ile pazarlama sonrası klinik olarak anlamlı hipotansiyon gözlenmiştir.
farmakokinetik etkileşimler
Risperidon esas olarak CYP2D6 yoluyla ve daha az ölçüde CYP3A4 yoluyla metabolize edilir. Hem risperidon hem de aktif metaboliti 9-hidroksirisperidon, P-glikoproteinin (P-gp) substratlarıdır. CYP2D6 aktivitesini değiştiren veya CYP3A4 ve/veya P-gp aktivitesinin güçlü inhibitörleri veya indükleyicileri olan maddeler, risperidonun aktif antipsikotik fraksiyonunun farmakokinetiğini etkileyebilir.
Güçlü CYP2D6 inhibitörleri
Enjeksiyonluk RISPERDAL'in güçlü bir CYP2D6 inhibitörü ile birlikte uygulanması, risperidonun plazma konsantrasyonlarını artırabilir, ancak bu, aktif antipsikotik fraksiyonunkileri daha az ölçüde artırabilir. Güçlü bir CYP2D6 inhibitörünün yüksek dozları, risperidonun aktif antipsikotik fraksiyonunun (örn. paroksetin, aşağıya bakınız) konsantrasyonlarını artırabilir. Kinidin gibi diğer CYP 2D6 inhibitörlerinin, risperidon plazma konsantrasyonlarını benzer şekilde etkilemesi beklenir. Paroksetin, kinidin veya özellikle yüksek dozlarda başka bir güçlü CYP2D6 inhibitörü ile eş zamanlı tedavi başlatıldığında veya sonlandırıldığında, doktor enjektabl RISPERDAL dozunu yeniden değerlendirmelidir.
CYP3A4 ve/veya P-gp inhibitörleri
Enjeksiyonluk RISPERDAL'in güçlü bir CYP3A4 ve/veya P-gp inhibitörü ile birlikte uygulanması, risperidonun aktif antipsikotik fraksiyonunun plazma konsantrasyonlarını önemli ölçüde artırabilir. Eşzamanlı itrakonazol veya başka bir güçlü CYP3A4 ve/veya P-gp inhibitörü başlatıldığında veya kesildiğinde, doktor RISPERDAL enjeksiyon dozunu yeniden değerlendirmelidir.
CYP3A4 ve/veya P-gp indükleyicileri
Enjeksiyonluk RISPERDAL'in güçlü bir CYP3A4 ve/veya P-gp indükleyicisi ile birlikte uygulanması, risperidon aktif antipsikotik fraksiyonunun plazma konsantrasyonlarını azaltabilir. Karbamazepin veya başka bir güçlü CYP3A4 ve/veya P-gp indükleyicisi ile eş zamanlı tedavi başlatıldığında veya kesildiğinde, doktor RISPERDAL enjeksiyonunun dozunu yeniden değerlendirmelidir. CYP3A4 indükleyicileri etkilerini zamana bağlı bir şekilde gösterirler ve uygulanmalarından sonra maksimum etkiye ulaşmaları en az 2 hafta sürebilir Tersine, CYP3A4 indüksiyonunun azalması en az 2 hafta sürebilir.
Plazma proteinlerine yüksek oranda bağlanan tıbbi ürünler
RISPERDAL CONSTA, plazma proteinlerine yüksek oranda bağlanan tıbbi ürünlerle birlikte alındığında, her iki tıbbi üründe de plazma proteinlerinden klinik olarak anlamlı bir kayma meydana gelmez.
Eşzamanlı tıbbi ürünler uygulanırken, metabolizma hakkında bilgi ve olası doz ayarlaması ihtiyacı ile ilgili olarak Kısa Ürün Bilgisine danışılmalıdır.
Pediatrik popülasyon
Etkileşim çalışmaları sadece yetişkinlerde yapılmıştır. Pediyatrik hastalarda bu çalışmaların sonuçlarının önemi bilinmemektedir.
Örnekler
Risperidon ile potansiyel olarak etkileşime girebilecek veya etkileşmediği gösterilmiş olan ilaç örnekleri aşağıda listelenmiştir.
Diğer tıbbi ürünlerin risperidon farmakokinetiği üzerindeki etkisi
Antibakteriyeller:
• Orta derecede bir CYP3A4 inhibitörü ve bir P-gp inhibitörü olan eritromisin, risperidon ve aktif antipsikotik fraksiyonun farmakokinetiğini değiştirmez.
• Güçlü bir CYP3A4 indükleyicisi ve bir P-gp indükleyicisi olan rifampisin, aktif antipsikotik fraksiyonun plazma konsantrasyonlarını azaltmıştır.
Antikolinesterazlar:
Hem CYP2D6 hem de CYP3A4 substratları olan donepezil ve galantamin, risperidon ve aktif antipsikotik fraksiyonun farmakokinetiği üzerinde klinik olarak anlamlı bir etki göstermez.
Antiepileptikler:
• Güçlü bir CYP3A4 indükleyicisi ve bir P-gp indükleyicisi olan karbamazepinin, risperidonun aktif antipsikotik fraksiyonunun plazma konsantrasyonlarını azalttığı gösterilmiştir. Benzer etkiler, örneğin, aynı zamanda hepatik enzim CYP 3A4'ün indükleyicileri olan fenitoin ve fenobarbitalin yanı sıra P-glikoprotein (P-gp) ile de görülebilir.Doktor, RISPERDAL enjeksiyonunun dozunu başlatırken veya durdururken yeniden değerlendirmelidir. karbamazepin veya diğer hepatik CYP 3A4 / P-glikoprotein enzim indükleyicileri ile tedavi.
• Topiramat, risperidonun biyoyararlanımını orta derecede azalttı, ancak aktif antipsikotik fraksiyonun biyoyararlanımını azaltmadı. Bu nedenle, bu etkileşimin klinik öneme sahip olması olası değildir.
Antifungaller:
• Güçlü bir CYP3A4 inhibitörü ve bir P-gp inhibitörü olan itrakonazol, 200 mg/gün dozunda, 2-8 mg/gün risperidon dozları ile aktif antipsikotik fraksiyonun plazma konsantrasyonlarını yaklaşık %70 artırmıştır.
• Güçlü bir CYP3A4 inhibitörü ve P-gp inhibitörü olan ketokonazol, 200 mg/gün dozunda risperidon plazma konsantrasyonlarını artırdı ve 9-hidroksirisperidon plazma konsantrasyonlarını azalttı.
Antipsikotikler:
• Fenotiyazinler, risperidonun plazma konsantrasyonlarını artırabilir, ancak aktif antipsikotik fraksiyonunkileri değil.
Antiviraller:
• Proteaz inhibitörleri: resmi çalışmalardan elde edilen veriler mevcut değildir; bununla birlikte, ritonavir güçlü bir CYP3A4 inhibitörü ve zayıf bir CYP2D6 inhibitörü olduğundan, ritonavir ve ritonavir destekli proteaz inhibitörleri, risperidonun aktif antipsikotik fraksiyonunun konsantrasyonlarını potansiyel olarak artırır.
Beta blokerler:
• Bazı beta blokerler, aktif antipsikotik fraksiyonun değil, risperidonun plazma konsantrasyonlarını artırabilir.
Kalsiyum kanal blokerleri:
• Orta derecede bir CYP3A4 inhibitörü ve bir P-gp inhibitörü olan Verapamil, risperidon ve aktif antipsikotik fraksiyonun plazma konsantrasyonunu arttırır.
Gastrointestinal ilaçlar:
• H2 reseptör antagonistleri: Her ikisi de CYP2D6 ve CYP3A4'ün zayıf inhibitörleri olan simetidin ve ranitidin, risperidonun biyoyararlanımını artırdı, ancak aktif antipsikotik fraksiyonun biyoyararlanımını çok az artırdı.
SSRI'lar ve trisiklik antidepresanlar:
• Güçlü bir CYP2D6 inhibitörü olan fluoksetin, risperidonun plazma konsantrasyonunu artırır, ancak aktif antipsikotik fraksiyonunkinden daha az oranda.
• Güçlü bir CYP2D6 inhibitörü olan paroksetin, risperidonun plazma konsantrasyonunu arttırır, ancak günde 20 mg'a kadar olan dozlarda, aktif antipsikotik fraksiyonunkinden daha düşüktür. Bununla birlikte, daha yüksek dozlarda paroksetin, risperidonun aktif antipsikotik fraksiyonunun konsantrasyonlarını artırabilir.
• Trisiklik antidepresanlar, aktif antipsikotik fraksiyonun değil, risperidonun plazma konsantrasyonlarını artırabilir. Amitriptilin, risperidon veya aktif antipsikotik fraksiyonun farmakokinetiğini etkilemez.
• 100 mg/gün'e kadar olan dozlarda zayıf bir CYP2D6 inhibitörü olan sertralin ve zayıf bir CYP3A4 inhibitörü olan fluvoksamin, risperidon aktif antipsikotik fraksiyonunun konsantrasyonlarında klinik olarak anlamlı değişikliklerle ilişkili değildir. Bununla birlikte, 100 mg/gün üzerindeki sertralin veya fluvoksamin dozları, risperidon aktif antipsikotik fraksiyonunun konsantrasyonlarını artırabilir.
Risperidonun diğer tıbbi ürünlerin farmakokinetiği üzerindeki etkisi
Antiepileptikler:
• Risperidon, valproat ve topiramatın farmakokinetiği üzerinde klinik olarak anlamlı bir etki göstermez.
Antipsikotikler:
• Aripiprazol, bir CYP2D6 ve CYP3A4 substratı: Oral veya enjekte edilebilir risperidon, aripiprazol ve aktif metaboliti dehidroaripiprazol toplamının farmakokinetiğini etkilememiştir.
Dijital glikozitler:
• Risperidon digoksinin farmakokinetiği üzerinde klinik olarak anlamlı bir etki göstermez.
Lityum:
• Risperidon, lityum farmakokinetiği üzerinde klinik olarak anlamlı bir etki göstermez.
Risperidon ve furosemidin birlikte kullanımı
Furosemid ile kombinasyon halinde tedavi edilen demansı olan yaşlı hastalarda artan mortalite ile ilgili olarak bölüm 4.4'e bakınız.
04.6 Hamilelik ve emzirme
Gebelik
Risperidon'un hamile kadınlarda kullanımına ilişkin veriler yetersizdir Risperidon hayvanlar üzerinde yapılan çalışmalarda teratojenik etkiler göstermemiştir, ancak diğer üreme toksisitesi türleri bulunmuştur (bkz. Bölüm 5.3) İnsanlar için potansiyel risk bilinmemektedir.
Hamileliğin üçüncü trimesterinde enjektabl RISPERDAL dahil antipsikotiklere maruz kalan bebekler, doğumdan sonra şiddeti ve süresi değişebilen ekstrapiramidal ve/veya yoksunluk semptomları dahil advers reaksiyon riski altındadır. Ajitasyon, hipertoni, hipotoni, tremor, somnolans, solunum sıkıntısı veya beslenme bozuklukları vakaları bildirilmiştir. Bu nedenle, yenidoğanlar dikkatle izlenmelidir. RISPERDAL ENJEKSİYON kesinlikle gerekli olmadıkça hamilelik sırasında kullanılmamalıdır.
Besleme zamanı
Hayvan çalışmalarında, risperidon ve 9-hidroksi-risperidon sütle atılır. Risperidon ve 9-hidroksi-risperidon'un da küçük miktarlarda anne sütüne geçtiği gösterilmiştir. Emzirilen bebeklerde advers reaksiyonlar hakkında veri bulunmamaktadır. Bu nedenle, emzirmenin yararı bebeğe yönelik potansiyel riske karşı tartılmalıdır.
Doğurganlık
Dopamin D2 reseptörünü antagonize eden diğer ilaçlarda olduğu gibi, RISPERDAL prolaktin düzeylerini artırır. Hiperprolaktinemi hipotalamik GnRH'yi baskılayarak hipofiz gonadotropin salgısının azalmasına neden olabilir Bu da hem kadın hem de erkek hastalarda gonadal steroidogenezden ödün vererek üreme fonksiyonunu inhibe edebilir.
Klinik olmayan çalışmalar sırasında ilgili herhangi bir etki gözlenmedi.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
RISPERDAL ENJEKSİYON, sinir sistemi ve görme üzerindeki potansiyel etkileri nedeniyle araç ve makine kullanma becerisini hafif veya orta düzeyde etkiler (bkz. bölüm 4.8). Bu nedenle hastalara, bireysel duyarlılıkları bilinene kadar araç veya makine kullanmamaları tavsiye edilmelidir.
04.8 İstenmeyen etkiler
En sık bildirilen advers ilaç reaksiyonları (ADR'ler) (insidans ≥1/10) şunlardır: Uykusuzluk, anksiyete, baş ağrısı, üst solunum yolu enfeksiyonu, parkinsonizm ve depresyon.
Dozla ilişkili gibi görünen ADR'ler arasında parkinsonizm ve akatizi yer alır.
Pazarlama sonrası, enjeksiyon bölgesi nekrozu, apse, selülit, ülser, hematom, kistler ve nodüller dahil olmak üzere şiddetli enjeksiyon bölgesi reaksiyonları bildirilmiştir. Sıklık bilinmiyor olarak kabul edilir (mevcut verilerden tahmin edilemez). İzole vakalar ameliyat gerektiriyordu.
Aşağıdaki ADR'ler, RISPERDAL enjekte edilebilir klinik çalışmalardan tahmin edilen sıklık kategorisine göre klinik çalışmalarda ve pazarlama sonrası deneyimlerde rapor edilenlerin tamamıdır. Aşağıdaki terimler ve ilgili sıklıklar geçerlidir: çok yaygın (≥1/10), yaygın (≥1/10), yaygın ( ≥1 / 10) 1/100 bir
Her bir sıklık sınıfı içinde, istenmeyen etkiler azalan önem sırasına göre rapor edilir.
a L "hiperprolaktinemi bazı durumlarda jinekomasti, menstrüel rahatsızlıklar, amenore, galaktoreye neden olabilir.
b Plasebo kontrollü klinik çalışmalarda plasebo grubundaki %0.11'e kıyasla risperidon ile tedavi edilen deneklerin %0.18'inde diabetes mellitus rapor edilmiştir. Tüm klinik çalışmaların genel insidansı, risperidon ile tedavi edilen tüm deneklerde %0.43'tür.
c RISPERDAL enjektabl klinik çalışmalarında gözlemlenmemiştir, ancak risperidon ile pazarlama sonrası deneyimlerde gözlemlenmiştir.
d Ekstrapiramidal bozukluklar oluşabilir: Parkinsonizm (tükürük hipersekresyonu, kas-iskelet sertliği, parkinsonizm, tükürük kaybıyla birlikte pitalizm, sarsıntılı sertlik, bradikinezi, hipokinezi, maske fasiyesi, kas gerginliği, akinezi, ense sertliği, kas sertliği, parkinson yürüyüşü ve glabellar refleks anormal, parkinson istirahatte titreme), akatizi (akatizi, huzursuzluk, hiperkinezi ve huzursuz bacak sendromu), tremor, diskinezi (diskinezi, kas seğirmesi, koreoatetoz, atetoz ve miyokloni), distoni. Distoni, distoni, hipertoni, tortikolis, istemsiz kas kasılmaları, kas kontraktürü, blefarospazm, okülogyrus, dil felci, yüz spazmı, laringospazm, miyotoni, opisthotonus, orofaringeal spazm, pleurotonus, lingual spazm ve trimusdur. Ekstrapiramidal kökenli olması gerekmeyen, daha geniş bir semptom yelpazesinin dahil edildiğini belirtmek önemlidir. Uykusuzluk şunları içerir: ilk uykusuzluk, merkezi uykusuzluk; nöbetler şunları içerir: büyük mal nöbetleri; adet bozuklukları şunları içerir: düzensiz adet kanaması, oligomenore; ödem şunları içerir: genel ödem, periferik ödem, plastik ödem.
Paliperidon formülasyonları ile bildirilen istenmeyen etkiler
Paliperidon, risperidonun aktif metabolitidir, bu nedenle bu bileşiklerin (hem oral hem de enjekte edilebilir formülasyonlar dahil) olumsuz rasyon profilleri birbiriyle ilişkilidir. Yukarıda bahsedilen advers reaksiyonlara ek olarak, paliperidon ürünlerinin kullanımı ile aşağıdaki advers reaksiyonlar rapor edilmiştir ve RISPERDAL enjekte edilebilir ile beklenebilir.
Kardiyak bozukluklar: postural ortostatik taşikardi sendromu.
Anafilaktik tepki
Daha önce oral risperidonu tolere etmiş hastalarda, pazarlama sonrası deneyimde, Risperdal Consta enjeksiyonundan sonra anafilaktik reaksiyon vakaları nadiren bildirilmiştir.
sınıf efektleri
Diğer antipsikotikler gibi risperidon ile pazarlama sonrası çok nadir QT aralığı uzaması vakaları bildirilmiştir QT aralığını uzatan antipsikotiklerle bildirilen diğer kardiyak sınıf etkileri arasında ventriküler aritmi, ventriküler fibrilasyon, ventriküler taşikardi , ani ölüm, kardiyak arrest ve torsades de pointes bulunur.
Venöz tromboembolizm
Antipsikotik ilaçlarla pulmoner emboli vakaları ve derin ven trombozu vakaları dahil venöz tromboembolizm vakaları bildirilmiştir (sıklığı bilinmemektedir).
Kilo almak
12 haftalık, çift kör, plasebo kontrollü bir klinik çalışmada, RISPERDAL CONSTA ile tedavi edilen hastaların %9'u her zaman gözlenmiştir."uç nokta plasebo ile tedavi edilen hastalardaki %6 ile karşılaştırıldığında ≥ %7 kilo artışı.
Enjektabl RISPERDAL'in açık etiketli 1 yıllık bir klinik çalışmasında, bireysel hastalarda vücut ağırlığı değişiklikleri genellikle başlangıç değerinin ± %7'si dahilindeydi; Hastaların %25'inde ≥%7 kilo artışı vardı.
Şüpheli advers reaksiyonların raporlanması
İlacın ruhsatlandırılmasından sonra meydana gelen şüpheli advers reaksiyonların raporlanması, tıbbi ürünün fayda/risk dengesinin sürekli olarak izlenmesine imkan verdiği için önemlidir. Sağlık profesyonellerinden şüpheli advers reaksiyonları ulusal raporlama sistemi aracılığıyla bildirmeleri istenmektedir. www.aifa.gov.it/responsabili.
04.9 Doz aşımı
İlacın parenteral uygulaması ile doz aşımı olasılığı, oral yoldan alınan ilaca göre daha düşük olmasına rağmen, oral yolla ilgili bilgiler rapor edilmektedir.
Belirtiler
Genel olarak, bildirilen belirti ve semptomlar, "risperidonun bilinen farmakolojik etkilerinin vurgulanmasından" kaynaklananlardır. Bunlara uyuklama ve sedasyon, taşikardi ve hipotansiyon ve ekstrapiramidal semptomlar dahildir. Doz aşımı durumunda, QT uzaması ve nöbetler bildirilmiştir. Torsades de kombine doz aşımı oral RISPERDAL ve paroksetin ile ilişkili olarak rapor edilmiştir.
Akut doz aşımı durumunda, birden fazla ilacın dahil olma olasılığı göz önünde bulundurulmalıdır.
Tedavi
Açık bir hava yolu oluşturun ve sürdürün ve yeterli oksijenasyon ve ventilasyon sağlayın Kardiyovasküler izleme hemen başlamalı ve olası aritmileri saptamak için sürekli elektrokardiyografik izlemeyi içermelidir.
RISPERDAL'in spesifik bir antidotu yoktur. Bu nedenle uygun genel destekleyici önlemler alınmalıdır. Hipotansiyon ve dolaşım kollapsı IV sıvılar ve/veya sempatomimetik ajanlar gibi uygun önlemlerle tedavi edilmelidir.Ağır ekstrapiramidal semptomlar durumunda antikolinerjik ilaçlar verilmelidir.Hasta iyileşene kadar yakın takip ve klinik gözetime devam edin. .
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
farmakoterapötik grup: diğer antipsikotikler.
ATC kodu: N05AX08.
Hareket mekanizması
Risperidon, benzersiz özelliklere sahip seçici bir monoaminerjik antagonisttir. 5-HT2 serotonerjik reseptörler ve D2 dopaminerjik reseptörler için yüksek bir afiniteye sahiptir Risperidon ayrıca alfa1-adrenerjik reseptörlere ve daha az ölçüde H1-histaminerjik ve alfa2-adrenerjik reseptörlere bağlanır Risperidon, kolinerjik reseptörlere afinitesi yoktur. şizofreninin pozitif semptomlarını iyileştirdiğine inanılan güçlü bir D2 antagonistidir, klasik antipsikotiklere göre motor aktivitede daha az depresyona ve katalepsi indüksiyonuna neden olur. Serotonin ve dopamin arasındaki dengeli merkezi antagonizma, ekstrapiramidal yan etki riskini azaltabilir ve terapötik aktiviteyi şizofreninin negatif ve afektif semptomlarına kadar genişletebilir.
Klinik etkinlik
Psikotik bozuklukların (şizofreni / şizoaffektif bozukluk) belirtilerinin yönetiminde enjektabl RISPERDAL'in (25 mg ve 50 mg) etkinliği, hastanede yatan yetişkin psikotik hastalarda ve DSM ile tanışan ayakta tedavi gören hastalarda yürütülen 12 haftalık, plasebo kontrollü bir klinik çalışmada belirlenmiştir. -IV şizofreni kriterleri.
Stabil şizofreni hastalarında yürütülen 12 haftalık karşılaştırmalı bir klinik çalışmada, RISPERDAL ENJEKSİYON oral tablet formülasyonu kadar etkili olmuştur. Enjektabl RISPERDAL'in uzun vadeli (50 haftalık) etkililiği ve güvenliliği, şizofreni veya bozukluk için DSM-IV kriterlerini karşılayan stabil yatan ve ayakta tedavi gören psikotik hastalarda yürütülen açık etiketli bir klinik çalışmada da değerlendirilmiştir. zaman içindeki etkinliği korunmuştur.
05.2 Farmakokinetik özellikler
absorpsiyon
RISPERDAL enjeksiyonundan risperidon emilimi tamamlanmıştır.
Enjeksiyonluk RISPERDAL'in tek bir intramüsküler enjeksiyonunu takiben, salınım profili küçük bir başlangıç risperidon salınımından oluşur (ek olarak
Bu nedenle, RISPERDAL enjeksiyonu ile tedavinin ilk 3 haftasında oral antipsikotikler verilmelidir (bkz. bölüm 4.2).
Salınım profili ve terapötik rejimin (iki haftada bir kas içi enjeksiyon) ilişkisi, uzun süre terapötik aralıkta tutulan plazma konsantrasyonları ile sonuçlanır. Terapötik plazma konsantrasyonları, son RISPERDAL enjeksiyonundan sonra 4-6 haftaya kadar kalır.
İki haftada bir 25 veya 50 mg RISPERDAL enjeksiyonunun tekrarlanan intramüsküler enjeksiyonlarından sonra, aktif antipsikotik fraksiyonun medyan minimum ve maksimum plazma konsantrasyonları sırasıyla 9.9-19.2 ng/ml ve 17.9-45.5 ng/ml arasında değişmiştir. İki haftada bir 25-50 mg doz enjekte edilen hastalarda uzun süreli (12 ay) kullanım sırasında, risperidon birikimi gözlenmemiştir.
Yukarıdaki çalışmalar kalçaya intramüsküler enjeksiyon ile yapılmıştır. Aynı dozlarda deltoid ve kalçaya intramüsküler enjeksiyonlar biyoeşdeğerdir ve bu nedenle birbirinin yerine kullanılabilir.
Dağıtım
Risperidon hızla dağılır. Dağılım hacmi 1-2 l / kg'dır. Plazmada, risperidon albümin ve alfa1-asit glikoproteine bağlanır Risperidon'un plazma proteinlerine bağlanması %90, aktif metaboliti olan 9-hidroksi-risperidon ise %77'dir.
Biyotransformasyon ve eliminasyon
Risperidon, CYP 2D6'dan, risperidonunkine benzer farmakolojik aktivite ile 9-hidroksi-risperidon'a metabolize edilir. Risperidon ve 9-hidroksi-risperidon, aktif antipsikotik fraksiyonu oluşturur. CYP2D6, genetik polimorfizme tabidir. CYP 2D6'nın yoğun metabolizörleri, risperidonu hızla 9-hidroksi-risperidon'a dönüştürürken, zayıf metabolizörler onu çok daha yavaş dönüştürür. Hızlı metabolize edenlerin, zayıf metabolizörlere göre daha düşük risperidon ve daha yüksek 9-hidroksi-risperidon konsantrasyonları olmasına rağmen, tekli ve çoklu dozlardan sonra risperidon ve 9-hidroksi-risperidon kombine farmakokinetiği (yani aktif antipsikotik fraksiyonu), bunlar geniş ve yavaş dozlarda benzerdir. CYP 2D6 metabolizörleri.
Risperidonun başka bir metabolik yolu, N-dealkilasyondur. İnsan karaciğer mikrozomlarında yapılan in vitro çalışmalar, klinik olarak anlamlı bir konsantrasyonda risperidonun, CYP 1A2, CYP 2A6, CYP 2C8 / 9/10, CYP 2D6, CYP dahil olmak üzere sitokrom P450 izoenzimleri tarafından metabolize edilen ilaçların metabolizmasını önemli ölçüde inhibe etmediğini göstermiştir. 2E1, CYP 3A4 ve CYP 3A5. Oral risperidon uygulamasından bir hafta sonra, dozun %70'i idrarla ve %14'ü feçesle atılır. İdrarda, risperidon artı 9-hidroksi-risperidon, oral yoldan uygulanan dozun %35-45'ini oluşturur. Geri kalan, aktif olmayan metabolitler ile temsil edilir. Eliminasyon aşaması, enjektabl RISPERDAL'in son enjeksiyonundan yaklaşık 7-8 hafta sonra tamamlanır.
doğrusallık
Enjektabl RISPERDAL'in tek dozlarını takiben risperidonun farmakokinetiği, 12.5 ila 75 mg doz aralığında doğrusaldır Risperidon farmakokinetiği, her 2 haftada bir enjekte edilen 25 ila 50 mg doz aralığında da doğrusaldır.
Yaşlı hastalar, karaciğer ve böbrek yetmezliği
Oral risperidon ile yapılan tek doz farmakokinetik çalışma, yaşlılarda aktif antipsikotik fraksiyonun ortalama %43 daha yüksek plazma konsantrasyonlarını, %38 daha uzun yarılanma ömrünü ve aktif antipsikotik fraksiyonun %30 daha düşük klerensini göstermiştir. böbrek yetmezliği olan, daha yüksek plazma aktif antipsikotik fraksiyonun konsantrasyonları ve aktif antipsikotik fraksiyonun klerensinde ortalama %60 oranında azalma gözlenmiştir.
Farmakokinetik / farmakodinamik ilişki
Faz III çalışmalarda, ilacın etkililiğini ve güvenliğini değerlendirmek için yapılan takip ziyaretleri sırasında, aktif antipsikotik fraksiyonun plazma konsantrasyonları ile PANSS toplam skorundaki değişiklik arasında bir ilişki bulunmamıştır (Pozitif ve Negatif Sendrom Ölçeği) ve ESRS (Ekstrapiramidal Belirti Derecelendirme Ölçeği) Toplam.
Seks, ırk ve sigara
Bir popülasyon farmakokinetik analizi, risperidonun veya aktif antipsikotik fraksiyonunun farmakokinetik profili üzerinde cinsiyet, ırk veya sigara kullanımının belirgin bir etkisi olmadığını ortaya koydu.
05.3 Klinik öncesi güvenlik verileri
Sıçanlarda ve köpeklerde oral risperidon ile yapılan (alt) kronik toksisite çalışmalarına benzer şekilde, RISPERDAL enjektabl tedavisinin (12 aya kadar intramüsküler uygulama) ana etkileri, meme bezinin prolaktin aracılı stimülasyonu, erkek ve dişi genital kanallarındaki değişikliklerdir. ve merkezi sinir sistemi (CNS) etkileri, risperidonun farmakodinamik aktivitesi ile ilgili olarak Oral risperidon ile tedavi edilen jüvenil sıçanlarda yapılan bir toksisite çalışmasında, yavru ölümlerinde artış ve gecikme gözlenmiştir. Fiziksel gelişimde. Jüvenillerde 40 haftalık bir çalışmada oral risperidon ile tedavi edilen köpeklerde cinsel olgunlaşma gecikmiştir. "EAA, köpeklerde uzun kemik büyümesi etkilenmedi, köpeklerde 3,6 kat l" maruziyette maksimum insan oral maruziyeti (1.5 mg/gün), uzun kemikler ve olgunlaşma üzerindeki etkiler gözlendi ergenlerde maksimum insan oral maruziyetinin 15 katına eşit maruziyetler için cinsel eylem.
Risperidon, sıçanlarda ve tavşanlarda teratojenik değildi. Risperidon ile sıçan üreme çalışmalarında, ebeveyn çiftleşme ve yavruların doğum ağırlığı ve hayatta kalma üzerinde olumsuz etkiler gözlenmiştir.Risperidon'a intrauterin maruziyet, sıçanlarda yetişkin bilişsel eksiklikler ile ilişkilendirilmiştir.Diğerleri.Dopamin antagonistleri, hamile hayvanlara uygulandığında, üzerinde olumsuz etkilere neden olmuştur. yavruların öğrenmesi ve motor gelişimi.
Erkek ve dişi sıçanlarda 12 ve 24 ay süreyle enjeksiyonluk RISPERDAL uygulaması, 40 mg/kg/2 hafta dozunda osteodistrofi ile sonuçlanmıştır. Sıçanlarda osteodistrofi için doz etkisi, mg/m2 bazında, önerilen maksimum insan dozundan 8 kat daha fazladır ve önerilen maksimum doza insanda beklenen maksimum maruziyetin iki katı bir plazma maruziyeti ile ilişkilendirilmiştir. 20 mg / kg / 2 haftaya kadar enjektabl RISPERDAL, osteodistrofi gözlenmedi.Bu doz, önerilen maksimum insan dozunun 14 katına kadar plazma maruziyeti üretti.
Genotoksik potansiyel kanıtı bulunamadı.
Güçlü bir dopaminerjik D2 reseptör antagonisti için beklendiği gibi, hipofiz bezi adenomlarında (fare), endokrin pankreas adenomlarında (sıçan) ve meme bezi adenomlarında (her iki tür) artışlar.
Wistar (Hannover) sıçanlarında (5 ve 40 mg/kg / 2 haftalık dozlarda) enjektabl RISPERDAL ile yapılan bir intramüsküler karsinojenisite çalışmasında, endokrin pankreas, hipofiz ve medüller tümör insidansında artış gözlenmiştir. 40 mg/kg, meme bezi tümörleri ise hem 5 hem de 40 mg/kg dozlarında gözlendi. Oral ve intramüsküler uygulamayı takiben gözlenen bu tümörler, uzun süreli dopaminerjik D2 antagonizması ve hiperprolaktinemi ile ilişkili olabilir. Doku kültürü çalışmaları, insan meme tümörlerinde hücre büyümesinin prolaktin tarafından uyarılabileceğini göstermektedir.RISPERDAL enjektabl ile tedavi edilen sıçanlarda, adrenal medulla tümörlerinin insidansının artmasına katkıda bulunduğu düşünülen hiperkalsemi, her iki doz grubunda da gözlenmiştir.Klinik kanıt yoktur. hiperkalseminin insanlarda feokromositoma neden olabileceğini önermek.
40 mg / kg / 2 hafta enjeksiyon için RISPERDAL dozu ile erkek sıçanlarda renal tübüler adenomlar bulundu. Düşük dozlu tedavi grubunda, %0.9 NaCl veya boncuk aracı kontrol grubunda böbrek tümörü gözlenmedi. Enjektabl RISPERDAL ile tedavi edilen erkek Wistar (Hannover) sıçanlarında böbrek tümörlerinin başlangıcının altında yatan mekanizma bilinmemektedir. böbrek tümörü insidansı gözlendi. Tümör organ profilindeki alt tür farklılıklarını incelemek için yürütülen klinik çalışmalar, kanserojenlik çalışmasında kullanılan Wistar (Hanover) alt türünün, oral kanserojenlik çalışmasında kullanılan Wistar (Wiga) alt türünden spontanelik açısından önemli ölçüde farklı olduğunu göstermektedir. , yaşa bağlı, böbreklerde neoplastik olmayan değişiklikler, risperidona yanıt olarak artan serum prolaktin ve böbrek değişiklikleri Kronik enjektabl RISPERDAL ile tedavi edilen köpeklerde böbrek ile ilgili değişiklikleri öneren hiçbir veri yoktur.
Sıçanlarda osteodistrofi, prolaktin aracılı tümörler ve muhtemelen alt türe özgü böbrek tümörlerinin insan riski açısından önemi bilinmemektedir.
Enjeksiyonluk RISPERDAL'in yüksek dozlarının uygulanmasından sonra, köpeklerde ve sıçanlarda enjeksiyon bölgesinde lokal tahriş gözlenmiştir. Sıçanlarda yapılan 24 aylık bir intramüsküler karsinojenisite çalışmasında, ne araç ne de aktif ilaç grubunda enjeksiyon bölgesinde tümör insidansında bir artış gözlenmemiştir.
Hayvan modelleri, hem in vitro hem de in vivo olarak, risperidonun yüksek dozlarda QT aralığının uzamasına neden olabileceğini ve bunun artan teorik risk ile ilişkili olduğunu göstermektedir. nokta kıvrımları hastalarda.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
Toz:
[poli- (d, 1-Laktid-ko-Glikolid)]
çözücü:
polisorbat 20
karmeloz sodyum
Disodyum hidrojen fosfat dihidrat
susuz sitrik asit
Sodyum klorit
Sodyum hidroksit
Enjeksiyonlar için su.
06.2 Uyumsuzluk
Bu tıbbi ürün, bölüm 6.6'da belirtilenler dışında başka tıbbi ürünlerle karıştırılmamalıdır.
06.3 Geçerlilik süresi
2 - 8 ° C'de 3 yıl
Sulandırıldıktan sonra: Kimyasal ve fiziksel olarak 25 °C'de 24 saat kullanım stabilitesi kanıtlanmıştır.
Mikrobiyolojik açıdan ürün hemen kullanılmalıdır.
Hemen kullanılmazsa, kullanım sırasındaki saklama süreleri ve kullanımdan önceki koşullar kullanıcının sorumluluğundadır ve sulandırma aseptik koşullar altında kontrol edilip onaylanmadıkça, normalde 25 °C'de 6 saatten uzun olmayacaktır.
06.4 Depolama için özel önlemler
Paketin tamamını buzdolabında (2 - 8°C) saklayınız.
Eğer soğutma mümkün değilse, RISPERDAL enjekte edilebilir, uygulamadan önce en fazla 7 gün süreyle 25 °C'yi aşmayan bir sıcaklıkta saklanabilir.
Orijinal ambalajında saklayın.
Sulandırılmış tıbbi ürünün saklama koşulları için bkz. bölüm 6.3.
06.5 İç ambalajın yapısı ve paketin içeriği
• RISPERDAL tozu içeren bir şişe
• Sulandırma için West-Medimop Flakon Adaptör Sistemi (flakon adaptörü)
• RISPERDAL için solvent içeren kullanıma hazır bir şırınga
• Kas içi enjeksiyon için iki Terumo SurGuard-3 iğnesi (1 inç (0,8 mm x 25 mm) deltoid uygulama için iğne korumalı UTW 21G güvenlik iğnesi ve 2 inç 20G TW güvenlik iğnesi -inç (0,9 mm x 51 mm) kalçaya uygulama için iğne koruma cihazı ile).
06.6 Kullanım ve kullanım talimatları
Önemli bilgi
Risperdal Enjeksiyon, başarılı bir uygulama sağlamak ve kit kullanımında zorluklardan kaçınmak için "Kullanım Talimatları"ndaki adımlara özel dikkat gösterilmesini gerektirir.
Sağlanan bileşenleri kullanın
Kitle birlikte verilen bileşenler, Risperdal ile kullanım için özel olarak tasarlanmıştır.
Risperdal yalnızca pakette sağlanan solvent ile sulandırılmalıdır.
Paketin HİÇBİR bileşenini değiştirmeyin.
Süspansiyonu sulandırdıktan sonra saklamayın.
Süspansiyonun çökmesini önlemek için, dozu sulandırdıktan hemen sonra uygulayınız.
Doğru dozun uygulanması
Amaçlanan Risperdal dozunun verilmesini sağlamak için flakonun tüm içeriği uygulanmalıdır.
TEK KULLANIMLIK CİHAZ
Yeniden kullanmayın. Tıbbi cihazların düzgün çalışması için belirli malzeme özellikleri gerekir. Bu özellikler yalnızca tek kullanım için doğrulanmıştır. Cihazı sonraki kullanım için yeniden kullanmaya yönelik herhangi bir girişim, cihazın bütünlüğünü olumsuz etkileyebilir veya çalışmasında bozulmaya neden olabilir.
Adım 1 (Bileşenleri birleştirin)
Paketten kaldır
Şişe adaptörünü şişeye bağlayın
30 dakika bekleyin
Enjeksiyonluk Risperdal paketini buzdolabından çıkarın ve sulandırmadan yaklaşık 30 dakika önce oda sıcaklığına getirin.
Başka bir şekilde tekrar ısıtmayın.
Kapağı şişeden çıkarın. Renkli koruyucu kapağı flakondan çıkarın.
Gri kapağın üstünü bir alkollü mendil.
Hava kurumasına izin verin.
Gri lastik kapağı çıkarmayın.
Şişe adaptörünü hazırlayın
Steril blisteri gösterildiği gibi saklayın.
Arka filmi soyun ve çıkarın.
Flakon adaptörünü blisterden çıkarmayın.
Cihazın sivri ucuna asla dokunmayın. Bu kontaminasyona yol açacaktır.
Şişe adaptörünü şişeye bağlayın
Şişeyi sert bir yüzeye yerleştirin ve şişenin tabanını tutun. Flakon adaptörünü gri kauçuk tıpanın ortasına yerleştirin. Adaptörü, klik sesi gelene kadar flakonun üst kısmından aşağıya doğru itin.
Şişe adaptörünü açılı bir konumda yönlendirmeyin, aksi takdirde seyreltici şişeye aktarılırken sızabilir.
Kullanıma hazır şırıngayı flakon adaptörüne bağlayın
Steril blisteri çıkarın
Sadece kullanıma hazır enjektörün beyaz kapağını çıkarmaya hazır olduğunuzda flakon adaptörünü steril blisterden çıkarın.
Sızıntıyı önlemek için flakonu dik tutun.
Şişenin tabanını tutun ve steril blisteri kaldırın.
Sallamayın.
Açıkta kalan flakon adaptörünün luer portuna dokunmayın.
Bu kontaminasyona yol açacaktır.
doğru tutun
Beyaz yakayı şırınganın ucunda tutun.
Montaj sırasında şırıngayı cam gövdesinden tutmayın.
Kapağı çıkarın
Beyaz yakayı tutarak beyaz kapağı kapatın.
Beyaz kapağı bükmeyin veya kesmeyin.
Şırınganın ucuna dokunmayın. Bu kontaminasyona yol açacaktır.
Çıkarılan kapak çıkarılabilir.
Şırıngayı flakon adaptörüne bağlayın
Sabit tutmak için adaptörün üzerindeki halkayı tutun.
Şırıngayı beyaz yakasından tutun, ardından ucu adaptörün luer portuna yerleştirin.
Şırıngayı cam gövdesinden tutmayın.
Beyaz yaka gevşeyebilir veya çıkabilir.
Şırıngayı adaptöre takın saat yönünde dönüş kanca gibi görünene kadar sağlam bir hareketle.
Aşırı sıkmayın. Zorlamak şırınga ucunun kırılmasına neden olabilir.
Adım 2 (Mikrokürelerin yeniden yapılandırılması)
Seyrelticiyi enjekte edin
Şırınganın tüm içeriğini şişeye enjekte edin.
Şişenin içeriği artık baskı altında olacaktır. Pistonu baş parmağınızla basılı tutun.
Seyreltici içinde boncukları askıya alın
Pistonu tutmaya devam ederken, sallayın. enerjik olarak gösterildiği gibi en az 10 saniye
Süspansiyonu kontrol edin. Doğru şekilde karıştırıldığında, süspansiyon homojen, yoğun ve süt renginde görünür. Mikroküreler sıvının içinde görünür olacaktır.
Süspansiyonun yerleşmemesi için hemen bir sonraki adıma geçin.
Süspansiyonu şırıngaya aktarın
Şişeyi tamamen çevirin. Şişedeki tüm içeriği şırıngaya çekmek için pistonu yavaşça çekin.
Şişe adaptörünü çıkarın
Şırınganın beyaz yakasını kavrayın ve adaptörden çıkarın.
Delikteki flakonun etiket kısmını çıkarın.
Tanımlama için etiketin soyulmuş kısmını şırıngaya takın.
Adım 3 (iğneyi takın)
Uygun iğneyi seçin
İğneyi enjekte edeceğiniz konuma göre seçin (kalça veya deltoid).
iğneyi takın
Sarma filmini kısmen soyun ve gösterildiği gibi iğne tabanını tutmak için kullanın.
Şırınganın beyaz yakasını tutarak, şırıngayı iğnenin luer bağlantısına takın. saat yönünde dönüş yerine oturana kadar sağlam bir hareketle.
İğnenin luer portuna dokunmayın. Bu kontaminasyona yol açacaktır.
Boncukları yeniden askıya alın
İğne paketini tamamen çıkarın Enjeksiyondan hemen önce, sulandırılmış ürün bu arada çökeceğinden şırıngayı bir kez daha kuvvetlice sallayın.
Adım 4 (dozu enjekte edin)
Şeffaf iğne kutusunu çıkarın
İğnenin güvenlik cihazını şırıngaya doğru hareket ettirin,
gosterildigi gibi.Ardından şırınganın beyaz yakasını tutun ve dikkatlice ancak sağlam bir hareketle şeffaf kılıfı çıkarın.
Luer bağlantısı gevşeyebileceğinden kasayı döndürmeyin.
Hava kabarcıklarını çıkarın
Şırıngayı dik tutun ve hava kabarcıklarının üste çıkması için hafifçe vurun.
Havayı çıkarmak için pistonu yavaşça ve dikkatlice yukarı doğru bastırın.
Enjeksiyon
Şırınganın tüm içeriğini hemen hastanın kalçasına veya deltoidine kas içine enjekte edin.
Popoya enjeksiyon, popo bölgesinin üst dış kadranına yapılmalıdır.
İntravenöz olarak uygulamayın.
Emniyet cihazındaki iğneyi kapatın
İle birlikte bir eliğne güvenlik cihazını sert, düz bir yüzeye 45 derecelik bir açıyla yerleştirin.İğne güvenlik cihazına tam olarak girene kadar hızlı ve sert bir hareketle bastırın.
Yaralanmaktan kaçının
İki el kullanmayın.
İğne güvenlik cihazını devre dışı bırakmayın veya kurcalamayın.
İğne bükülmüş veya hasarlıysa iğneyi düzeltmeye veya güvenlik cihazını takmaya çalışmayın.
İğneleri uygun şekilde atın
İğnenin güvenlik cihazına tam olarak oturduğunu kontrol edin.
Uygun ve onaylanmış bir kapta imha edin.
Ayrıca pakette bulunan kullanılmamış iğneyi de atın.
07.0 PAZARLAMA YETKİ SAHİBİ
Janssen-Cilag SpA
M.Buonarroti aracılığıyla, 23
20093 Cologno Monzese (MI)
08.0 PAZARLAMA YETKİ NUMARASI
RISPERDAL 25 mg / 2ml intramüsküler kullanım için enjeksiyon için uzun süreli salımlı süspansiyon için toz ve solvent - 1 flakon toz + 2ml solvent içeren kullanıma hazır şırınga
AIC N° 028752172
RISPERDAL 37.5 mg / 2ml intramüsküler kullanım için enjeksiyon için uzun süreli salımlı süspansiyon için toz ve solvent - 1 flakon toz + 2 ml solvent içeren önceden doldurulmuş bir şırınga
AIC N° 028752184
RISPERDAL 50 mg / 2ml intramüsküler kullanım için enjeksiyon için uzun süreli salımlı süspansiyon için toz ve solvent - 1 flakon toz + 2 ml solvent içeren önceden doldurulmuş bir şırınga
AIC N° 028752196
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
Ağustos 2005
10.0 METİN REVİZYON TARİHİ
Nisan 2015