Aktif maddeler: Darbepoetin alfa
Kullanıma hazır şırıngada ARANESP 10 mikrogram enjeksiyonluk çözelti
Kullanıma hazır şırıngada ARANESP 15 mikrogram enjeksiyonluk çözelti
Aranesp 20 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Kullanıma hazır şırıngada 30 mikrogram enjeksiyonluk ARANESP solüsyonu
Kullanıma hazır şırıngada ARANESP 40 mikrogram enjeksiyonluk çözelti
Kullanıma hazır şırıngada ARANESP 50 mikrogram enjeksiyonluk çözelti
Aranesp 60 mikrogram kullanıma hazır şırıngada enjeksiyonluk çözelti
Kullanıma hazır şırıngada ARANESP 80 mikrogram enjeksiyonluk çözelti
Aranesp 100 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Aranesp 130 mikrogram kullanıma hazır enjektörde enjeksiyonluk çözelti
Kullanıma hazır şırıngada 150 mikrogram ARANESP enjeksiyonluk çözelti
Aranesp 300 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Kullanıma hazır şırıngada 500 mikrogram enjeksiyonluk ARANESP solüsyonu
Paket boyutları için Aranesp prospektüsleri mevcuttur: - Aranesp kullanıma hazır şırıngada 10 mikrogram enjeksiyonluk solüsyon, Aranesp kullanıma hazır enjektörde 15 mikrogram enjeksiyonluk solüsyon, Aranesp 20 mikrogram kullanıma hazır enjektörde enjeksiyonluk solüsyon, Aranesp 30 mikrogram kullanıma hazır şırıngada enjeksiyonluk solüsyon, Aranesp 40 50 mikrogram enjeksiyonluk çözelti içinde mikrogram enjeksiyonluk çözelti, kullanıma hazır enjektörde 50 mikrogram enjeksiyonluk çözelti içinde Aranesp 40 mikrogram enjeksiyonluk çözelti, kullanıma hazır enjektörde 60 mikrogram enjeksiyonluk çözelti Aranesp, ön-dolu şırıngada Aranesp 80 mikrogram enjeksiyonluk çözelti Aranesp kullanıma hazır şırıngada 100 mikrogram enjeksiyonluk solüsyon, Aranesp kullanıma hazır enjektörde 130 mikrogram enjeksiyonluk solüsyon, Aranesp kullanıma hazır enjektörde 150 mikrogram enjeksiyonluk solüsyon, Aranesp kullanıma hazır enjektörde 150 mikrogram enjeksiyonluk solüsyon Aranesp 150 mikrogram kullanıma hazır şırıngada enjeksiyonluk çözelti 300 mikrogram kullanıma hazır şırıngada enjeksiyonluk çözelti, Aranesp 500 mikrogram kullanıma hazır şırıngada enjeksiyonluk çözelti
- Aranesp 10 mikrogramlık kullanıma hazır kalemde enjeksiyonluk solüsyon (SureClick), Aranesp 15 mikrogramlık kullanıma hazır kalemde enjeksiyonluk solüsyon (SureClick), Aranesp 20 mikrogramlık kullanıma hazır kalemde enjeksiyonluk solüsyon (SureClick), kullanıma hazır kalemde enjeksiyon (SureClick), kullanıma hazır kalemde enjeksiyon için Aranesp 40 mikrogram solüsyonu (SureClick), kullanıma hazır kalemde (SureClick) Aranesp 50 mikrogram enjeksiyonluk solüsyonu, kullanıma hazır doldurulmuş kalemde Aranesp 60 mikrogram enjeksiyonluk solüsyonu kalem (SureClick), Aranesp 80 mikrogram kullanıma hazır kalemde enjeksiyonluk solüsyon (SureClick), Aranesp 100 mikrogram kullanıma hazır kalemde enjeksiyonluk solüsyon (SureClick), kullanıma hazır kalemde Aranesp 130 mikrogram enjeksiyonluk solüsyon (SureClick), Aranesp 150 mikrogram kullanıma hazır kalemde enjeksiyonluk solüsyon (SureClick), Aranesp 300 mikrogram kullanıma hazır kalemde enjeksiyonluk solüsyon (SureClick), Aranesp 500 mikrogram enjeksiyonluk solüsyon kullanıma hazır kalem (SureClick
- Aranesp flakonda 25 mikrogram enjeksiyonluk çözelti, flakonda Aranesp 40 mikrogram enjeksiyonluk çözelti, flakonda 60 mikrogram enjeksiyonluk çözelti Aranesp, flakon içinde 100 mikrogram enjeksiyonluk çözelti Aranesp, flakon içinde Aranesp 200 mikrogram enjeksiyonluk çözelti, flakon içinde Aranesp 300 mikrogram enjeksiyonluk çözelti şişeye enjeksiyon
Aranesp neden kullanılır? Bu ne için?
Doktor, anemisini tedavi etmek için Aranesp'i (bir antianemik) reçete etti. Kanda yeterli sayıda kırmızı kan hücresi olmadığında anemiden muzdarip olursunuz ve anemi belirtileri yorgunluk, halsizlik ve nefes darlığı olabilir.
Aranesp, doğal hormon olan eritropoietin ile tamamen aynı şekilde çalışır.Eritropoietin böbrekler tarafından üretilir ve kemik iliğini daha fazla kırmızı kan hücresi üretmesi için uyarır. Aranesp'teki aktif madde, genetik mühendisliği ile Çin hamsteri yumurtalık hücrelerinde (CHO-K1) üretilen darbepoetin alfa'dır.
Kronik böbrek yetmezliğiniz varsa
ARANESP, yetişkinlerde ve çocuklarda kronik böbrek yetmezliği ile ilişkili semptomatik anemiyi tedavi etmek için kullanılır.Böbrek yetmezliğinde, böbrekler genellikle anemiye neden olabilen doğal hormon eritropoietin'i yeterince üretmez.
Vücudunuzun daha fazla kırmızı kan hücresi yapması biraz zaman alacak ve ardından herhangi bir etki fark etmeniz yaklaşık dört hafta sürecektir.Aranesp'in anemiyi tedavi etme yeteneği normal diyaliz uygulamasından etkilenmeyecektir.
Kemoterapi alıyorsanız
ARANESP, kemoterapi alan ve kemik iliği dışı tümörleri olan (miyeloid olmayan maligniteler) yetişkin hastalarda semptomatik anemi tedavisinde kullanılır.
Kemoterapinin ana yan etkilerinden biri, kemik iliğinin yeterli kan hücresi üretmesini engellemesidir. Kemoterapi tedavinizin sonuna doğru, özellikle çok fazla kemoterapi aldıysanız, kırmızı kan hücre sayınız düşebilir ve sizi anemik hale getirebilir.
Kontrendikasyonlar Aranesp ne zaman kullanılmamalıdır?
Aranesp'i kullanmayın
- darbepoetin alfaya veya bu ilacın içerdiği diğer maddelerden herhangi birine karşı alerjiniz varsa (bölüm 6'da listelenmiştir).
- Doktorunuz tarafından reçete edilen diğer ilaçlarla şu anda kontrol altına alınamayan yüksek tansiyon teşhisi konduysa
ARANESP'i kullanmadan önce dikkat edilmesi gerekenler
ARANESP'i kullanmadan önce doktorunuzla, eczacınızla veya hemşirenizle konuşun.
Aşağıdakilerden muzdaripseniz veya geçmişte yaşadıysanız doktorunuza söyleyiniz:
- şu anda tıbbi olarak reçete edilen ilaçlarla kontrol edilen yüksek tansiyon;
- Orak hücre anemisi;
- nöbetler (konvülsiyonlar);
- konvülsiyonlar (uyuyor veya uyuyor);
- karaciğer hastalığı;
- anemiyi tedavi etmek için kullanılan ilaçlara önemli yanıt eksikliği;
- lateks alerjisi (kullanıma hazır şırınganın iğne kapağı lateks türevi içerir); veya
- Hepatit C.
Özel uyarılar:
- Olağandışı yorgunluk ve güç kaybı gibi semptomlar yaşarsanız, hastalarda bildirilen saf kırmızı hücre aplazisine (PRCA) sahip olabilirsiniz. PRCA, vücudun ciddi anemiye neden olan kırmızı kan hücrelerinin üretimini durdurması veya üretimini azaltması anlamına gelir.Bu semptomları yaşarsanız, en iyi anemi tedavi stratejisine karar verecek olan doktorunuzu bilgilendirmelisiniz.
- Kırmızı kan hücrelerinin üretimini uyaran diğer ilaçları alırken özel dikkat gösterin: ARANESP, insan eritropoietininin yanı sıra kırmızı kan hücrelerinin üretimini de uyaran bir ürün grubuna dahildir. Sağlık uzmanınız, aldığınız ilacın her zaman doğru adını kaydetmelidir.
- Doktorunuz, hemoglobin düzeyinizi 10 ila 12 g/dl arasında tutmaya çalışmalıdır.Yüksek hemoglobin düzeyleri sizi kalp veya kan damarı sorunları yaşama riskine sokabileceğinden ve kan damarı sorunlarını artırabileceğinden, doktorunuz hemoglobin düzeyinizin belirli bir düzeyi aşmadığını kontrol edecektir. miyokard enfarktüsü, felç ve ölüm riskleri.
- Kronik böbrek yetmezliğiniz varsa, hemoglobin çok yüksek tutulursa ciddi kalp veya kan damarı sorunları (kardiyovasküler olaylar) riski artar.
- Şiddetli baş ağrısı, uyku hali, kafa karışıklığı, görme sorunları, mide bulantısı, kusma veya nöbetler gibi semptomlarınız varsa, bu çok yüksek tansiyonunuz olduğu anlamına gelebilir. Bu semptomları yaşarsanız, doktorunuza başvurmalısınız.
- Kanseriniz varsa, Aranesp'in kan hücreleri için bir büyüme faktörü olarak hareket edebileceğini ve bazı durumlarda kanser üzerinde olumsuz etkileri olabileceğini bilmelisiniz. Spesifik duruma bağlı olarak, kan transfüzyonu tercih edilebilir. Bunu doktorunuzla tartışın.
- Sağlıklı denekler tarafından uygunsuz kullanım, kişiyi hemen hayati tehlikeye sokan kalp ve damar sorunlarına neden olabilir.
Etkileşimler Hangi ilaçlar veya yiyecekler ARANESP'in etkisini değiştirebilir
Diğer ilaçlar ve Aranesp
Başka ilaçlar kullanıyorsanız, yakın zamanda kullandıysanız veya kullanabilecekseniz doktorunuza veya eczacınıza söyleyiniz.
Siklosporin ve takrolimus ilaçları (bağışıklık sistemini baskılayan ilaçlar) kırmızı kan hücrelerinin sayısından etkilenebilir. Bu ilaçlardan herhangi birini alıyorsanız doktorunuza söylemeniz önemlidir.
Aranesp'in yiyecek ve içecek ile kullanılması
Yiyecek ve içecekler Aranesp'i etkilemez.
Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme
Hamileyseniz veya emziriyorsanız, hamile olabileceğinizi düşünüyorsanız veya bebek sahibi olmayı planlıyorsanız, bu ilacı almadan önce doktorunuza veya eczacınıza danışınız.
ARANESP hamile kadınlarda test edilmemiştir. Aşağıdaki durumlarda doktorunuza söylemeniz önemlidir:
- hamile;
- hamile olabileceğinizi düşünüyorsunuz; veya
- hamilelik planlıyor.
Darbepoetin alfa'nın insan sütüne geçip geçmediği bilinmemektedir. ARANESP kullanıyorsanız emzirmeyi bırakmalısınız.
Araç ve makine kullanma
ARANESP'in araç veya makine kullanma yeteneğini sınırlaması beklenmez.
ARANESP sodyum içerir
Bu tıbbi ürün, doz başına 1 mmol'den (23 mg) daha az sodyum içerir, yani esasında sodyum içermez.
Doz, Yöntem ve Uygulama Süresi Aranesp nasıl kullanılır: Pozoloji
Bu ilacı her zaman tam olarak doktorunuzun veya eczacınızın size söylediği şekilde kullanın. Şüpheniz varsa, doktorunuza veya eczacınıza danışın.
Bazı kan testlerine dayanarak, hemoglobin seviyeniz 10 g/dl veya daha az olduğu için doktorunuz ARANESP'e ihtiyacınız olduğunu belirledi.Doktorunuz, hemoglobin düzeyini 10 ile 12 arasında tutmak için ARANESP'in ne kadar ve ne sıklıkla verildiğini size söyleyecektir. g / dl.Bu, yetişkin veya çocuk olmasına bağlı olarak değişebilir.
Aranesp'i kendinize nasıl enjekte edersiniz
Doktorunuz, sizin veya bakıcınızın ARANESP'i enjekte etmesinin en iyisi olduğuna karar verebilir. Doktorunuz, hemşireniz veya eczacınız kullanıma hazır enjektörü kendinize nasıl enjekte edeceğinizi gösterecektir. Size nasıl yapılacağı söylenmediyse kendi kendinize enjekte etmeye çalışmayın.
Kronik böbrek yetmezliğiniz varsa
Kronik böbrek yetmezliği olan ≥ 11 yaşındaki tüm yetişkin ve pediyatrik hastalarda ARANESP, deri altına (deri altı) veya damar içine (intravenöz) tek bir enjeksiyon olarak uygulanır.
Anemiyi düzeltmek için vücut ağırlığının kilogramı başına ARANESP'in başlangıç dozu şöyle olacaktır:
- 0.75 mikrogram iki haftada bir veya
- Haftada bir kez 0.45 mikrogram.
Diyalize girmeyen yetişkin hastalarda da başlangıç dozu olarak ayda bir kez 1.5 mikrogram/kg kullanılabilir.
Kronik böbrek yetmezliği olan ≥ 11 yaşındaki tüm yetişkin ve pediyatrik hastalar, anemileri düzeltildikten sonra, haftada bir veya iki haftada bir olmak üzere tek enjeksiyon olarak ARANESP almaya devam edecektir. ayrıca ayda bir enjeksiyon olarak da verilebilir.
Doktorunuz, aneminizin nasıl yanıt verdiğini kontrol etmek için düzenli kan testleri yaptıracak ve gerektiğinde dört haftada bir dozunuzu ayarlayabilir.
Aneminiz düzeldikten sonra doktorunuz düzenli kan testleri yaptırmaya devam edecek ve aneminin uzun süreli kontrolünü sağlamak için doz yine de ayarlanabilir. Dozun değişip değişmeyeceği konusunda doktorunuz sizi bilgilendirecektir.
Tansiyonunuz da özellikle tedavinin başlangıcında düzenli olarak kontrol edilecektir.
Bazı durumlarda doktorunuz demir takviyesi almanızı önerebilir.
Doktorunuz enjeksiyonun uygulanma şeklini değiştirmeye karar verebilir (deri altına veya damar içine) Eğer enjeksiyon şeklini değiştirirseniz, daha önce aldığınız dozla başlayacaksınız ve doktorunuz bazı testler yapacaktır. Aneminin her zaman doğru şekilde tedavi edilmesini sağlamak için kan testleri.
Doktorunuz tedavinizi r-HuEPO'dan (genetik teknolojiyle üretilen eritropoietin) Aranesp'e değiştirmeye karar verdiyse, ARANESP'in ne sıklıkta haftada bir veya iki haftada bir verilmesi gerektiğine de karar verecektir. r-HuEPO için, ancak doktorunuz size ne kadar ve ne zaman alacağınızı söyleyecektir ve gerekirse dozu ayarlayabilir.
Kemoterapi alıyorsanız
ARANESP haftada bir veya üç haftada bir cilt altına tek enjeksiyon olarak verilir.
Anemiyi düzeltmek için başlangıç dozu şöyle olacaktır:
- Her üç haftada bir 500 mikrogram (vücut ağırlığının kilogramı başına 6.75 mikrogram Aranesp) veya
- Vücut ağırlığının kilogramı başına 2.25 mikrogram (haftada bir kez) Aranesp.
Doktorunuz aneminizin nasıl tepki verdiğini kontrol etmek için düzenli kan testleri yaptıracak ve gerektiği şekilde dozu ayarlayabilir.Tedavi, kemoterapinin seyri bittikten sonra yaklaşık dört hafta devam edecektir.Doktorunuz ilacı tam olarak ne zaman bırakacağınızı size söyleyecektir. Aranesp.
Bazı durumlarda doktorunuz demir takviyesi almanızı önerebilir.
ARANESP kullanıma hazır şırıngayı kendinize enjekte etmek için talimatlar
Bu bölüm ARANESP'i kendinize nasıl enjekte edeceğinize dair bilgiler içermektedir.Doktorunuz, hemşireniz veya eczacınız tarafından size nasıl enjekte edileceği söylenmediyse kendi kendinize enjekte etmeye çalışmamanız önemlidir.Nasıl enjekte edileceğine dair herhangi bir sorunuz varsa, yardım için doktorunuza, hemşirenize veya eczacınıza
ARANESP, siz veya enjeksiyonu yapan kişi tarafından kullanıma hazır enjektörde nasıl kullanılır?
Doktorunuz, ARANESP'i derinin hemen altındaki dokuya enjeksiyon için kullanıma hazır enjektör içinde reçete etmiştir.Doktorunuz, hemşireniz veya eczacınız ne kadar ARANESP'e ihtiyacınız olduğunu ve ne sıklıkla enjekte etmeniz gerektiğini size söyleyecektir.
İhtiyaç duyulan şey:
Kendinize bir enjeksiyon yapmak için ihtiyacınız olacak:
- Aranesp'in yeni kullanıma hazır şırıngası; Ve
- alkollü mendiller veya benzeri dezenfektanlar.
Kendime "deri altı Aranesp enjeksiyonu" yapmadan önce ne yapmalıyım?
- Kullanıma hazır şırıngayı buzdolabından çıkarın. Kullanıma hazır şırıngayı yaklaşık 30 dakika oda sıcaklığında bırakın. Bu enjeksiyonu daha rahat hale getirecektir.Aranesp'i başka bir şekilde ısıtmayın (mikrodalga fırın veya sıcak su gibi).Ayrıca şırıngayı doğrudan güneş ışığına maruz bırakmayın.
- Kullanıma hazır şırıngayı sallamayın.
- Enjekte etmeye hazır olana kadar iğne kapağını şırıngadan çıkarmayın.
- Dozajın tam olarak doktorunuz tarafından reçete edilen doz olup olmadığını kontrol edin.
- Kullanıma hazır şırınga etiketindeki (EXP) son kullanma tarihini kontrol edin.Bu, gösterilen ayın son gününden sonraysa kullanmayın.
- Aranesp'in görünüşünü kontrol edin Berrak, renksiz veya hafif opak bir sıvı olmalıdır.Bulanıksa veya partikül görüyorsanız kullanmamalısınız.
- Ellerinizi iyice yıkayın.
- Rahat, iyi aydınlatılmış, temiz bir yüzey bulun ve ihtiyacınız olan her şeyi elinizin altında tutun.
Aranesp enjeksiyonunu nasıl hazırlarım?
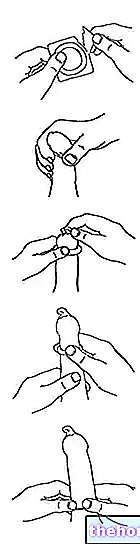
Aranesp'i enjekte etmeden önce şunları yapmalısınız: 1. İğnenin bükülmesini önlemek için, şekil 1 ve 2'de gösterildiği gibi, iğneyi bükmeden kapağı nazikçe çıkarın. 2. İğneye dokunmayın ve pistonu itmeyin. 3. Kullanıma hazır şırıngada küçük bir hava kabarcığı görebilirsiniz.Enjekte etmeden önce hava kabarcığı çıkarmamalısınız.Çözeltiyi hava kabarcığı ile enjekte etmek zararsızdır.4.Şimdi kullanıma hazır şırıngayı kullanabilirsiniz.
Enjeksiyonu nereden almalıyım?
Kendinize enjeksiyon yapmak için en iyi yerler üst uyluklar ve karındır. Bir başkası size enjeksiyon yaparsa, kollarınızın arkasını da kullanabilirsiniz.
Bölgenin kırmızı veya ağrılı olduğunu fark ederseniz enjeksiyon bölgesini değiştirin.
Kendime enjeksiyonu nasıl yaparım?
- Alkollü mendil kullanarak cildi dezenfekte edin ve cildi baş ve işaret parmağınız arasında kaldırın (sıkmadan).
- Doktorunuz, hemşireniz veya eczacınız tarafından gösterildiği gibi iğneyi tamamen cildinize itin.
- Reçete edilen dozu doktorunuz, hemşireniz veya eczacınız tarafından belirtildiği şekilde deri altına enjekte ediniz.
- Pistonu, şırınga boşalana kadar cildi daima sıkıştırarak yavaş, sabit bir basınçla itin.
- İğneyi dışarı çekin ve deriyi bırakın.
- Bir kan lekesi fark ederseniz, enjeksiyon bölgesine bir pamuk topu veya gazlı bezle hafifçe bastırabilirsiniz. Enjeksiyon bölgesini ovalamayın. Gerekirse, enjeksiyon bölgesini yapışkan bir sıva ile kaplayabilirsiniz.
- Her şırıngayı yalnızca bir enjeksiyon için kullanın. Şırıngada kalan Aranesp'i tekrar kullanmayın.
Unutmayın: Herhangi bir sorununuz varsa, yardım veya tavsiye için doktorunuza veya hemşirenize danışmaktan çekinmeyin.
Kullanılmış şırıngaların atılması
- Yanlışlıkla kendinizi delebileceğiniz için kapağı kullanılmış iğnelerin üzerine geri koymayın.
- Kullanılmış şırıngaları çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
- Kullanılmış kullanıma hazır şırıngalar yerel gerekliliklere uygun olarak atılmalıdır. Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorunuz. Bu, çevrenin korunmasına yardımcı olacaktır.
Doz aşımı Çok fazla ARANESP aldıysanız ne yapmalısınız?
Kullanmanız gerekenden daha fazla Aranesp kullandıysanız
ARANESP'i ihtiyacınızdan fazla alırsanız, örneğin çok yüksek tansiyon gibi ciddi sorunlarınız olabilir. Böyle bir durumda doktorunuza, hemşirenize veya eczacınıza, kendinizi iyi hissetmiyorsanız hemen doktorunuza, hemşirenize veya eczacınıza başvurunuz.
ARANESP'i kullanmayı unutursanız
Unutulan bir dozu telafi etmek için çift doz almayınız.
Bir ARANESP dozunu unuttuysanız, bir sonraki enjeksiyonunuzu ne zaman yaptırmanız gerektiğini öğrenmek için doktorunuzla iletişime geçmelisiniz.
ARANESP almayı bırakırsanız
Aranesp'i kullanmayı bırakmak istiyorsanız, bunu önce doktorunuzla konuşmalısınız.
Yan Etkiler Aranesp'in yan etkileri nelerdir?
Tüm ilaçlar gibi, bu ilaç da yan etkilere neden olabilir, ancak bunları herkes almayabilir.
ARANESP uygulamasının ardından bazı hastalarda aşağıdaki yan etkiler görülmüştür:
Kronik böbrek yetmezliği olan hastalar
Çok yaygın: 10 kişiden 1'inden fazlasını etkileyebilir
- Yüksek tansiyon (hipertansiyon)
- Alerjik reaksiyonlar
Yaygın: 10 kişiden 1'ini etkileyebilir
- Felç
- Enjeksiyon yerinde ağrı
- Deri döküntüleri ve/veya deride kızarıklık
Yaygın olmayan: 100 kişiden 1 kişiye kadarını etkileyebilir
- Kan pıhtıları (tromboz)
- Konvülsiyonlar (nöbetler)
Bilinmiyor: mevcut verilerden sıklık tahmin edilemiyor
- Saf kırmızı hücre aplazisi (PRCA) - (anemi, olağandışı yorgunluk, güç kaybı)
Kanserli hastalar
Çok yaygın: 10 kişiden 1'inden fazlasını etkileyebilir
- Alerjik reaksiyonlar
- Sıvı tutulması (ödem)
Yaygın: 10 kişiden 1'ini etkileyebilir
- Yüksek tansiyon (hipertansiyon)
- Kan pıhtıları (tromboz)
- Enjeksiyon yerinde ağrı
- Deri döküntüleri ve/veya deride kızarıklık
Yaygın olmayan: 100 kişiden 1 kişiye kadarını etkileyebilir
- Konvülsiyonlar (nöbetler)
Tüm hastalar
Bilinmiyor: mevcut verilerden sıklık tahmin edilemiyor
Aşağıdakileri içerebilen ciddi alerjik reaksiyonlar:
- Ölümcül olabilen ani alerjik reaksiyonlar (anafilaksi)
- Yüzde, dudaklarda, ağızda, dilde veya boğazda yutmayı veya nefes almayı zorlaştırabilecek şişme (anjiyoödem)
- Nefes darlığı (alerjik bronkospazm)
- Deri döküntüleri
- Kurdeşen (kurdeşen)
Herhangi bir yan etki yaşarsanız, bu broşürde listelenmeyen olası yan etkiler de dahil olmak üzere doktorunuzla veya eczacınızla veya hemşirenizle konuşun.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
Bu ilacı, EXP'den sonra karton ve kullanıma hazır şırınga etiketinde belirtilen son kullanma tarihinden sonra kullanmayın.Son kullanma tarihi o ayın son gününü ifade eder.
Buzdolabında (2°C - 8°C) saklayınız. Dondurmayın. Donmuş olduğunu düşünüyorsanız ARANESP'i kullanmayınız.
İlacı ışıktan korumak için kullanıma hazır enjektörü dış kartonda saklayınız.
Enjeksiyondan önce şırınga buzdolabından çıkarıldıktan ve yaklaşık 30 dakika oda sıcaklığında bırakıldıktan sonra ya 7 gün içinde kullanılmalı ya da atılmalıdır.
Kullanıma hazır enjektörün içeriğinin bulanık olduğunu veya içinde görünür partiküller olduğunu fark ederseniz bu ilacı kullanmayınız.
Herhangi bir ilacı atık su veya evsel atık yoluyla atmayın.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorun.Bu çevrenin korunmasına yardımcı olacaktır.
Kompozisyon ve farmasötik form
Aranesp'in içeriği
- Etkin madde darbepoetin alfa, r-HuEPO'dur (genetik mühendisliği ile üretilen eritropoietin). Kullanıma hazır şırınga 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300 veya 500 mikrogram darbepoetin alfa içerir.
- Diğer bileşenler monobazik sodyum fosfat, dibazik sodyum fosfat, sodyum klorür, polisorbat 80 ve enjeksiyonluk sudur.
Aranesp'in görünüşü ve paketin içeriği
ARANESP, kullanıma hazır şırınga içinde enjeksiyon için berrak, renksiz veya hafif opak bir çözeltidir.
ARANESP 1 veya 4 kullanıma hazır şırıngadan oluşan paketlerde mevcuttur. Şırıngalar, kabarcıklı (1 veya 4 şırıngalı paketler) veya kabarcıksız (1 şırıngalı paketler) paketlenir. Tüm paket boyutları pazarlanmayabilir.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
ARANESP
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Kullanıma hazır şırıngada ARANESP 10 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,4 mL (25 mikrogram/mL) içinde 10 mikrogram darbepoetin alfa içerir.
Kullanıma hazır şırıngada ARANESP 15 mikrogram enjeksiyonluk çözeltiHer kullanıma hazır şırınga, 0,375 mL (40 mcg / mL) içinde 15 mcg darbepoetin alfa içerir.
Aranesp 20 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,5 mL (40 mikrogram/mL) içinde 20 mikrogram darbepoetin alfa içerir.
Kullanıma hazır şırıngada 30 mikrogram enjeksiyonluk ARANESP solüsyonu
Her kullanıma hazır şırınga 0,3 mL (100 mikrogram/mL) içinde 30 mikrogram darbepoetin alfa içerir.
Kullanıma hazır şırıngada ARANESP 40 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0.4 mL (100 mcg / mL) içinde 40 mcg darbepoetin alfa içerir.
Kullanıma hazır şırıngada ARANESP 50 mcg enjeksiyonluk çözeltiHer kullanıma hazır şırınga 0,5 mL (100 mcg/mL) içinde 50 mcg darbepoetin alfa içerir.
Aranesp 60 mikrogram kullanıma hazır şırıngada enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0,3 mL (200 mcg / mL) içinde 60 mcg darbepoetin alfa içerir.
Kullanıma hazır şırıngada ARANESP 80 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0.4 mL (200 mcg / mL) içinde 80 mikrogram darbepoetin alfa içerir.
Aranesp 100 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0,5 mL (200 mcg/mL) içinde 100 mcg darbepoetin alfa içerir.
Aranesp 130 mikrogram kullanıma hazır enjektörde enjeksiyonluk çözelti
Her bir kullanıma hazır şırınga, 0.65 mL (200 mcg / mL) içinde 130 mcg darbepoetin alfa içerir.
Kullanıma hazır şırıngada 150 mikrogram ARANESP enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0,3 mL (500 mcg / mL) içinde 150 mcg darbepoetin alfa içerir.
Aranesp 300 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0.6 mL (500 mcg / mL) içinde 300 mcg darbepoetin alfa içerir.
Kullanıma hazır şırıngada 500 mikrogram enjeksiyonluk ARANESP solüsyonu
Her kullanıma hazır şırınga, 1 mL (500 mcg / mL) içinde 500 mcg darbepoetin alfa içerir.
Kullanıma hazır kalem içinde ARANESP 10 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,4 mL (25 mikrogram/mL) içinde 10 mikrogram darbepoetin alfa içerir.
Kullanıma hazır kalem içinde Aranesp 15 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,375 mL (40 mcg/mL) içinde 15 mikrogram darbepoetin alfa içerir.
Kullanıma hazır kalem içinde Aranesp 20 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,5 mL (40 mikrogram/mL) içinde 20 mikrogram darbepoetin alfa içerir.
Kullanıma hazır kalem içinde ARANESP 30 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0.3 mL (100 mikrogram / mL) içinde 30 mikrogram darbepoetin alfa içerir.
Kullanıma hazır kalemde ARANESP 40 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,4 mL (100 mikrogram/mL) içinde 40 mikrogram darbepoetin alfa içerir.
Kullanıma hazır kalem içinde Aranesp 50 mcg enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,5 mL (100 mikrogram/mL) içinde 50 mikrogram darbepoetin alfa içerir.
Kullanıma hazır kalem içinde ARANESP 60 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,3 mL (200 mikrogram/mL) içinde 60 mikrogram darbepoetin alfa içerir.
Kullanıma hazır kalem içinde ARANESP 80 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0.4 mL (200 mikrogram / mL) içinde 80 mikrogram darbepoetin alfa içerir.
Kullanıma hazır kalem içinde Aranesp 100 mcg enjeksiyonluk solüsyon
Her kullanıma hazır kalem, 0,5 mL (200 mcg/mL) içinde 100 mcg darbepoetin alfa içerir.
Kullanıma hazır kalem içinde Aranesp 130 mcg enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0.65 mL (200 mcg / mL) içinde 130 mcg darbepoetin alfa içerir.
Kullanıma hazır kalem içinde ARANESP 150 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0.3ml (500mcg/ml) içinde 150 mcg darbepoetin alfa içerir.
Kullanıma hazır kalem içinde Aranesp 300 mcg enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0.6 mL (500 mcg/mL) içinde 300 mcg darbepoetin alfa içerir.
Kullanıma hazır kalemde enjeksiyon için Aranesp 500 mcg solüsyonu
Her kullanıma hazır kalem, 1 mL (500 mcg/mL) içinde 500 mcg darbepoetin alfa içerir.
Aranesp 25 mcg flakon içinde enjeksiyonluk çözelti
Her flakon 1 mL'de (25 mikrogram/mL) 25 mikrogram darbepoetin alfa içerir.
Aranesp 40 mcg flakon içinde enjeksiyonluk çözelti
Her flakon 1 mL (40 mcg/mL) içinde 40 mcg darbepoetin alfa içerir.
Aranesp 60 mcg flakon içinde enjeksiyonluk çözelti
Her flakon 1 mL (60 mcg/mL) içinde 60 mcg darbepoetin alfa içerir.
Aranesp 100 mcg flakon içinde enjeksiyonluk çözelti
Her flakon, 1 mL'de (100 mcg/mL) 100 mcg darbepoetin alfa içerir.
Şişe içinde enjeksiyon için Aranesp 200 mcg solüsyonu
Her flakon 1 mL (200 mcg/mL) içinde 200 mcg darbepoetin alfa içerir.
Şişe içinde enjeksiyon için Aranesp 300 mcg solüsyonu
Her flakon 1 mL (300 mcg/mL) içinde 300 mcg darbepoetin alfa içerir.
Darbepoetin alfa, Çin Hamster Yumurtalık (CHO-K1) hücrelerinde genetik mühendisliği ile üretilir.
Etkileri bilinen yardımcı maddeler:
Kullanıma hazır şırıngada ARANESP 10 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0,4 ml'de 1,52 mg sodyum içerir.
Kullanıma hazır şırıngada ARANESP 15 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,375 mL'de 1,42 mg sodyum içerir.
Aranesp 20 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,5 ml'de 1,90 mg sodyum içerir.
Kullanıma hazır şırıngada 30 mikrogram enjeksiyonluk ARANESP solüsyonu
Her kullanıma hazır şırınga 0,3 ml'de 1,14 mg sodyum içerir.
Kullanıma hazır şırıngada ARANESP 40 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0,4 ml'de 1,52 mg sodyum içerir.
Kullanıma hazır şırıngada ARANESP 50 mcg enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,5 ml'de 1,90 mg sodyum içerir.
Aranesp 60 mikrogram kullanıma hazır şırıngada enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,3 ml'de 1,14 mg sodyum içerir.
Kullanıma hazır şırıngada ARANESP 80 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır şırınga, 0,4 ml'de 1,52 mg sodyum içerir.
Aranesp 100 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,5 ml'de 1,90 mg sodyum içerir.
Aranesp 130 mikrogram kullanıma hazır enjektörde enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,65 mL içinde 2,46 mg sodyum içerir.
Kullanıma hazır şırıngada 150 mikrogram ARANESP enjeksiyonluk çözelti
Her kullanıma hazır şırınga 0,3 ml'de 1,14 mg sodyum içerir.
Aranesp 300 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Her kullanıma hazır enjektör 0,6 ml içinde 2,27 mg sodyum içerir.
Kullanıma hazır şırıngada 500 mikrogram enjeksiyonluk ARANESP solüsyonu
Her kullanıma hazır şırınga 1 ml'de 3.79 mg sodyum içerir.
Kullanıma hazır kalem içinde ARANESP 10 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,4 ml'de 1,52 mg sodyum içerir.
Kullanıma hazır kalem içinde Aranesp 15 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,375 mL'de 1,42 mg sodyum içerir.
Kullanıma hazır kalem içinde Aranesp 20 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,5 ml'de 1,90 mg sodyum içerir.
Kullanıma hazır kalem içinde ARANESP 30 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,3 ml'de 1,14 mg sodyum içerir.
Kullanıma hazır kalemde ARANESP 40 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,4 ml'de 1,52 mg sodyum içerir.
Kullanıma hazır kalem içinde Aranesp 50 mcg enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,5 ml'de 1,90 mg sodyum içerir.
Kullanıma hazır kalem içinde ARANESP 60 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,3 ml'de 1,14 mg sodyum içerir.
Kullanıma hazır kalem içinde ARANESP 80 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,4 ml'de 1,52 mg sodyum içerir.
Kullanıma hazır kalem içinde Aranesp 100 mcg enjeksiyonluk solüsyon
Her kullanıma hazır kalem, 0,5 ml'de 1,90 mg sodyum içerir.
Kullanıma hazır kalem içinde Aranesp 130 mcg enjeksiyonluk çözelti
Her kullanıma hazır kalem 0,65 mL içinde 2,46 mg sodyum içerir.
Kullanıma hazır kalem içinde ARANESP 150 mikrogram enjeksiyonluk çözelti
Her kullanıma hazır kalem, 0,3 ml'de 1,14 mg sodyum içerir.
Kullanıma hazır kalem içinde Aranesp 300 mcg enjeksiyonluk çözelti
Her kullanıma hazır kalem 0,6 ml içinde 2,27 mg sodyum içerir.
Kullanıma hazır kalemde enjeksiyon için Aranesp 500 mcg solüsyonu
Her kullanıma hazır kalem, 1 ml'de 3.79 mg sodyum içerir.
Aranesp 25 mcg flakon içinde enjeksiyonluk çözelti
Her flakon 3.79 mg sodyum içerir.
Aranesp 40 mcg flakon içinde enjeksiyonluk çözelti
Her flakon 3.79 mg sodyum içerir.
Aranesp 60 mcg flakon içinde enjeksiyonluk çözelti
Her flakon 3.79 mg sodyum içerir.
Aranesp 100 mcg flakon içinde enjeksiyonluk çözelti
Her flakon 3.79 mg sodyum içerir.
Şişe içinde enjeksiyon için Aranesp 200 mcg solüsyonu
Her flakon 3.79 mg sodyum içerir.
Şişe içinde enjeksiyon için Aranesp 300 mcg solüsyonu
Her flakon 3.79 mg sodyum içerir.
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakın.
03.0 FARMASÖTİK FORM
Kullanıma hazır şırıngada enjeksiyon (enjeksiyon) için çözelti.
Kullanıma hazır kalemde (SureClick) enjeksiyon (enjeksiyon) için çözelti.
Şişe içinde enjeksiyon (enjeksiyon) için çözelti.
Berrak, renksiz çözelti.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Yetişkinlerde ve pediyatrik hastalarda kronik böbrek yetmezliği (CRI) ile ilişkili semptomatik aneminin tedavisi (bkz. bölüm 4.2).
Kemoterapi alan miyeloid olmayan maligniteleri olan yetişkin hastalarda semptomatik anemi tedavisi.
04.2 Pozoloji ve uygulama yöntemi
ARANESP tedavisi, yukarıdaki endikasyonlarda deneyimli bir hekim tarafından başlatılmalıdır.
Dozaj
Kronik böbrek yetmezliği olan yetişkin ve pediatrik hastalarda semptomatik anemi tedavisi
Aneminin semptomları ve sekelleri yaşa, cinsiyete ve hastalığın genel şiddetine göre değişiklik gösterebilir; bu nedenle her bir hastanın klinik seyri ve koşullarının doktor tarafından değerlendirilmesi gereklidir. ARANESP, hemoglobin konsantrasyonunu 12 g/dl'den (7.5 mmol/l) fazla olmayacak şekilde artırmak için deri altından veya damardan uygulanmalıdır. Hemodiyalize girmeyen hastalarda periferik damarların delinmesini önlemek için deri altı kullanımı tercih edilir.
Hemoglobin konsantrasyonu 12 g/dl'ye (7 , 5 mmol/l) eşit veya altında tutulurken, onaylanmış en düşük Aranesp dozu kullanılarak anemi semptomlarının yeterli kontrolünü sağlamak için hastalar yakından izlenmelidir. Kronik böbrek yetmezliği olan hastalarda artan ARANESP dozlarında dikkatli olunmalıdır.
ARANESP'e zayıf hemoglobin yanıtı olan hastalarda, zayıf yanıtın alternatif nedenleri düşünülmelidir (bkz. bölüm 4.4 ve 5.1).
Hasta içi değişkenlik nedeniyle bazen aynı kişide istenilen hemoglobin seviyesinin üstünde ve altında tek hemoglobin değerleri gözlemlenebilir. Hemoglobinin değişkenliği, 10 g/dl (6,2 mmol/l) ila 12 g/dl (7,5 mmol/l) olan hedef hemoglobin aralığı dikkate alınarak doz yönetimi ile kontrol edilmelidir. g/dl (7.5 mmol/l)'den kaçınılmalıdır; 12 g/dl (7.5 mmol/l) üzerindeki hemoglobin değerleri için uygun doz ayarlaması için kılavuzlar aşağıda verilmiştir. mmol / l) 4 haftalık bir süre boyunca da kaçınılmalıdır. Bu meydana gelirse, dozun ayarlanması gerekecektir.
Aranesp ile tedavi, düzeltme aşaması ve idame aşaması olmak üzere iki aşamaya ayrılır. Talimatlar, yetişkin ve pediatrik hastalar için ayrı olarak sağlanır.
Kronik böbrek yetmezliği olan yetişkin hastalar
Düzeltme aşaması:
Subkutan veya intravenöz uygulama için başlangıç dozu, haftada bir kez tek enjeksiyon olarak 0.45 mcg/kg vücut ağırlığıdır. Alternatif olarak, aşağıdaki başlangıç dozları, diyalize girmeyen hastalara tek bir enjeksiyon olarak deri altından da uygulanabilir: iki haftada bir 0.75 mcg / kg veya ayda bir 1.5 mcg / kg. Hemoglobin artışı yetersizse (dört hafta boyunca 1 g/dl'den (0,6 mmol/l'den az) az), doz yaklaşık %25 oranında artırılmalıdır. Doz artışları 4 haftada bir defadan fazla yapılmamalıdır.
Hemoglobin artışı dört hafta içinde 2 g/dl (1.25 mmol/l) den fazla ise doz yaklaşık %25 oranında azaltılmalıdır. Hemoglobin değeri 12 g/dl'den (7.5 mmol/l) fazla ise doz azaltılması düşünülmelidir. Hemoglobin artmaya devam ederse doz yaklaşık %25 oranında azaltılmalıdır. Doz azaltıldıktan sonra hemoglobin değeri artmaya devam ederse dozda bir azalma gözlenene kadar uygulamaya geçici olarak ara verilmelidir. önceki dozdan yaklaşık %25 daha düşük bir dozda.
Hemoglobin stabilize olana kadar her 1-2 haftada bir ölçülmelidir.Daha sonra hemoglobin daha uzun aralıklarla ölçülebilir.
Bakım aşaması:
Diyaliz hastalarında ARANESP haftada bir veya iki haftada bir tek enjeksiyon olarak devam ettirilebilir. Haftada bir kez Aranesp'ten iki haftada bire geçiş yapan diyaliz hastaları, başlangıçta önceki haftalık dozun iki katına eşdeğer bir doz almalıdır.
Diyalize girmeyen hastalarda ARANESP haftada bir veya iki haftada bir veya ayda bir tek enjeksiyon olarak verilmeye devam edilebilir. İki haftada bir ARANESP ile tedavi edilen hastalarda, hemoglobin konsantrasyonu hedefine ulaştıktan sonra, ARANESP daha önce iki haftada bir verilen dozun iki katı ile başlayarak ayda bir kez subkutan enjeksiyon yoluyla uygulanabilir.
Doz, hedef hemoglobin konsantrasyonunu korumak için gerektiği gibi titre edilmelidir.
Hemoglobini istenilen düzeyde tutmak için doz ayarlaması gerekiyorsa, dozun yaklaşık %25 oranında ayarlanması önerilir.
Hemoglobin artışı dört haftada 2 g/dl (1.25 mmol/l) üzerinde ise artış hızına göre doz yaklaşık %25 oranında azaltılmalıdır. 12 g/dl'den (7.5 mmol) fazla ise / L) doz azaltımı düşünülmeli Hemoglobin yükselmeye devam ederse doz yaklaşık %25 oranında azaltılmalıdır. Doz azaltıldıktan sonra hemoglobin değerinin artmaya devam etmesi durumunda, hemoglobinde bir azalma gözlemlenene kadar uygulamaya geçici olarak ara verilmeli ve böylece dozdan yaklaşık %25 daha düşük bir dozda tedaviye yeniden başlanmalıdır.
Doz veya dozlama programında herhangi bir ayarlamadan sonra, hemoglobin 1-2 haftada bir kontrol edilmelidir.İdame aşamasında doz değişiklikleri iki haftada bir defadan daha sık yapılmamalıdır.
Uygulama yolu değiştirildiğinde, aynı doz kullanılmalı ve hemoglobini istenen seviyede tutmak için dozu ayarlamak için hemoglobin her 1-2 haftada bir kontrol edilmelidir.
Klinik çalışmalar, haftada bir, iki veya üç kez r-HuEPO alan yetişkin hastaların, haftada bir veya iki haftada bir Aranesp'e geçebileceğini göstermiştir. Aranesp'in başlangıç haftalık dozu (mcg/hafta), toplam haftalık r-HuEPO dozunun (IU/hafta) 200'e bölünmesiyle hesaplanabilir. Aranesp'in iki haftada bir uygulanacak başlangıç dozu (iki hafta boyunca mcg), iki haftalık bir süre boyunca uygulanan toplam r-HuEPO dozunun 200'e bölünmesiyle hesaplanabilir. Bireysel değişkenlik göz önüne alındığında, bireysel hasta için optimal terapötik dozu tanımlamak için dozun modüle edilmesi gerekeceği beklenir. r-HuEPO'yu Aranesp ile değiştirirken, hemoglobin 1-2 haftada bir kontrol edilmeli ve aynı uygulama yolu kullanılmalıdır.
Kronik böbrek yetmezliği olan pediatrik popülasyon
Randomize klinik çalışmalarda 1 yaşından küçük pediyatrik hastaların tedavisine ilişkin veri yoktur (bkz. bölüm 5.1).
Düzeltme aşaması:
≥ 1 yaşındaki hastalar için subkutan veya intravenöz uygulama için başlangıç dozu, haftada bir kez tek enjeksiyon olarak 0.45 mcg / kg vücut ağırlığıdır. Alternatif olarak, diyalize girmeyen hastalara iki haftada bir tek subkutan enjeksiyon olarak 0.75 mcg / kg'lık bir başlangıç dozu verilebilir. Hemoglobin artışı yetersizse (dört hafta boyunca 1 g/dl'den (0,6 mmol/l'den az) az), doz yaklaşık %25 oranında artırılmalıdır. Doz artışları dört haftada bir defadan fazla yapılmamalıdır.
Hemoglobin artışı dört haftada 2 g/dl (1.25 mmol/l) üzerinde ise artış hızına göre doz yaklaşık %25 oranında azaltılmalıdır. 12 g/dl'den (7.5 mmol) fazla ise / L) doz azaltımı düşünülmeli Hemoglobin yükselmeye devam ederse doz yaklaşık %25 oranında azaltılmalıdır. Doz azaltıldıktan sonra hemoglobin değerinin artmaya devam etmesi durumunda, hemoglobinde bir azalma gözlemlenene kadar uygulama geçici olarak durdurulmalı, böylece dozdan yaklaşık %25 daha düşük bir dozda tedaviye yeniden başlanmalıdır.
Hemoglobin stabilize olana kadar her 1-2 haftada bir ölçülmelidir.Daha sonra hemoglobin daha uzun aralıklarla ölçülebilir.
Pediyatrik hastalarda ayda bir kez ARANESP kullanılarak aneminin düzeltilmesi çalışılmamıştır.
Bakım aşaması:
≥ 1 yaşındaki pediyatrik hastalarda, idame aşamasında, ARANESP haftada bir veya iki haftada bir tek enjeksiyon olarak devam ettirilebilir. Hastalar, yaşlı hastalara kıyasla hemoglobin düzeylerini yaşlandırdı. Haftada bir kez Aranesp'ten iki haftada bire geçiş yapan diyaliz hastaları, başlangıçta önceki haftalık dozun iki katına eşdeğer bir doz almalıdır.
3-11 yaş arası diyaliz olmayan hastalarda, iki haftada bir hedef hemoglobin konsantrasyonuna ulaşıldığında, ARANESP daha önce uygulanan dozun iki katı ile başlayarak ayda bir kez, iki haftada bir deri altı enjeksiyon yoluyla uygulanabilir.
Pediyatrik hastalardaki klinik veriler, haftada iki veya üç kez r-HuEPO alan hastaların haftada bir kez Aranesp'e geçebileceğini ve haftada bir kez r-HuEPO alan hastaların haftada bir kez r-HuEPO uygulamasına geçebileceğini göstermiştir. iki hafta. Aranesp'in ilk haftalık pediatrik dozu (mcg/hafta), toplam haftalık r-HuEPO dozunun (IU/hafta) 240'a bölünmesiyle hesaplanabilir. Aranesp'in iki haftada bir başlangıç dozu (mcg / iki haftada bir), iki hafta boyunca uygulanan toplam kümülatif r-HuEPO dozunun 240'a bölünmesiyle hesaplanabilir. Hasta için optimal terapötik doz r-HuEPO'yu Aranesp ile değiştirirken, hemoglobin 1-2 haftada bir kontrol edilmeli ve aynı uygulama yolu kullanılmalıdır.
Doz, hedef hemoglobin konsantrasyonunu korumak için gerektiği gibi titre edilmelidir.
Hemoglobini istenilen düzeyde tutmak için doz ayarlaması gerekiyorsa, dozun yaklaşık %25 oranında ayarlanması önerilir.
Dört haftada hemoglobin artışı 2 g/dl'den (1.25 mmol/l) fazla ise artış hızına göre doz yaklaşık %25 oranında azaltılmalıdır. 12 g/dl'den (7.5 mmol) fazla ise / l), doz azaltılması düşünülmelidir.Hemoglobin değeri artmaya devam ederse, doz yaklaşık %25 oranında azaltılmalıdır.Dozda bir azalma, hemoglobin değeri artmaya devam eder, uygulamanın geçici olarak durdurulması gerekecektir. Hemoglobinde bir azalma gözlemlenene kadar, tedaviye önceki dozdan yaklaşık %25 daha düşük bir dozda yeniden başlanır.
ARANESP tedavisi sırasında diyalize başlayan hastalar, hemoglobin düzeylerinin yeterli kontrolü için yakından izlenmelidir.
Doz veya dozlama programında herhangi bir ayarlamadan sonra, hemoglobin 1-2 haftada bir kontrol edilmelidir.İdame aşamasında doz değişiklikleri iki haftada bir defadan daha sık yapılmamalıdır.
Uygulama yolu değiştirildiğinde, aynı doz kullanılmalı ve hemoglobini istenen seviyede tutmak için dozu ayarlamak için hemoglobin her 1-2 haftada bir kontrol edilmelidir.
Kanser hastalarında kemoterapinin neden olduğu semptomatik aneminin tedavisi
ARANESP anemik hastalara deri altından uygulanmalıdır (örn. hemoglobin konsantrasyonu ≤ 10 g/dl (6,2 mmol/l), hemoglobin değerini 12 g/dl'den (7,5 mmol/l) fazla olmayacak şekilde artırmak için. Anemi belirtileri ve sekelleri yaşa, cinsiyete ve hastalığın genel şiddetine göre değişebileceğinden, her hastanın klinik seyri ve durumunun hekim tarafından değerlendirilmesi gerekir.
Hasta içi değişkenlik nedeniyle bazen aynı kişide istenilen hemoglobin seviyesinin üstünde ve altında tek hemoglobin değerleri gözlemlenebilir. Hemoglobinin değişkenliği, 10 g/dl (6,2 mmol/l) ila 12 g/dl (7,5 mmol/l) olan hedef hemoglobin aralığı dikkate alınarak doz yönetimi ile kontrol edilmelidir.Kalıcı hemoglobin değerlerinden kaçınmak gerekir. 12 g/dl (7.5 mmol/l) üzeri; hemoglobin değerlerinin 12 g/dl (7,5 mmol/l) üzerinde olması durumunda uygun doz ayarlaması için endikasyonlar aşağıdadır.
Önerilen başlangıç dozu, üç haftada bir verilen 500 mikrogram (6.75 mikrogram/kg) veya haftada bir kez 2.25 mikrogram/kg vücut ağırlığıdır. Dokuz hafta sonra hastanın klinik yanıtı (yorgunluk, hemoglobin yanıtı) yetersizse, devam eden tedavi etkili olmayabilir.
ARANESP tedavisi kemoterapi kürünün bitiminden yaklaşık 4 hafta sonra kesilmelidir.
Bireysel hasta için tedavi hedefine ulaşıldığında, hemoglobini anemi semptomlarını kontrol eden bir seviyede tutmak için onaylanmış en düşük Aranesp dozunun kullanılmasını sağlamak için doz %25-50 oranında azaltılmalıdır.500 mcg, 300 mcg ve 150 mcg arasında uygun doz titrasyonu düşünülmelidir.
Hastalar yakından izlenmeli, hemoglobin 12 g/dl'yi (7.5 mmol/l) aşıyorsa doz yaklaşık %25-50 azaltılmalı, hemoglobin düzeyleri 13 g/dl'yi (8 , 1 mmol/l) aşarsa ARANESP tedavisi yapılmalıdır. Hemoglobin seviyesi 12 g/dl veya altına (7.5 mmol/l) düştükten sonra tedavi bir önceki dozdan yaklaşık %25 daha düşük bir dozda yeniden başlatılmalıdır.
4 haftalık periyotta hemoglobin artışı 2 g/dl'den (1.25 mmol/l) fazla ise doz %25-50 azaltılmalıdır.
Uygulama yöntemi
Aranesp 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300, 500 mcg kullanıma hazır şırınga içinde enjeksiyonluk çözelti
ARANESP, pozolojide açıklandığı gibi deri altından veya damardan uygulanır.
Enjeksiyon bölgesindeki rahatsızlığı en aza indirmek için enjeksiyon yerlerini değiştirin ve yavaşça enjekte edin. ARANESP kullanıma hazır şırıngalar içinde sunulur.
Aranesp 10, 15, 20, 30, 40, 50, 60, 80, 100, 130, 150, 300, 500 mcg kullanıma hazır dolu kalemde enjeksiyon için solüsyon
Kullanıma hazır kalem içinde ARANESP sadece subkutan uygulama içindir.
Enjeksiyon bölgesindeki rahatsızlığı en aza indirmek için alternatif enjeksiyon bölgeleri.
Aranesp kullanıma hazır, kullanıma hazır bir kalemle sağlanır.
Aranesp 25, 40, 60, 100, 200, 300 mcg flakon içinde enjeksiyonluk çözelti
ARANESP, pozolojide açıklandığı gibi deri altından veya damardan uygulanır.
Enjeksiyon bölgesindeki rahatsızlığı en aza indirmek için enjeksiyon yerlerini değiştirin ve yavaşça enjekte edin.
ARANESP bir flakon içinde kullanıma hazır olarak sağlanır.
Kullanım, elleçleme ve imha talimatları bölüm 6.6'da verilmiştir.
04.3 Kontrendikasyonlar
Etkin maddeye veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
Kontrolsüz hipertansiyon.
04.4 Özel uyarılar ve uygun kullanım önlemleri
Genel
Eritropoezi uyarıcı ajanların (ESA) izlenebilirliğini geliştirmek için, uygulanan ESA'nın ticari adı hasta kaydına açıkça kaydedilmelidir (veya rapor edilmelidir).
Özellikle ARANESP tedavisinin başlangıcında olmak üzere tüm hastalarda kan basıncı izlenmelidir.Eğer uygun önlemler alınarak kan basıncının kontrol edilmesi zorsa, ARANESP uygulaması azaltılarak veya durdurularak hemoglobin düşürülebilir (bkz. paragraf 4.2). ARANESP ile tedavi edilen KBY hastalarında hipertansif kriz, hipertansif ensefalopati ve nöbet dahil olmak üzere şiddetli hipertansiyon vakaları gözlenmiştir.
Etkili eritropoezi sağlamak için, tedavi öncesi ve sırasında tüm hastalarda demir depoları kontrol edilmelidir ve ek demir tedavisi gerekebilir.
ARANESP ile tedaviye yanıt alınamaması, neden olan faktörlerin araştırılmasına yol açmalıdır.Demir, folik asit veya B12 vitamini eksiklikleri ESA'ların etkinliğini azaltır ve bu nedenle düzeltilmelidir. Eşzamanlı enfeksiyonlar, inflamatuar veya travmatik ataklar, gizli kan kaybı, hemoliz, şiddetli alüminyum zehirlenmesi, altta yatan hematolojik hastalıklar veya kemik iliği fibrozu, eritropoietik yanıtı tehlikeye atabilir. Retikülosit sayımı değerlendirmenin bir parçası olarak düşünülmelidir. Tipik yanıtsızlık nedenleri dışlanmışsa ve hasta retikülositopeni ile başvuruyorsa kemik iliği incelemesi düşünülmeli, kemik iliği PRCA tanısıyla uyumluysa antikor testi -eritropoietin yapılmalıdır.
Aranesp de dahil olmak üzere ESA tedavisi ile ilişkili olarak eritropoietin antikorlarının nötralize edilmesinin neden olduğu saf kırmızı hücre aplazisi bildirilmiştir. Bu bulgu ağırlıklı olarak subkutan yolla tedavi edilen kronik böbrek yetmezliği (CRI) olan hastalarda bildirilmiştir. Bu antikorların tüm eritropoietik proteinlerle çapraz reaksiyona girdiği gösterilmiştir ve eritropoietine karşı nötralize edici antikorların varlığından şüphelenilen veya doğrulanan hastalarda ARANESP tedavisi başlatılmamalıdır (bkz. bölüm 4.8).
Hemoglobinde paradoksal bir azalma ve düşük retikülosit sayılarıyla ilişkili şiddetli aneminin başlaması, epoetin tedavisinin derhal kesilmesine ve anti-eritropoietin antikor testinin yürütülmesine yol açmalıdır. Epoetinler birlikte kullanıldığında interferon ve ribavirin ile tedavi edilen hepatit C hastalarında vakalar bildirilmiştir. Epoetinler, hepatit C ile ilişkili aneminin tedavisi için onaylanmamıştır.
Aranesp ile yapılan tüm çalışmalarda aktif karaciğer hastalığı bir dışlama kriteriydi, bu nedenle karaciğer fonksiyon bozukluğu olan hastalarda veri mevcut değildir. Darbepoetin alfa ve r-HuEPO'nun başlıca eliminasyon yolunun karaciğer olduğu düşünüldüğünden, ARANESP karaciğer hastalığı olan hastalarda dikkatli kullanılmalıdır.
Orak hücre anemisi olan hastalarda ARANESP dikkatli kullanılmalıdır.
ARANESP'in sağlıklı kişiler tarafından yanlış kullanımı hematokritte aşırı artışa neden olabilir. Bu, deneği hemen hayati tehlikeye sokan kardiyovasküler komplikasyonlarla ilişkilendirilebilir.
Kullanıma hazır şırınga veya kullanıma hazır kalemin iğne kapağı, alerjik reaksiyonlara neden olabilen kuru doğal kauçuk (bir lateks türevi) içerir.
ARANESP epilepsili hastalarda dikkatli kullanılmalıdır. ARANESP alan hastalarda nöbetler bildirilmiştir.
Bu tıbbi ürün, doz başına 1 mmol'den (23 mg) daha az sodyum içerir, yani esasında sodyum içermez.
Kronik böbrek yetmezliği olan hastalar
Kronik böbrek yetmezliği olan hastalarda hemoglobin, bölüm 4.2'de önerilen hedef hemoglobin konsantrasyonunun üst sınırını aşmayacak bir seviyede tutulmalıdır.Klinik çalışmalarda ölüm, ciddi kardiyovasküler veya kardiyovasküler olaylar riskinde artış gözlenmiştir. 12 g / dl'den (7.5 mmol / l) daha yüksek bir hemoglobin değerine ulaşmayı amaçlayan ESA uygulanması durumunda inme ve damar yollarının trombozu dahil.
Kümülatif yüksek epoetin dozları artmış mortalite riski, ciddi kardiyovasküler ve serebrovasküler olaylar ile ilişkili olabileceğinden, kronik böbrek yetmezliği olan hastalarda artan ARANESP dozlarında dikkatli olunmalıdır. zayıf yanıt için alternatif nedenler düşünülmelidir (bkz. bölüm 4.2 ve 5.1).
Kontrollü klinik deneyler, hemoglobin konsantrasyonu anemi semptomlarını kontrol etmek ve kan transfüzyonlarından kaçınmak için gerekli seviyenin üzerine çıktığında epoetinlerin uygulanmasına atfedilebilecek önemli bir fayda göstermemiştir.
Serum ferritin değerleri 100 mcg/L'nin altında veya transferrin satürasyonu %20'nin altında olan tüm hastalarda ek demir tedavisi önerilir.
ARANESP tedavisi sırasında serum potasyum seviyeleri düzenli olarak izlenmelidir. ARANESP alan bazı hastalarda potasyumda yükselmeler bildirilmiştir, ancak tedavi ile korelasyon kurulmamıştır. Yüksek veya artan potasyum seviyeleri gözlemlenirse, bu seviye düzeltilene kadar ARANESP uygulamasının kesilmesi düşünülmelidir.
Kanserli hastalar
Tümör ilerlemesi üzerindeki etkisi
Epoetinler, öncelikle kırmızı kan hücrelerinin üretimini uyaran büyüme faktörleridir. Eritropoietin reseptörleri, çeşitli kanser hücrelerinin yüzeyinde eksprese edilebilir.Tüm büyüme faktörlerinde olduğu gibi, epoetinlerin de tümörlerin büyümesini uyarabileceği endişesi vardır. Birkaç kontrollü klinik çalışmada, epoetinlerin, malignitelerle ilişkili anemisi olan hastalarda genel sağkalımı iyileştirdiği veya tümör progresyonu riskini azalttığı gösterilmemiştir.
ARANESP ve diğer ESA'ların uygulandığı kontrollü klinik çalışmalarda aşağıdakiler gösterilmiştir:
• ESA'lar 14 g/dl'den (8 , 7 mmol/l) daha yüksek bir hedef hemoglobin değerine ulaşmak için uygulandığında, radyoterapi ile tedavi edilen ilerlemiş baş ve boyun kanserli hastalarda tümör ilerlemesine kadar geçen sürenin kısaltılması; Bu hasta popülasyonunda ESA kullanımı endike değildir.
• 12-14 g / dl (7.5-8.7 mmol / l) hedef hemoglobin değerine ulaşmak için uygulandığında, kemoterapi ile tedavi edilen metastatik meme kanserli hastalarda 4 ayda hastalığın ilerlemesine atfedilen genel sağkalımda azalma ve ölümlerde artış.
• Kemoterapi veya radyoterapi ile tedavi edilmeyen aktif malign neoplazmalı hastalarda 12 g / dl (7.5 mmol / l) hemoglobin değerine ulaşmayı amaçlayan pozoloji durumunda artan ölüm riski. Bu hasta popülasyonunda ESA kullanımı endike değildir.
Yukarıdakilere dayanarak, bazı klinik durumlarda kanser hastalarında aneminin tedavisi için kan transfüzyonu tercih edilen tedavi olmalıdır.Rekombinant eritropoietin uygulama kararı, bireysel hastanın katılımıyla fayda-risk oranının değerlendirilmesine dayanmalıdır. ve spesifik klinik bağlamı dikkate almalıdır.Bu değerlendirmede dikkate alınacak faktörler, kanserin tipini ve evresini, aneminin derecesini, yaşam beklentisini, hastanın tedavi edildiği ortamı ve hastanın tercihlerini içermelidir (bkz. bölüm 5.1).
Solid tümörleri veya lenfoproliferatif neoplazmaları olan hastalarda, hemoglobin değeri 12 g/dl'yi (7.5 mmol/l) aşarsa, tromboembolik olay riskini en aza indirmek için bölüm 4.2'de açıklanan doz ayarlamasına kesinlikle uyulmalıdır. Trombosit sayısı ve hemoglobin düzeyi düzenli aralıklarla kontrol edilmelidir.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Bugüne kadar elde edilen klinik sonuçlar, darbepoetin alfa'nın diğer maddelerle herhangi bir etkileşimi olduğunu göstermez. Bununla birlikte, "siklosporin ve takrolimus gibi kırmızı kan hücrelerine önemli ölçüde bağlanan maddelerle etkileşim" olasılığı vardır. ARANESP bu tedavilerden biriyle birlikte uygulanırsa, ikincisinin kan seviyeleri izlenmeli ve dozları ayarlanmalıdır. Hemoglobin artışına göre.
04.6 Hamilelik ve emzirme
Gebelik
ARANESP'in gebe kadınlarda kullanımına ilişkin yeterli ve iyi kontrollü çalışma bulunmamaktadır.
Hayvanlar üzerinde yapılan çalışmalar, hamilelik, embriyonal / fetal gelişim, doğum veya doğum sonrası gelişim üzerinde doğrudan zararlı etkiler göstermemiştir. Doğurganlıkta herhangi bir bozulma gözlenmedi.
ARANESP hamile kadınlara reçete edilirken dikkatli olunmalıdır.
Aranesp tedavisi görürken hamile kalan kadınların Amgen'in Gebelik Gözetim Programına kaydolmaları teşvik edilir. İletişim bilgileri Paket Broşürünün 6. bölümünde verilmiştir.
Besleme zamanı
ARANESP'in insan sütüne geçip geçmediği bilinmemektedir. Bebekler için bir risk göz ardı edilemez. Emzirmenin durdurulup durdurulmayacağına veya ARANESP tedavisinin durdurulup durdurulmayacağına/tedaviden kaçınılmasına karar verilmelidir.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
ARANESP'in araç veya makine kullanma yeteneği üzerinde etkisi yoktur veya ihmal edilebilir düzeydedir.
04.8 İstenmeyen etkiler
Güvenlik profilinin özeti
ARANESP kullanımıyla ilişkili tanımlanmış advers reaksiyonlar hipertansiyon, felç, tromboembolik olaylar, konvülsiyonlar, alerjik reaksiyonlar, döküntü/eritem ve saf kırmızı hücre aplazisidir (PRCA); bkz. bölüm 4.4.
ARANESP'in subkutan enjeksiyon olarak verildiği çalışmalarda, enjeksiyon bölgesi ağrısının tedaviye atfedilebileceği düşünülmüştür. Enjeksiyon bölgesi rahatsızlığı genellikle hafif ve geçiciydi ve ağırlıklı olarak ilk enjeksiyondan sonra meydana geldi.
Advers reaksiyon tablosu
Advers reaksiyonların insidansı aşağıda sistem organ sınıfına ve sıklık sınıfına göre sunulmuştur Sıklıklar şu şekilde tanımlanmıştır: Çok yaygın (≥ 1/10); yaygın (≥ 1/100,
Veriler, bu popülasyonlardaki farklı advers reaksiyon profillerini yansıtmak için kronik böbrek yetmezliği hastaları ve kanser hastaları için ayrı ayrı sunulmuştur.
Kronik böbrek yetmezliği olan hastalar
Kontrollü klinik çalışmalardan sunulan veriler, Aranesp ile tedavi edilen 766 ve r-HuEPO ile tedavi edilen 591 hasta olmak üzere 1.357 hastayı içermektedir. Aranesp grubunda, hastaların %83'ü diyaliz tedavisi almış ve %17'si diyalize girmemiştir.İlave bir klinik çalışmada inme advers reaksiyon olarak tanımlanmıştır (TREAT, bakınız bölüm 5.1).
Kontrollü klinik çalışmalarda ve pazarlama sonrası kullanımda advers reaksiyonların insidansı aşağıdaki gibidir:
* "Seçilen advers reaksiyonların tanımı" bölümüne bakın
Kanserli hastalar
Advers reaksiyonlar, toplam 2.112 hastayı (1.200 Aranesp, 912 plasebo) içeren yedi randomize, çift kör, plasebo kontrollü çalışmadan toplanan verilere dayanarak belirlendi. Klinik deneyler, katı tümörleri (örn. akciğer, meme, kolon ve yumurtalık kanserleri) ve lenfoid maligniteleri (örn. lenfoma, multipl miyelom) olan hastaları kaydetmiştir.
Kontrollü klinik çalışmalarda ve pazarlama sonrası kullanımda advers reaksiyonların insidansı aşağıdaki gibidir:
* "Seçilen advers reaksiyonların tanımı" bölümüne bakın
Seçilmiş advers reaksiyonların tanımı
Kronik böbrek yetmezliği olan hastalar
TREAT'de, KBY hastalarında inme yaygın olarak bildirilmiştir (bkz. bölüm 5.1).
İzole vakalarda, ağırlıklı olarak subkutan olarak tedavi edilen CRF hastalarında, ARANESP tedavisiyle ilişkili eritropoietin nötrleştirici antikorları ile saf kırmızı hücre aplazisi (PRCA). PRCA teşhisi konulursa, ARANESP tedavisi kesilmeli ve hastalar başka bir rekombinant eritropoietik protein ile tedavi edilmemelidir (bkz. bölüm 4.4).
Klinik çalışma verilerine dayanarak, tüm aşırı duyarlılık reaksiyonlarının sıklığı, KBY hastalarında çok yaygın olarak tanımlandı. Anafilaktik reaksiyon, anjiyoödem, alerjik bronkospazm, deri döküntüsü ve ürtiker dahil olmak üzere darbepoetin alfa kullanımıyla ilişkili ciddi aşırı duyarlılık reaksiyonları bildirilmiştir.
Darbepoetin alfa alan hastalarda nöbetler bildirilmiştir (bkz. bölüm 4.4).
Klinik çalışma verilerine dayanarak, CRF hastalarında sıklık yaygın olmayan olarak tanımlanmıştır.
Kanserli hastalar
Pazarlama sonrası kullanım sırasında kanser hastalarında hipertansiyon gözlenmiştir (bkz. bölüm 4.4) Klinik çalışma verilerine göre, sıklık kanser hastalarında yaygın olarak ve plasebo ile tedavi edilen gruplarda da yaygın olarak tanımlanmıştır.
Pazarlama sonrası kullanım sırasında kanser hastalarında aşırı duyarlılık reaksiyonları gözlenmiştir.Klinik çalışma verilerine göre, kanser hastalarında sıklık çok yaygın olarak tanımlanmıştır.Aşırı duyarlılık reaksiyonları çok yaygındı.plasebo gruplarında da.Şiddetli raporlar vardır. anafilaktik reaksiyon, anjiyoödem, alerjik bronkospazm, deri döküntüsü ve ürtiker dahil olmak üzere darbepoetin alfa kullanımına bağlı aşırı duyarlılık reaksiyonları.
Pazarlama sonrası kullanım sırasında darbepoetin alfa alan hastalarda nöbetler bildirilmiştir (bkz. bölüm 4.4) Klinik çalışma verilerine göre, kanser hastalarında sıklık yaygın olmayan olarak tanımlanmıştır Plasebo gruplarında nöbetler yaygındı.
Kronik böbrek yetmezliği olan pediatrik popülasyon
IRC'deki tüm pediyatrik klinik çalışmalarda, pediyatrik hastalarda, daha önce yetişkin hastalarda bildirilenden daha fazla advers reaksiyon tanımlanmamıştır (bkz. bölüm 5.1).
Şüpheli advers reaksiyonların raporlanması
Tıbbi ürünün ruhsatlandırılmasından sonra şüpheli advers reaksiyonların raporlanması, tıbbi ürünün yarar/risk oranının sürekli olarak izlenmesine olanak sağladığı için önemlidir.Sağlık profesyonellerinden, herhangi bir şüpheli advers reaksiyonu ulusal raporlama sistemine bildirmeleri istenir.
04.9 Doz aşımı
Tek veya çoklu dozlarda güvenle uygulanabilecek maksimum ARANESP miktarı belirlenmemiştir. Hemoglobin dikkatle izlenmezse ve doz uygun şekilde ayarlanmazsa ARANESP tedavisi polisitemi ile sonuçlanabilir Aranesp ile doz aşımını takiben şiddetli hipertansiyon vakaları gözlenmiştir (bkz. bölüm 4.4).
Polisitemi durumunda, ARANESP geçici olarak askıya alınmalıdır (bkz. bölüm 4.2). Klinik olarak endike ise flebotomi yapılabilir.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: Antianemik müstahzarlar, diğer antianemik müstahzarlar. ATC kodu: B03XA02.
Hareket mekanizması
Bir endojen glikoprotein hormonu olan insan eritropoietini, kemik iliğindeki eritroid progenitör hücreler üzerindeki eritropoietin reseptörü ile spesifik etkileşim yoluyla eritropoezin ana düzenleyicisidir. Eritropoietin üretimi birincil olarak meydana gelir ve doku oksijenasyonundaki değişikliklere yanıt olarak böbrekte düzenlenir.Kronik böbrek yetmezliği hastalarında endojen eritropoietin üretimi azalır ve bu hastalarda aneminin başlıca nedeni eritropoietin eksikliğidir. Kemoterapi alan kanser hastalarında anemi etiyolojisi multifaktöriyeldir. Bu hastalarda, eritropoietin eksikliği ve eritroid progenitör hücrelerin endojen eritropoietin'e verdiği yanıtın azalması, anemiye önemli ölçüde katkıda bulunan faktörlerdir.
farmakodinamik etkiler
Darbepoetin alfa, endojen hormonla aynı mekanizma ile eritropoezi uyarır. Darbepoetin alfa, N-ucuna bağlı beş karbonhidrat zincirine sahipken, endojen hormon ve rekombinant insan eritropoietinlerinde (r-HuEPO) üç tane bulunur. Ek karbonhidrat kalıntıları moleküler düzeyde endojen hormon üzerinde bulunanlardan ayırt edilemezler Daha yüksek karbonhidrat içeriği nedeniyle darbepoetin alfa, r-HuEPO'dan daha uzun bir terminal yarı ömre sahiptir ve bu nedenle daha büyük aktiviteye sahiptir. canlıda. Bu moleküler modifikasyonlara rağmen darbepoetin alfa, eritropoietin reseptörü için çok yüksek bir özgüllük sağlar.
Klinik etkinlik ve güvenlik
Kronik böbrek yetmezliği olan hastalar
İki klinik çalışmada, ESA'lar düşük hemoglobin düzeylerinden (13.5 g/dL (8 , 4 mmol/l) ve 11.3 g/dl'ye (7.1) kıyasla daha yüksek hemoglobin düzeylerine ulaşmak için uygulandığında, CRF hastalarının ölüm ve ciddi kardiyovasküler olay riskleri daha yüksekti. mmol / l); 14 g / dl (8.7 mmol / l) ve 10 g / dl (6,2 mmol / l)).
Diyalize girmeyen KBY hastalarında iki haftada bir ve ayda bir dozlama programlarını karşılaştıran randomize, çift kör, düzeltme çalışmasında (n = 358), ayda bir kez darbepoetin alfa dozu aneminin düzeltilmesiyle sonuçlanmıştır. Hemoglobin düzeltmesi (≥ 10.0 g / dL ve başlangıca göre ≥ 1.0 g / dL artış) elde etmek için medyan süre (çeyrek 1, çeyrek 3) her iki haftada bir için 5 haftaydı ( 3,7 hafta) ve ayda bir (3,9 hafta) dozlama. Değerlendirme döneminde (29 - 33. haftalar), ortalama haftalık eşdeğer doz (%95 GA) iki haftada bir kolunda 0.20 (0.17 - 0.24) mcg/kg ve kolda 0.27 (0.23 - 0.32) mcg/kg idi. ayda bir kol.
Tip 2 diyabetli ve hemoglobin düzeyleri ≤ 11 g/dL olan 4.038 diyaliz olmayan CRF hastasının yer aldığı randomize, çift kör, plasebo kontrollü bir çalışmada (TREAT), hastalara hedef hemoglobin düzeyleri olan 13 g/dL'ye ulaşmak için darbepoetin alfa tedavisi uygulandı. dl veya plasebo (9 g / dl'nin altındaki hemoglobin seviyelerinde darbepoetin alfa ile iyileşme tedavisi ile). Çalışma, tüm nedenlere bağlı ölüm veya kardiyovasküler morbidite riskinde azalma olduğunu gösterme birincil amacını karşılamadı (plaseboya karşı darbepoetin alfa; HR 1.05, %95 GA (0.94-1.17)), o Tüm nedenlere bağlı ölüm oranı o Son aşama böbrek hastalığı (SDBY) (plaseboya karşı darbepoetin alfa; HR 1.06, %95 GA (0.95-1.19)). "Bileşik son noktanın bireysel bileşen analizi, aşağıdaki HR'yi (%95 GA): ölüm 1.05 (0.92-1.21) ), konjestif kalp yetmezliği (KKY) 0,89 (0,74-1,08), miyokard enfarktüsü (MI) 0,96 (0,75-1,23), inme 1,92 (1,38-2,68), miyokard iskemisi nedeniyle hastaneye yatış 0,84 (0,55-1,27), ESRD 1,02 (0,87) -1.18).
ESA ile yapılan klinik çalışmaların havuzlanmış post-hoc analizleri, kronik böbrek yetmezliği olan hastalarda (diyalizde, diyalizde değil, diyabetik, diyabetik olmayan) gerçekleştirilmiştir. Diyabet veya diyaliz durumundan bağımsız olarak, daha yüksek kümülatif ESA dozları ile ilişkili tüm nedenlere bağlı ölüm, kardiyovasküler ve serebrovasküler olayların tahmini riskinde artış yönünde bir eğilim vardı (bkz. bölüm 4.2 ve 4.4).
Pediatrik popülasyon
Randomize bir klinik çalışmada, 2 ila 18 yaşları arasında, kronik böbrek hastalığı olan, diyalizde olan veya olmayan, anemik (hemoglobin) 114 pediyatrik hasta
1 ila 18 yaşları arasında diyaliz tedavisi gören veya diyaliz almayan 124 pediyatrik kronik böbrek hastalığı hastası üzerinde yapılan bir klinik çalışmada, epoetin alfa üzerinde stabil olan hastalar, doz dönüştürme oranı kullanılarak haftada bir (deri altı) veya intravenöz olarak darbepoetin alfa almak üzere randomize edilmiştir. 238: 1 veya aynı doz, program ve uygulama yolunda epoetin alfa tedavisine devam edin. Birincil etkinlik son noktası [başlangıç ve değerlendirme dönemi (21-28. hafta) arasındaki hemoglobin seviyelerindeki değişiklik] iki grup arasında benzerdi.Başlangıçta rHuEPO ve darbepoetin alfa için ortalama hemoglobin seviyeleri 11, 1 (SD 0.7) g / idi. Sırasıyla dL ve 11.3 (SD 0.6) g/dL rHuEPO ve darbepoetin alfa için 28. haftada ortalama hemoglobin seviyeleri sırasıyla 11.1 (SD 1.4) g/dl ve 11.1 (SD 1.1) g/dl idi.
Kronik böbrek hastalığı olan 319 pediyatrik hastayı içeren bir Avrupa gözlemsel kayıt çalışmasında (13 (% 4,1) yaşında)
Bu çalışmalarda, pediyatrik hastalar için güvenlilik profili ile yetişkin hastalar için daha önce bildirilenler arasında anlamlı bir farklılık tanımlanmamıştır (bkz. bölüm 4.8).
Kanserli ve kemoterapi gören hastalar
Platin bazlı kemoterapi alan 314 akciğer kanseri hastasının prospektif, randomize, çift kör, plasebo kontrollü bir çalışmasında, transfüzyon ihtiyacında önemli bir azalma bulundu (p
Klinik çalışmalar darbepoetin alfa'nın toplam dozu artırmaya gerek kalmadan 3 haftada bir, iki haftada bir veya haftada bir tek enjeksiyon olarak verildiğinde benzer etkinliğe sahip olduğunu göstermiştir.
ARANESP tedavisinin kemoterapi gören hastalarda transfüzyon ihtiyacını azaltmada 3 haftada bir uygulanmasının tolere edilebilirliği ve etkinliği, randomize, çift kör, uluslararası bir çalışmada değerlendirilmiştir.Bu çalışma 705 hastada yapılmıştır. Hastalar 3 haftada bir 500 mcg veya haftada bir 2,25 mcg/kg ARANESP almak üzere randomize edilmiştir.Her iki grupta da doz önceki doza göre %40 azaltılmıştır (örn. ilk doz azaltımı, hemoglobinde 14 günde 1 g/dl'den fazla artış olması durumunda 3 haftada bir grupta 300 mcg'ye ve haftada bir grupta 1.35 mcg/kg'a düşürüldü. . Her 3 haftada bir grupta, hastaların %72'sinde doz azaltılması gerekmiştir. Haftada bir kez grubunda, hastaların %75'inde doz azaltılması gerekmiştir. Bu çalışma, her 3 haftada bir 500 mcg'lik dozlamanın, 5. hafta ile tedavinin sonu arasında en az bir transfüzyon gerektiren hastaların insidansı açısından haftada bir dozla karşılaştırılabilir olduğunu göstermektedir.
Lenfoproliferatif neoplazmaları olan ve kemoterapi gören 344 anemik hastada prospektif, randomize, çift kör, plasebo kontrollü bir çalışmada, transfüzyon ihtiyacında önemli bir azalma ve hemoglobin yanıtında bir iyileşme bulundu (p
Eritropoietin, öncelikle kırmızı kan hücrelerinin üretimini uyaran bir büyüme faktörüdür.Eritropoietin reseptörleri, çeşitli kanser hücrelerinin yüzeyinde eksprese edilebilir.
Sağkalım ve tümör ilerlemesi, toplam 2.833 hastayı içeren beş büyük kontrollü klinik çalışmada değerlendirildi; bunlardan dördü plasebo kontrollü ve çift kör çalışmalardı ve biri açık etiketliydi. Bu çalışmalardan ikisi kemoterapi ile tedavi edilen hastaları kaydetmiştir. İki çalışmada hedef hemoglobin konsantrasyonu 13 g/dL'nin üzerindeydi; kalan üç çalışmada ise 12-14 g/dl olmuştur. Açık etiketli çalışmada, rekombinant insan eritropoietinleri ile tedavi edilen hastalar ile kontrol hastaları arasında genel sağkalımda hiçbir farklılık gözlenmemiştir. Dört plasebo kontrollü çalışmada, genel sağkalım için tehlike oranları kontrol grubu lehine 1.25 ila 2.47 arasında değişmiştir. Bu çalışmalar, kontrollerle karşılaştırıldığında, çeşitli yaygın tümör tipleri ile ilişkili anemisi olan ve rekombinant insan eritropoietini alan hastalarda mortalitede sürekli ve açıklanamayan istatistiksel olarak anlamlı bir artış gösterdi. Bu çalışmalarda genel sağkalım sonucu, rekombinant insan eritropoietini ile tedavi edilen hastalar ile kontrol grubundakiler arasındaki tromboz insidansı ve ilişkili komplikasyonlar arasındaki farka dayanarak tatmin edici bir şekilde açıklanamadı.
9.000'den fazla kanser hastasını içeren 57 klinik çalışmanın sistematik bir analizi de yapılmıştır.Genel sağkalım verilerinin meta-analizi, Kontroller lehine 1.08'lik bir Tehlike Oranı nokta tahmini gösterdi (%95 CI: 0.99-1.18; 42 çalışmalar ve 8.167 hasta).
Rekombinant insan eritropoietini ile tedavi edilen hastalarda tromboembolik olay riskinde artış (RR 1.67, %95 GA: 1.35-2.06, 35 çalışma ve 6.769 hasta) gözlenmiştir. Bu nedenle, rekombinant insan eritropoietini ile tedavi edilen kanser hastalarında önemli zarar olabileceğini düşündüren tutarlı kanıtlar vardır. Analiz edilen verilere bu özelliklere sahip az sayıda hasta dahil edildiğinden, hemoglobin konsantrasyonlarının 13 g/dl'nin altında olması için kemoterapi gören kanser hastalarına rekombinant insan eritropoietin uygulamasına bu sonuçların ne ölçüde uygulanabilir olduğu belirsizdir.
Farklı epoetinler kullanan 53 kontrollü klinik araştırmaya katılan 13.900'den fazla kanser hastasında (kemoterapi, radyo, kemoradio veya terapisiz) bireysel hasta verilerinin bir analizi de yapıldı. Genel sağkalım verilerinin meta-analizi, kontroller lehine 1.06'lık bir Tehlike Oranı (%95 GA: 1.00-1.12; 53 çalışma ve 13.933 hasta) ve kemoterapi alan kanser hastaları için 1.04'lük bir Tehlike Oranı nokta tahmini üretti ( %95 GA: 0.97-1.11; 38 çalışma ve 10.441 hasta) Meta-analiz ayrıca, rekombinant insan eritropoietini alan kanser hastalarında tromboembolik olayların göreceli riskinin önemli ölçüde arttığını tutarlı bir şekilde gösterir (bkz. bölüm 4.4).
05.2 Farmakokinetik özellikler
Daha yüksek karbonhidrat içeriği göz önüne alındığında, darbepoetin alfa'nın dolaşımdaki seviyesi, molar eşdeğer r-HuEPO dozundan daha uzun süre minimum eritropoezi uyarıcı konsantrasyonun üzerinde kalır ve aynı biyolojik yanıtı elde etmek için darbepoetin alfa'nın daha az sıklıkla uygulanmasına izin verir.
Kronik böbrek yetmezliği olan hastalar
Darbepoetin alfa'nın farmakokinetiği, intravenöz ve subkutan uygulamayı takiben kronik böbrek yetmezliği hastalarında klinik olarak incelenmiştir. Darbepoetin alfanın terminal yarı ömrü intravenöz olarak uygulandığında 21 saattir (SD 7.5).Darbepoetin alfanın klerensi 1,9 ml/saat/kg (SD 0,56) ve kararlı durumda dağılım hacmi (Vss) yaklaşık olarak eşittir plazma hacmi (50 ml / kg). Deri altı uygulama için biyoyararlanım% 37'dir. Darbepoetin alfa'nın aylık subkutan uygulamasından sonra, 0.6 ila 2.1 μg / kg dozlarında, 1 "terminal yarılanma ömrü 73 saattir (SD 24). Deri altı absorpsiyon kinetiği, deri altından uygulandığında, intravenöz olarak uygulandığında, darbepoetin alfa'nın daha uzun bir "terminal yarı ömrü ile sonuçlanır. Klinik çalışmalarda, her iki uygulama yolunda da minimum birikim gözlemlenmiştir. Klinik öncesi çalışmalar, böbrek klerensinin minimum (maksimum) olduğunu göstermiştir. toplam klirensin %2'si) ve serum yarı ömrünü etkilemez.
Avrupa klinik çalışmalarında Aranesp ile tedavi edilen 809 hastadan elde edilen veriler, hemoglobini korumak için gereken dozu tanımlamak için analiz edildi; intravenöz veya subkutan olarak uygulanan haftalık ortalama doz arasında hiçbir fark gözlenmedi.
Hem diyaliz hem de diyaliz olmayan CRF'li pediyatrik hastalarda (2-16 yaş) darbepoetin alfa'nın farmakokinetiği, bir veya iki subkutan veya intravenöz dozdan sonra 2 haftaya (336 saat) kadar olan örnekleme periyotları için değerlendirildi. Aynı örnekleme süresini kullanarak, gözlemlenen farmakokinetik veriler ve popülasyon farmakokinetik modeli, darbepoetin alfa'nın farmakokinetik profilinin pediatrik ve yetişkin CRF hastalarında benzer olduğunu göstermiştir.
Bir faz I farmakokinetik çalışmasında, intravenöz uygulamadan sonra, eğri altında kalan alan için pediyatrik ve yetişkin hastalar arasında 0'dan sonsuza (AUC [0-∞]) yaklaşık %25'lik bir fark gözlenmiştir; ancak bu fark iki katından az olmuştur. Pediyatrik hastalarda gözlenen AUC [0-∞] aralığı Subkutan uygulamadan sonra EAA [0-∞] CRF'li yetişkin ve pediatrik hastalarda benzerdi.Yarı ömür yetişkin hastalarda da benzerdi. ve her ikisinden sonra pediatrik CRF intravenöz ve subkutan uygulama.
Kanserli ve kemoterapi gören hastalar
Yetişkin kanser hastalarına 2,25 μg/kg deri altı uygulamasından sonra, ortalama 91 saatlik bir süreden (SD 19,7) sonra 10.6 ng/ml (SD 5.9) darbepoetin alfa ortalama pik konsantrasyonuna ulaşılmıştır. Bu parametreler, geniş bir doz aralığında (haftada 0,5 ila 8 mcg/kg ve iki haftada bir 3 ila 9 mcg/kg) lineer dozla ilişkili farmakokinetik ile tutarlıydı. 12 hafta boyunca (haftalık veya 2 haftada bir) çoklu doz uygulamasından sonra farmakokinetik parametreler değişmedi. Beklenen ılımlı bir artış vardı (
05.3 Klinik öncesi güvenlik verileri
Sıçanlarda ve köpeklerde yapılan tüm çalışmalarda, darbepoetin alfa hemoglobin, hematokrit, kırmızı kan hücresi sayısı ve retikülositte beklenen farmakolojik etkilere karşılık gelen bir artışla sonuçlanmıştır. Çok yüksek dozlarda meydana gelen advers olayların hepsinin, abartılı bir farmakolojik etkiye ("artmış kan viskozitesine bağlı olarak azalan doku perfüzyonu)" atfedilebileceği düşünülmüştür. Bu olaylar arasında miyelofibroz, splenik hipertrofi ve ayrıca köpeklerde "elektrokardiyogramda" EKG-QRS kompleksinin uzaması yer alır. ancak QT aralığı üzerinde herhangi bir aritmi veya etki gözlenmedi.
Darbepoetin alfa herhangi bir genotoksik potansiyel göstermedi ve çoğalma üzerinde herhangi bir etkisi olmadı. laboratuvar ortamında veya canlıda hematolojik olmayan hücrelerdir. Kronik toksisite çalışmalarında, herhangi bir doku tipinde beklenmeyen onkojenik veya mitojenik tepkiler gözlenmemiştir. Darbepoetin alfa'nın kanserojen potansiyeli, uzun süreli hayvan çalışmalarında değerlendirilmemiştir.
Sıçanlarda ve tavşanlarda yapılan çalışmalarda, gebelik, embriyonal / fetal gelişim, doğum veya doğum sonrası gelişim üzerinde klinik olarak anlamlı herhangi bir yan etki kanıtı gözlemlenmemiştir. Transplasental geçiş minimaldi. Doğurganlıkta herhangi bir bozulma gözlenmedi.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
monobazik sodyum fosfat
Dibazik sodyum fosfat
Sodyum klorit
polisorbat 80
Enjeksiyonluk su
06.2 Uyumsuzluk
Uyumluluk çalışmalarının olmaması nedeniyle, bu tıbbi ürün diğer tıbbi ürünlerle karıştırılmamalı veya diğer tıbbi ürünlerle infüzyon yoluyla uygulanmamalıdır.
06.3 Geçerlilik süresi
3 yıl.
06.4 Depolama için özel önlemler
Buzdolabında (2°C - 8°C) saklayınız.
Dondurmayın.
İlacı ışıktan korumak için kabı dış kartonda saklayın.
Ayakta tedavi için, Aranesp oda sıcaklığında (25 °C'ye kadar) yalnızca bir kez ve yedi güne kadar saklanabilir. Buzdolabından çıkarılıp oda sıcaklığına (25°C'ye kadar) ulaştıktan sonra 7 gün içinde kullanılmalı veya imha edilmelidir.
06.5 İç ambalajın yapısı ve paketin içeriği
Kullanıma hazır şırıngada ARANESP 10 mikrogram enjeksiyonluk çözelti
0.4 ml enjeksiyonluk çözelti (25 mcg / ml darbepoetin alfa), paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırınga içinde. 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Kullanıma hazır şırıngada ARANESP 15 mikrogram enjeksiyonluk çözelti
0.375 ml enjeksiyonluk çözelti (40 mcg / ml darbepoetin alfa), paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırınga içinde.1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Aranesp 20 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırıngada 0,5 ml enjeksiyonluk çözelti (40 mcg / ml darbepoetin alfa). 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Kullanıma hazır şırıngada 30 mikrogram enjeksiyonluk ARANESP solüsyonu
0.3 ml enjeksiyonluk çözelti (100 mcg / ml darbepoetin alfa), paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırınga içinde. 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Kullanıma hazır şırıngada ARANESP 40 mikrogram enjeksiyonluk çözelti
0.4 ml enjeksiyonluk çözelti (100 mcg / ml darbepoetin alfa), paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırınga içinde. 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Kullanıma hazır şırıngada ARANESP 50 mcg enjeksiyonluk çözelti
Paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırıngada 0,5 ml enjeksiyonluk çözelti (100 mcg / ml darbepoetin alfa). 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Aranesp 60 mikrogram kullanıma hazır şırıngada enjeksiyonluk çözelti
Paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırıngada 0,3 ml enjeksiyonluk çözelti (200 μg / ml darbepoetin alfa). 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Kullanıma hazır şırıngada ARANESP 80 mikrogram enjeksiyonluk çözelti
Paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırıngada 0,4 ml enjeksiyonluk çözelti (200 μg / ml darbepoetin alfa). 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Aranesp 100 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
Paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırıngada 0,5 ml enjeksiyonluk çözelti (200 μg / ml darbepoetin alfa). 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Aranesp 130 mikrogram kullanıma hazır enjektörde enjeksiyonluk çözelti
0.65 ml enjeksiyonluk çözelti (200 mcg / ml darbepoetin alfa), paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırınga içinde. 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Kullanıma hazır şırıngada 150 mikrogram ARANESP enjeksiyonluk çözelti
0.3 ml enjeksiyonluk çözelti (500 mcg / ml darbepoetin alfa), paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırınga içinde. 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Aranesp 300 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
0.6 ml enjeksiyonluk çözelti (500 mcg / ml darbepoetin alfa), paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırınga içinde. 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Kullanıma hazır şırıngada 500 mikrogram enjeksiyonluk ARANESP solüsyonu
Paslanmaz çelik 27 gauge iğneli tip 1 cam kullanıma hazır şırıngada 1 ml enjeksiyonluk çözelti (500 mcg / ml darbepoetin alfa). 1 veya 4 kullanıma hazır şırıngadan oluşan paket boyutu.
Şırıngalar, otomatik iğne koruyuculu veya koruyucusuz veya kabarcıksız (yalnızca 1 şırıngalı paketler) blister ambalajlarda (1 ve 4 şırıngalık paketler) paketlenebilir.
Kullanıma hazır şırınganın iğne kapağı kuru doğal kauçuk (bir lateks türevi) içerir.Bkz. bölüm 4.4.
Kullanıma hazır kalem içinde ARANESP 10 mikrogram enjeksiyonluk çözelti
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde 0.4 ml enjeksiyonluk çözelti (25 mcg / ml darbepoetin alfa). 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde Aranesp 15 mikrogram enjeksiyonluk çözelti
0,375 ml enjeksiyonluk çözelti (40 mcg / ml darbepoetin alfa), tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde. 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde Aranesp 20 mikrogram enjeksiyonluk çözelti
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde 0,5 ml enjeksiyonluk çözelti (40 mcg / ml darbepoetin alfa). 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde ARANESP 30 mikrogram enjeksiyonluk çözelti
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde 0,3 ml enjeksiyonluk çözelti (100 mcg / ml darbepoetin alfa). 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalemde ARANESP 40 mikrogram enjeksiyonluk çözelti
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalemde 0,4 ml enjeksiyonluk çözelti (100 μg / ml darbepoetin alfa). 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde Aranesp 50 mcg enjeksiyonluk çözelti
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalemde 0,5 ml enjeksiyonluk çözelti (100 mcg / ml darbepoetin alfa). 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde ARANESP 60 mikrogram enjeksiyonluk çözelti
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğne ile kullanıma hazır bir kalemde 0,3 ml enjeksiyonluk çözelti (200 μg / ml darbepoetin alfa). 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde ARANESP 80 mikrogram enjeksiyonluk çözelti
0,4 ml enjeksiyonluk çözelti (200 μg / ml darbepoetin alfa), tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde. 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde Aranesp 100 mcg enjeksiyonluk solüsyon
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır bir kalemde 0,5 ml enjeksiyonluk çözelti (200 μg / ml darbepoetin alfa). 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde Aranesp 130 mcg enjeksiyonluk çözelti
0.65 mL enjeksiyonluk çözelti (200 mcg / mL darbepoetin alfa), tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde. 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde ARANESP 150 mikrogram enjeksiyonluk çözelti
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde 0.3 ml enjeksiyonluk çözelti (500 mcg / ml darbepoetin alfa). 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalem içinde Aranesp 300 mcg enjeksiyonluk çözelti
0,6 ml enjeksiyonluk çözelti (500 mcg / ml darbepoetin alfa), tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde. 1 veya 4 adet kullanıma hazır kalem paketi.
Kullanıma hazır kalemde enjeksiyon için Aranesp 500 mcg solüsyonu
Tip 1 cam şırınga ve paslanmaz çelik 27 gauge iğneli kullanıma hazır kalem içinde 1 ml enjeksiyonluk çözelti (500 mcg / ml darbepoetin alfa). 1 veya 4 Aranesp kullanıma hazır kalemlik paket boyutu.
Kullanıma hazır kalemin iğne kapağı kuru doğal kauçuk (bir lateks türevi) içerir.Bkz. bölüm 4.4.
Aranesp 25 mcg flakon içinde enjeksiyonluk çözelti
Floropolimer kaplı kauçuk tıpalı ve toz kapaklı alüminyum contalı tip I cam flakonda 1 ml enjeksiyonluk çözelti (25 mcg / ml darbepoetin alfa). 1 veya 4 flakonluk ambalaj boyutu.
Aranesp 40 mcg flakon içinde enjeksiyonluk çözelti
Floropolimer kaplı kauçuk tıpalı ve toz kapaklı alüminyum contalı tip I cam flakonda 1 ml enjeksiyonluk çözelti (40 mcg / ml darbepoetin alfa). 1 veya 4 flakonluk ambalaj boyutu.
Aranesp 60 mcg flakon içinde enjeksiyonluk çözelti
Floropolimer kaplı kauçuk tıpalı ve toz kapaklı alüminyum contalı tip I cam flakonda 1 ml enjeksiyonluk çözelti (60 mcg / ml darbepoetin alfa). 1 veya 4 flakonluk ambalaj boyutu.
Aranesp 100 mcg flakon içinde enjeksiyonluk çözelti
Floropolimer kaplı kauçuk tıpalı ve toz kapaklı alüminyum contalı tip I cam flakonda 1 ml enjeksiyonluk çözelti (100 mcg / ml darbepoetin alfa). 1 veya 4 flakonluk ambalaj boyutu.
Şişe içinde enjeksiyon için Aranesp 200 mcg solüsyonu
Floropolimer kaplı kauçuk tıpalı ve toz kapaklı alüminyum contalı tip I cam flakonda 1 ml enjeksiyonluk çözelti (200 mcg / ml darbepoetin alfa). 1 veya 4 flakonluk ambalaj boyutu.
Şişe içinde enjeksiyon için Aranesp 300 mcg solüsyonu
Floropolimer kaplı kauçuk tıpalar ve toz kapaklı alüminyum conta ile tip I cam flakonda 1 ml enjeksiyonluk çözelti (300 mcg / ml darbepoetin alfa). 1 veya 4 flakonluk ambalaj boyutu.
Tüm paket boyutları pazarlanmayabilir.
06.6 Kullanım ve kullanım talimatları
Kutu, kullanım ve işleme için eksiksiz talimatları içeren bir prospektüs içerir.
Aranesp kullanıma hazır kalem (SureClick) her sunum için tam dozu verir.
Aranesp steril bir üründür ancak koruyucu içermez. Birden fazla doz uygulamayın. Kalan ilaç miktarı atılmalıdır.
ARANESP solüsyonunu uygulamadan önce görünür partiküllerin olup olmadığı kontrol edilmelidir.Sadece renksiz, berrak veya hafif opalesan solüsyonlar enjekte edilmelidir.Çalkalamayın.Solüsyonu enjekte etmeden önce kabın oda sıcaklığına gelmesini bekleyin.
Kullanılmayan ilaçlar ve bu ilaçtan elde edilen atıklar yerel yönetmeliklere uygun olarak atılmalıdır.
07.0 PAZARLAMA YETKİ SAHİBİ
Amgen Avrupa B.V.
Minervum 7061
NL-4817 ZK Breda
Hollanda
08.0 PAZARLAMA YETKİ NUMARASI
Kullanıma hazır şırıngada ARANESP 10 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/001 1 adet blisterli
EU / 1/01/185/002 4 adet blisterli
EU / 1/01/185/033 1 adet blistersiz
EU / 1/01/185/074 1 adet, iğne korumalı blisterli
EU / 1/01/185/075 4 adet, iğne korumalı blisterli
Kullanıma hazır şırıngada ARANESP 15 mikrogram enjeksiyonluk çözelti
EU / 1/01/185/003 1 adet blisterli
EU / 1/01/185/004 4 adet blisterli
EU / 1/01/185/034 1 adet blistersiz
EU / 1/01/185/076 1 adet, iğne korumalı blisterli
EU / 1/01/185/077 4 adet, iğne korumalı blisterli
Aranesp 20 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
EU / 1/01/185/005 1 adet blisterli
EU / 1/01/185/006 4 adet blisterli
EU / 1/01/185/035 1 adet blistersiz
EU / 1/01/185/078 1 adet, iğne korumalı blisterli
EU / 1/01/185/079 4 adet, iğne korumalı blisterli
Kullanıma hazır şırıngada 30 mikrogram enjeksiyonluk ARANESP solüsyonu
EU / 1/01/185/007 1 adet blisterli
EU / 1/01/185/008 4 adet blisterli
EU / 1/01/185/036 1 adet blistersiz
EU / 1/01/185/080 1 adet, iğne korumalı blisterli
EU / 1/01/185/081 4 adet, iğne korumalı blisterli
Kullanıma hazır şırıngada ARANESP 40 mikrogram enjeksiyonluk çözelti
EU / 1/01/185/009 1 adet blisterli
EU / 1/01/185/010 4 adet blisterli
EU / 1/01/185/037 1 adet blistersiz
EU / 1/01/185/082 1 adet, iğne korumalı blisterli
EU / 1/01/185/083 4 adet, iğne korumalı blisterli
Kullanıma hazır şırıngada ARANESP 50 mcg enjeksiyonluk çözelti
EU / 1/01/185/011 1 adet blisterli
EU / 1/01/185/012 4 adet blisterli
EU / 1/01/185/038 1 adet blistersiz
EU / 1/01/185/084 1 adet, iğne korumalı blisterli
EU / 1/01/185/085 4 adet, iğne korumalı blisterli
Aranesp 60 mikrogram kullanıma hazır şırıngada enjeksiyonluk çözelti
EU / 1/01/185/013 1 adet blisterli
EU / 1/01/185/014 4 adet blisterli
EU / 1/01/185/039 1 adet blistersiz
EU / 1/01/185/086 1 adet, iğne korumalı blisterli
EU / 1/01/185/087 4 adet, iğne korumalı blisterli
Kullanıma hazır şırıngada ARANESP 80 mikrogram enjeksiyonluk çözelti
EU / 1/01/185/015 1 adet blisterli
EU / 1/01/185/016 4 adet blisterli
EU / 1/01/185/040 1 adet blistersiz
EU / 1/01/185/088 1 adet, iğne korumalı blisterli
EU / 1/01/185/089 4 adet, iğne korumalı blisterli
Aranesp 100 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
EU / 1/01/185/017 1 adet blisterli
EU / 1/01/185/018 4 adet blisterli
EU / 1/01/185/041 1 adet blistersiz
EU / 1/01/185/090 1 adet, iğne korumalı blisterli
EU / 1/01/185/091 4 adet, iğne korumalı blisterli
Aranesp 130 mikrogram kullanıma hazır enjektörde enjeksiyonluk çözelti
EU / 1/01/185/069 1 adet blisterli
EU / 1/01/185/070 4 adet blisterli
EU / 1/01/185/071 1 adet blistersiz
EU / 1/01/185/092 1 adet, iğne korumalı blisterli
EU / 1/01/185/093 4 adet, iğne korumalı blisterli
Kullanıma hazır şırıngada 150 mikrogram ARANESP enjeksiyonluk çözelti
EU / 1/01/185/019 1 adet blisterli
EU / 1/01/185/020 4 adet blisterli
EU / 1/01/185/042 1 adet blistersiz
EU / 1/01/185/094 1 adet, iğne korumalı blisterli
EU / 1/01/185/095 4 adet, iğne korumalı blisterli
Aranesp 300 mikrogram kullanıma hazır şırınga içinde enjeksiyonluk çözelti
EU / 1/01/185/021 1 adet blisterli
EU / 1/01/185/022 4 adet blisterli
EU / 1/01/185/043 1 adet blistersiz
EU / 1/01/185/096 1 adet, iğne korumalı blisterli
EU / 1/01/185/097 4 adet, iğne korumalı blisterli
Kullanıma hazır şırıngada 500 mikrogram enjeksiyonluk ARANESP solüsyonu
EU / 1/01/185/031 1 adet blisterli
EU / 1/01/185/032 4 adet blisterli
EU / 1/01/185/044 1 adet blistersiz
EU / 1/01/185/098 1 adet, iğne korumalı blisterli
EU / 1/01/185/099 4 adet, iğne korumalı blisterli
Kullanıma hazır kalem içinde ARANESP 10 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/045 1 adet
AB / 1/01/185/057 4 adet
Kullanıma hazır kalem içinde Aranesp 15 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/046 1 adet
AB / 1/01/185/058 4 adet
Kullanıma hazır kalem içinde Aranesp 20 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/047 1 adet
AB / 1/01/185/059 4 adet
Kullanıma hazır kalem içinde ARANESP 30 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/048 1 adet
AB / 1/01/185/060 4 adet
Kullanıma hazır kalemde ARANESP 40 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/049 1 adet
AB / 1/01/185/061 4 adet
Kullanıma hazır kalem içinde Aranesp 50 mcg enjeksiyonluk çözelti
AB / 1/01/185/050 1 adet
AB / 1/01/185/062 4 adet
Kullanıma hazır kalem içinde ARANESP 60 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/051 1 adet
AB / 1/01/185/063 4 adet
Kullanıma hazır kalem içinde ARANESP 80 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/052 1 adet
AB / 1/01/185/064 4 adet
Kullanıma hazır kalem içinde Aranesp 100 mcg enjeksiyonluk solüsyon
AB / 1/01/185/053 1 adet
AB / 1/01/185/065 4 adet
Kullanıma hazır kalem içinde Aranesp 130 mcg enjeksiyonluk çözelti
AB / 1/01/185/072 1 adet
AB / 1/01/185/073 4 adet
Kullanıma hazır kalem içinde ARANESP 150 mikrogram enjeksiyonluk çözelti
AB / 1/01/185/054 1 adet
AB / 1/01/185/066 4 adet
Kullanıma hazır kalem içinde Aranesp 300 mcg enjeksiyonluk çözelti
AB / 1/01/185/055 1 adet
AB / 1/01/185/067 4 adet
Kullanıma hazır kalemde enjeksiyon için Aranesp 500 mcg solüsyonu
AB / 1/01/185/056 1 adet
AB / 1/01/185/068 4 adet
Aranesp 25 mcg flakon içinde enjeksiyonluk çözelti
AB / 1/01/185/100 1 adet
AB / 1/01/185/101 4 adet
Aranesp 40 mcg flakon içinde enjeksiyonluk çözelti
AB / 1/01/185/102 1 adet
AB / 1/01/185/103 4 adet
Aranesp 60 mcg flakon içinde enjeksiyonluk çözelti
AB / 1/01/185/104 1 adet
AB / 1/01/185/105 4 adet
Aranesp 100 mcg flakon içinde enjeksiyonluk çözelti
AB / 1/01/185/106 1 adet
AB / 1/01/185/107 4 adet
Şişe içinde enjeksiyon için Aranesp 200 mcg solüsyonu
AB / 1/01/185/108 1 adet
AB / 1/01/185/109 4 adet
Şişe içinde enjeksiyon için Aranesp 300 mcg solüsyonu
AB / 1/01/185/110 1 adet
AB / 1/01/185/111 4 adet
035691017
035691029
035691031
035691043
035691056
035691068
035691070
035691082
035691094
035691106
035691118
035691120
035691132
035691144
035691157
035691169
035691171
035691183
035691195
035691207
035691219
035691221
035691310
035691322
035691334
035691346
035691359
035691361
035691373
035691385
035691397
035691409
035691411
035691423
035691435
035691447
035691536
035691548
035691551
035691563
035691575
035691587
035691599
035691601
035691613
035691625
035691637
035691649
035691652
035691664
035691676
035691688
035691690
035691702
035691714
035691726
035691738
035691740
035691753
035691765
035691777
035691789
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
İlk izin tarihi: 8 Haziran 2001
En son yenileme tarihi: 19 Mayıs 2006
10.0 METİN REVİZYON TARİHİ
Eylül 2015