Aktif maddeler: Asenapin (asenapin maleat)
Sycrest 5 mg dil altı tabletleri
Sycrest 10 mg dil altı tabletleri
Sycrest neden kullanılır? Bu ne için?
Sycrest, aktif madde asenapin içerir. Bu ilaç, antipsikotikler adı verilen bir ilaç grubuna aittir. Sycrest, yetişkinlerde bipolar I bozukluğu ile ilişkili orta ila şiddetli manik atakların tedavisinde kullanılır. Antipsikotik ilaçlar, sinir hücrelerinin (nörotransmitterlerin) iletişim kurmasını sağlayan kimyasalları etkiler. Bipolar I bozukluğu gibi beyni etkileyen hastalıklar, beyindeki dopamin ve serotonin gibi bazı kimyasalların dengesizliğinden kaynaklanabilir ve bu da yaşadığınız bazı semptomlara neden olabilir. Bu ilacın nasıl çalıştığının kesin mekanizması bilinmemektedir, ancak bu kimyasalların dengesini düzenlediğine inanılmaktadır.
Bipolar I bozukluğu ile ilişkili manik ataklar, "kendini iyi hissetme", "aşırı miktarda enerjiye sahip olma, normalden daha az uykuya ihtiyaç duyma, çok hızlı konuşma ve fikir uçuşması ve bazen sinirlilik gibi semptomları olan bir durumu temsil eder. ciddi.
Kontrendikasyonlar Sycrest ne zaman kullanılmamalıdır?
Sycrest'i almayın
Asenapine veya bu ilacın diğer bileşenlerinden herhangi birine karşı alerjiniz varsa (bölüm 6'da listelenmiştir).
Kullanım Önlemleri Sycrest'i almadan önce bilmeniz gerekenler
Sycrest'i almadan önce doktorunuzla, eczacınızla veya hemşirenizle konuşun.
SYCrest, demansı olan yaşlı hastalarda çalışılmamıştır. Bununla birlikte, diğer benzer türde ilaçlarla tedavi edilen demanslı yaşlı hastalar, inme veya ölüm geliştirme riski altında olabilir.
Sycrest demansı olan yaşlı hastaların tedavisi için onaylanmamıştır ve bu özel hasta grubunda kullanılması tavsiye edilmez.Sycrest düşük tansiyona neden olabilir.Tedavinin erken evrelerinde bazı kişiler özellikle pozisyon alırken bayılabilir. yattıktan veya oturduktan sonra dik durun.Bu genellikle kendi kendine geçer, değilse lütfen doktorunuza söyleyiniz.Dozunuzun ayarlanması gerekebilir.
meydana gelirse hemen doktorunuza söyleyiniz.
- dil, ağız ve yüzün istemsiz ritmik hareketleri. Sycrest'in durdurulması gerekebilir.
- ateş, şiddetli kas sertliği, terleme veya bilinç düzeyinde azalma ("nöroleptik malign sendrom" adı verilen bir bozukluk). Acil tıbbi tedavi gerekebilir.
SYCrest'i almadan önce doktorunuza veya eczacınıza danışınız:
- Belirtileri arasında yüksek sıcaklık ve kas sertliği (nöroleptik malign sendrom olarak da bilinir) olan bir durum teşhisi konduysa,
- Dilinizde veya yüzünüzde anormal hareketler olduysa (tardif diskinezi). Bu koşulların her ikisinin de bu tür ilaçlardan kaynaklanabileceğini bilmelisiniz.
- Kalp hastalığınız varsa veya sizi düşük kan basıncına yatkın hale getiren kalp hastalığı için tedavi görüyorsanız
- şeker hastasıysanız veya şeker hastalığına yatkınsanız
- Parkinson hastalığınız veya demansınız varsa
- Epilepsiniz varsa (uyuyorsa)
- Yutma güçlüğü çekiyorsanız (disfaji)
- Ciddi karaciğer problemleriniz varsa. Bu durumda Sycrest'i kullanmayınız.
- Çekirdek vücut sıcaklığınızı kontrol altında tutmakta zorluk çekiyorsanız
- intihar düşünceleriniz varsa
- Kanda yüksek prolaktin seviyeniz varsa (hiperprolaktinemi)
Dozunuzu ayarlamayı veya bir süre sizi izlemeyi tercih edebileceğinden, bunlardan herhangi biri sizin için geçerliyse doktorunuza bildirdiğinizden emin olun. Sycrest'i kullanırken bu koşullardan herhangi biri gelişirse veya kötüleşirse derhal doktorunuzla iletişime geçin.
Çocuklar ve ergenler
Sycrest'in 18 yaşın altındaki hastalarda kullanılması önerilmez.
Etkileşimler Hangi ilaçlar veya yiyecekler Sycrest'in etkisini değiştirebilir?
Diğer ilaçlar ve Sycrest
Başka ilaçlar alıyorsanız, yakın zamanda aldıysanız veya alma ihtimaliniz varsa doktorunuza veya eczacınıza söyleyiniz. Bazı ilaçlar Sycrest'in etkisini azaltabilir veya artırabilir.
Başka ilaçlar alıyorsanız, SYCREST en son alınmalıdır.
Antidepresan ilaçlar (özellikle fluvoksamin, paroksetin ve fluoksetin) kullanıyorsanız, SYCREST veya antidepresan ilacın dozunun ayarlanması gerekebileceğinden doktorunuza söylemelisiniz.
Parkinson hastalığı için ilaç (levodopa gibi) alıyorsanız, bu ilaç onları daha az etkili hale getirebileceğinden doktorunuza söylemelisiniz.
Sycrest esas olarak beyne etki ettiğinden, beyin işlevi üzerindeki ek bir etki nedeniyle beyne etki eden diğer ilaçların (veya alkolün) etkisi olabilir.
SYCrest kan basıncını düşürebildiğinden, SYCREST'i kan basıncını düşüren diğer ilaçlarla birlikte kullanırken dikkatli olunmalıdır.
Yiyecek, içecek ve alkol içeren Sycrest
Bu ilacı aldıktan sonra 10 dakika boyunca içmeyin veya yemek yemeyin.Bu ilacı alırken alkol almaktan kaçınmalısınız.
Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme
Hamileyseniz veya emziriyorsanız, hamile olabileceğinizi düşünüyorsanız veya hamile kalmayı planlıyorsanız bu ilacı kullanmadan önce doktorunuza veya eczacınıza danışınız.
Doktorunuz size söylemediği sürece, hamileyseniz SYCREST almayınız. Bu ilacı alıyor ve hamile kalıyorsanız veya hamile kalmayı planlıyorsanız, SYCREST almaya devam edip edemeyeceğinizi en kısa zamanda doktorunuza sorun.
Son üç aylık dönemde (gebeliklerinin son üç ayında) SYCREST kullanmış annelerin yeni doğan bebeklerinde aşağıdaki belirtiler ortaya çıkabilir: titreme, kas sertliği ve/veya güçsüzlük, uyku hali, ajitasyon, nefes alma sorunları ve beslenmede zorluk. Bu belirtilerden dolayı doktorunuza başvurmanız gerekebilir.
SYCrest alırken emzirmeyiniz.
Araç ve makine kullanma
Sycrest uyuşukluğa veya sedasyona neden olabilir. Bu nedenle araç veya makine kullanmadan önce konsantrasyonunuzun ve dikkatinizin etkilenmediğinden emin olun.
Doz, Yöntem ve Uygulama Süresi Sycrest Nasıl Kullanılır: Pozoloji
Bu ilacı her zaman tam olarak doktorunuzun veya eczacınızın size söylediği şekilde alınız. Şüpheniz varsa, doktorunuza veya eczacınıza danışın.
Önerilen doz günde iki kez bir adet 5 mg veya 10 mg dilaltı tablettir. Sabah bir doz, akşam bir doz alınmalıdır.
Kullanım için talimatlar
Sycrest dil altı kullanım içindir.
Tableti aşağıda açıklandığı şekilde alamıyorsanız, Sycrest önerilmez. Bu ilacı aşağıda açıklandığı şekilde alamıyorsanız, tedavi sizin için etkili olmayabilir.
- Dil altı tabletini almaya hazır olana kadar blisterden çıkarmayın.
- Tablete dokunurken elleriniz kuru olmalıdır.
- Tableti blisterin içinden itmeyin. Blister kesmeyin veya yırtmayın.
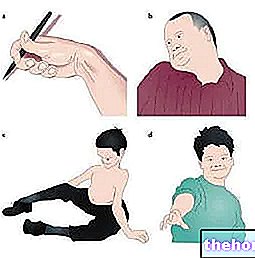
- Renkli tırnağı ayırın (şekil 1).
- Tableti yavaşça çıkarın (şekil 2). Tableti ezmeyin.
- Optimum emilimi sağlamak için tableti dilin altına yerleştirin ve tamamen eriyene kadar bekleyin (şekil 3). Tablet tükürük ile saniyeler içinde çözülür.
- Tableti yutmayın veya çiğnemeyin.
- Tableti aldıktan sonra 10 dakika boyunca içmeyin veya yemek yemeyin.
Aşırı doz: Çok fazla SYCREST aldıysanız ne yapmalısınız?
Kullanmanız gerekenden daha fazla Sycrest kullandıysanız
Çok fazla SYCREST aldıysanız hemen bir doktora başvurun. İlaç paketini yanınıza alın. Doz aşımı durumunda kendinizi uykulu veya yorgun hissedebilir veya anormal vücut hareketleri, ayakta durma ve yürüme sorunları, düşük tansiyon nedeniyle baş dönmesi ve ajite ve şaşkınlık hissedebilirsiniz.
SYCREST'i kullanmayı unutursanız
Unutulan bir dozu telafi etmek için çift doz almayınız. Bir dozu atlarsanız, bir sonraki dozunuzu her zamanki gibi alınız. İki veya daha fazla dozu atlarsanız, doktorunuza veya eczacınıza danışınız.
SYCREST almayı bırakırsanız
SYCREST almayı bırakırsanız, bu ilacın etkilerini kaybedersiniz. Belirtileriniz geri dönebileceğinden, doktorunuz söylemedikçe bu ilacı almayı bırakmamalısınız.
Bu ilacın kullanımıyla ilgili başka sorularınız varsa, doktorunuza veya eczacınıza sorunuz.
Yan Etkiler Sycrest'in yan etkileri nelerdir?
Tüm ilaçlar gibi, bu ilaç da yan etkilere neden olabilir, ancak bu yan etkiler herkeste görülmez.
Bu ilaçla ciddi yan etkiler bildirilmiştir. Aşağıdaki belirtilerden herhangi birini yaşarsanız derhal doktorunuza başvurun:
- alerjik reaksiyonlar (bunlar genellikle nefes almada veya yutmada zorluk, yüzde, dudaklarda, dilde veya boğazda şişme, döküntü, kaşıntı ve kalp hızında artış gibi etkilerin bir karışımını içerir)
- Vücut sıcaklığında ani yükselme, terleme, hızlı kalp atışı, şiddetli kas sertliği, kafa karışıklığı ve komaya neden olabilen kan basıncı dalgalanmaları
- konvülsiyonlar, nöbetler veya nöbetler
- bayılma
Aşağıdaki durumlarda derhal doktorunuza söyleyiniz:
- Aşırı susama, açlık veya aşırı idrara çıkma, zayıflık veya diyabetin kötüleşmesi gibi kan şekerinde yükselme belirtileri
- dilin solucan benzeri hareketleri veya dilin, ağzın, yanakların veya çenenin kollara ve bacaklara yayılabilen diğer kontrolsüz hareketleri
Bu ilaçla bildirilen diğer yan etkiler şunlardır:
Çok yaygın yan etkiler (10 kişiden 1'inden fazlasını etkileyebilir)
- endişe
- uyuşma
Yaygın yan etkiler (10 kişiden 1'ini etkileyebilir)
- kilo almak
- Iştah artışı
- yavaş veya sürekli kas kasılmaları
- huzursuzluk
- istemsiz kas kasılmaları
- yavaş hareketler, titreme
- sedasyon
- baş dönmesi
- mide bulantısı
- tat değişikliği
- dilde veya ağızda uyuşma hissi
- artan tükürük (tükürük kaybı)
- kas sertliği
- tükenmişlik
- artan karaciğer enzimleri seviyesi
Yaygın olmayan yan etkiler (100 kişiden 1'ini etkileyebilir)
- anormal kas hareketleri: ekstrapiramidal semptomlar (EPS) olarak bilinen ve aşağıdaki semptomlardan bir veya daha fazlasını içerebilen bir dizi semptom: kasların, dilin veya çenenin anormal hareketleri, yavaş veya sürekli kas kasılmaları, kas spazmları, titreme (titreme), anormal göz hareketleri, istemsiz kas seğirmesi, yavaş hareketler veya huzursuzluk
- bacaklarda rahatsızlık hissi (huzursuz bacak sendromu da denir)
- konuşma sorunları
- anormal, yavaş veya hızlı kalp atışı
- şube kalp bloğu
- anormal elektrokardiyogram (QT uzaması)
- ayakta dururken düşük tansiyon
- düşük kan basıncı
- dilde veya ağızda karıncalanma
- şişmiş veya ağrılı dil
- yutma zorluğu
- ağız içinde ülserler, ağrı, kızarıklık, şişlik ve kabarcıklar
- cinsel işlev bozukluğu
- düzenli adet döngüsü eksikliği
Seyrek yan etkiler (1.000 kişiden 1'ini etkileyebilir)
- beyaz kan hücresi seviyelerindeki değişiklikler
- görme ile odaklanma zorluğu
- kan damarlarında akciğerlere giden kan pıhtıları göğüs ağrısına ve nefes almada zorluğa neden olur
- açıklanamayan sürekli ağrılar ve keskin ağrılar olarak ortaya çıkan kas bozuklukları
- erkek meme boyutunda artış
- memeden süt veya sıvı kaybı
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuzla, eczacınızla veya hemşirenizle konuşun.Bu broşürde listelenmeyen olası yan etkiler de buna dahildir.Yan etkileri Ek V'de listelenen ulusal raporlama sistemi aracılığıyla da doğrudan bildirebilirsiniz. Yardımcı olabileceğiniz yan etkiler Bu ilacın güvenliği hakkında daha fazla bilgi sağlayın.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
Blister ve karton üzerinde belirtilen son kullanma tarihinden sonra bu ilacı kullanmayınız. Son kullanma tarihi, ayın son gününü ifade eder.
İlacı ışık ve nemden korumak için bu ilacı orijinal ambalajında saklayınız.
Bu tıbbi ürün herhangi bir özel saklama sıcaklığı gerektirmez.
Herhangi bir ilacı atık su veya evsel atık yoluyla atmayın.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorun.Bu, çevrenin korunmasına yardımcı olacaktır.
Kompozisyon ve farmasötik form
Sycrest'in içeriği
- Aktif bileşen asenapindir.
- Her bir Sycrest 5 mg dilaltı tableti, 5 mg asenapin içerir.
- Her bir Sycrest 10 mg dilaltı tableti, 10 mg asenapin içerir.
- Tam içerik, Sycrest tabletlerinin ambalajında belirtilmiştir.
- Diğer bileşenler jelatin ve mannitoldür (E421).
Sycrest'in görünümü ve paketin içeriği
5 mg dilaltı tabletleri yuvarlak, beyazdan kirli beyaza, bir tarafında "5" ile işaretlenmiştir.
10 mg dilaltı tabletleri yuvarlak, beyazdan kirli beyaza, bir tarafında "10" olarak işaretlenmiştir.
Dil altı tabletleri, her biri 10 tablet içeren soyulabilir folyo kabarcıklar içinde sağlanır. Paketler 20, 60 veya 100 tablet içerir.
Tüm paket boyutları pazarlanmayabilir.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
SYCREST 10 MG DİL TABLETLERİ
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Her dil altı tableti 10 mg asenapin (maleat olarak) içerir.
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakın.
03.0 FARMASÖTİK FORM
Dil altı tableti.
Beyazdan kirli beyaza, yuvarlak, dilaltı tabletler, bir tarafında "10" ile oyulmuş.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Sycrest, yetişkinlerde bipolar I bozukluğu ile ilişkili orta ila şiddetli manik atakların tedavisinde endikedir.
04.2 Pozoloji ve uygulama yöntemi
Dozaj
Manikür bölümü
Sycrest'in önerilen başlangıç dozu, monoterapi olarak günde iki kez 10 mg'dır. Sabah bir doz, akşam bir doz alınmalıdır. Doz, ancak klinik değerlendirmeden sonra günde iki kez 5 mg'a düşürülebilir. Kombinasyon tedavisi için günde iki kez 5 mg'lık bir başlangıç dozu önerilir. Bireysel hastanın klinik yanıtına ve tolere edilebilirliğine bağlı olarak, doz günde iki kez 10 mg'a yükseltilebilir.
Özel hasta popülasyonları hakkında daha fazla bilgi edinin
Pediatrik popülasyon
Sycrest'in 18 yaşın altındaki çocuklarda güvenliliği ve etkililiği belirlenmemiştir.Sycrest'in adolesan hastalarda kullanımına ilişkin sınırlı güvenlik verileri mevcuttur. Adolesan hastalarda farmakokinetik bir çalışma yapılmıştır. Halihazırda mevcut veriler bölüm 5.2'de açıklanmıştır, ancak bir pozoloji hakkında herhangi bir tavsiyeye izin vermemektedir.
Yaşlı hastalar
SYCREST yaşlılarda dikkatli kullanılmalıdır. 65 yaş ve üzerindeki hastalarda sınırlı etkililik verileri mevcuttur Mevcut farmakokinetik veriler bölüm 5.2'de açıklanmıştır.
Böbrek yetmezliği olan hastalar
Böbrek yetmezliği olan hastalarda doz ayarlaması gerekli değildir. Kreatinin klerensi 15 ml/dak'nın altında olan şiddetli böbrek yetmezliği olan hastalarda asenapin ile deneyim yoktur.
Karaciğer yetmezliği olan hastalar
Hafif karaciğer yetmezliği olan hastalarda doz ayarlaması gerekli değildir. Orta derecede karaciğer yetmezliği (Child-Pugh Sınıf B) olan bazı hastalarda plazma asenapin düzeylerinin yükselmesi olasılığı göz ardı edilemez ve dikkatli olunması önerilir. Şiddetli karaciğer yetmezliği olan hastalarda (Child-Pugh Sınıf C), asenapin maruziyetinde 7 kat artış gözlenmiştir, bu nedenle şiddetli karaciğer yetmezliği olan hastalarda SYCrest önerilmemektedir.
Uygulama yöntemi
Tablet, almaya hazır olana kadar blisterden çıkarılmamalıdır.Tablete dokunurken elleriniz kuru olmalıdır.Tablet paketin içine itilmemelidir.Paket kesilmemeli veya yırtılmamalıdır.Taşı çekin. tableti nazikçe renklendirin. Tablet ezilmemelidir.
Optimum emilimi sağlamak için, Sycrest dilaltı tableti tamamen çözülecek şekilde dilin altına yerleştirilmelidir. Tablet tükürük ile saniyeler içinde çözülür. Sycrest dil altı tabletleri çiğnenmemeli veya yutulmamalıdır. Uygulamadan sonra 10 dakika boyunca içmekten ve yemek yemekten kaçının.
Diğer ilaçlarla birlikte kullanıldığında SYCrest en son alınmalıdır.
Yutulduğunda asenapin biyoyararlanımı düşük olduğundan, bu uygulama yöntemine uymayan hastalarda SYCrest tedavisi önerilmez (
04.3 Kontrendikasyonlar
Etkin maddeye veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
04.4 Özel uyarılar ve uygun kullanım önlemleri
Demansla ilişkili psikozu olan yaşlı hastalar
Antipsikotik ilaçlarla tedavi edilen demansla ilişkili psikozu olan yaşlı hastalar, yüksek ölüm riski altındadır.
Sycrest, demansla ilişkili psikozlu hastaların tedavisi için onaylanmamıştır ve bu özel hasta grubunda kullanılması önerilmez.
Nöroleptik malign sendrom
Hipertermi, kas sertliği, otonomik dengesizlik, bilinç değişikliği ve serum kreatin fosfokinaz düzeylerinde yükselme ile karakterize olan Nöroleptik Malign Sendromun (NMS) başlangıcı, asenapin dahil antipsikotik ilaçların uygulanmasıyla bildirilmiştir. klinik raporlar, miyoglobinüri ( rabdomiyoliz) ve akut böbrek yetmezliği bildirilmiştir.
Bir hasta NMS'yi düşündüren belirti ve semptomlar geliştirirse, Sycrest uygulaması kesilmelidir.
konvülsiyonlar
Klinik çalışmalarda, asenapin tedavisi sırasında zaman zaman konvülsiyon vakaları bildirilmiştir.Bu nedenle, nöbet bozukluğu öyküsü veya nöbetlerle ilişkili diğer durumları olan hastalarda SYCrest dikkatli kullanılmalıdır.
İntihar
İntihar girişimi olasılığı, psikotik patolojinin ve bipolar bozukluğun bir parçasıdır. Bu nedenle, tedavi sırasında yüksek riskli hastaların dikkatli bir şekilde izlenmesi gerekir.
Ortostatik hipotansiyon
Asenapin, muhtemelen α1-adrenerjik antagonist özelliklerinden dolayı özellikle tedavinin başlangıcında ortostatik hipotansiyon ve senkopu indükleyebilir Yaşlı hastalar özellikle ortostatik hipotansiyon riski altındadır (bkz. bölüm 4.8). Klinik çalışmalarda, Sycrest tedavisi sırasında zaman zaman senkop vakaları bildirilmiştir. SYCrest, yaşlı hastalarda ve kardiyovasküler hastalığı (örn. kalp yetmezliği, miyokard enfarktüsü veya iskemi, iletim anormallikleri), serebrovasküler bozuklukları veya hastayı hipotansiyona yatkın hale getiren durumları (örn. dehidratasyon ve hipovolemi) olduğu bilinen hastalarda dikkatle uygulanmalıdır.
tardif diskinezi
Anti-dopaminerjik özelliklere sahip tıbbi ürünler, "ağırlıklı olarak dil ve/veya yüzde ritmik istemsiz hareketlerle karakterize geç diskinezi indüksiyonu" ile ilişkilendirilmiştir. Klinik çalışmalarda, asenapin ile tedavi sırasında zaman zaman tardif diskinezi vakaları bildirilmiştir. L" Ekstrapiramidal semptomların başlaması, geç diskinezi için bir risk faktörüdür. Sycrest ile tedavi edilen bir hastada geç diskinezi belirti ve semptomları ortaya çıkarsa, tedaviyi bırakma olasılığı düşünülmelidir.
hiperprolaktinemi
SYCrest alan bazı hastalarda prolaktin düzeylerinde artışlar gözlenmiştir. Klinik çalışmalarda, bildirilen anormal prolaktin seviyeleri ile ilgili az sayıda advers reaksiyon gözlenmiştir.
QT aralığı
QT aralığının klinik olarak anlamlı uzaması asenapin ile ilişkili görünmemektedir. SYCrest'i bilinen kardiyovasküler hastalığı olan veya ailesinde QT aralığı uzaması öyküsü olan hastalara ve uzadığı düşünülen diğer tıbbi ürünlerle kombinasyon halinde reçete ederken dikkatli olunmalıdır. QT aralığı.
Hiperglisemi ve diabetes mellitus
Asenapin tedavisi sırasında bazen hiperglisemi veya önceden var olan diyabetin alevlenmesi bildirilmiştir. Atipik antipsikotiklerin kullanımı ile anormal glikoz değerleri arasındaki ilişkinin değerlendirilmesi, şizofreni veya bipolar bozukluğu olan hastalarda arka planda diabetes mellitus riskinin artması olasılığı ve "popülasyonda artan diabetes mellitus insidansı" nedeniyle karmaşıktır. Genel Diyabetik hastaların ve diyabetes mellitus gelişimi için risk faktörleri olan kişilerin yeterli klinik izleme altına alınması önerilir.
disfaji
Dismotilite ve özofagus aspirasyonu antipsikotik tedavi ile ilişkilendirilmiştir. Sycrest ile tedavi edilen hastalarda sporadik olarak birkaç disfaji vakası bildirilmiştir.
Vücut termoregülasyonu
Vücudun çekirdek vücut ısısını düşürme yeteneğinin değişmesi, antipsikotik ilaçlara bağlanmıştır. Klinik çalışmalar, vücut sıcaklığındaki klinik olarak anlamlı değişikliklerin asenapin kullanımı ile ilişkili görünmediği sonucuna varmıştır. fiziksel egzersiz, aşırı sıcağa maruz kalma, antikolinerjik ilaçlarla birlikte tedavi veya dehidratasyona yatkın hastalarda.
Şiddetli karaciğer yetmezliği olan hastalar
Şiddetli karaciğer yetmezliği olan hastalarda (Child-Pugh Sınıf C) asenapine maruziyet 7 kat artmıştır.Bu nedenle bu hastalarda SYCrest önerilmemektedir.
Lewy cisimcikli Parkinson hastalığı ve bunama
Doktorlar, Parkinson hastalığı veya Lewy cisimcikli demansı (DLB) olan hastalara Sycrest dahil antipsikotik ilaçlar yazmanın risklerini ve yararlarını değerlendirmelidir, çünkü her iki grup da Nöroleptik Malign Sendrom için yüksek risk altında olabilir ve ayrıca antipsikotiklere karşı artan duyarlılığa sahip olabilir. . Bu artan duyarlılığın tezahürü, ekstrapiramidal semptomlara ek olarak, kafa karışıklığı, donukluk, sık düşmelerle birlikte postural instabiliteyi içerebilir.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Asenapinin birincil merkezi sinir sistemi (CNS) etkilerine dayanarak (bkz. bölüm 4.8), tıbbi ürün diğer merkezi etkili tıbbi ürünlerle birlikte dikkatle uygulanmalıdır. Hastalara SYCrest ile tedavi edilirken alkol tüketmemeleri tavsiye edilmelidir.
Diğer ilaçların Sycrest'i etkileme potansiyeli
Asenapin birincil olarak UGT1A4'ün doğrudan glukuronidasyonu ve sitokrom P450 izoenzimleri (esas olarak CYP1A2) tarafından oksidatif metabolizma yoluyla elimine edilir.İnhibitörlerin ve bu enzim döngülerinin birkaçının bir aktivatörünün asenapin farmakokinetiği üzerindeki potansiyel etkileri, özellikle fluvoksamin (CYP1A2 inhibitörü) araştırılmıştır. , paroksetin (CYP2D6 inhibitörü), imipramin (CYP1A2/2C19/3A4 inhibitörü), simetidin (CYP3A4/2D6/1A2 inhibitörü), karbamazepin (CYP3A4/1A2 inhibitörü), "UGT). Fluvoksamin dışında, etkileşime giren tıbbi ürünlerin hiçbiri asenapin farmakokinetiğinde klinik olarak anlamlı değişikliklere yol açmamıştır.
5 mg'lık tek bir asenapin dozu ile eşzamanlı uygulama sırasında, günde iki kez 25 mg fluvoksamin, asenapin EAA'sında %29'luk bir artışa neden olmuştur. Fluvoksaminin tam terapötik dozunun, konsantrasyonlarda daha büyük bir artışa neden olduğundan şüphelenilmektedir. bu nedenle dikkatli olunmalıdır.
Sycrest'in diğer ilaçları etkileme potansiyeli
Ortostatik hipotansiyonu indükleme potansiyeline sahip α1-adrenerjik antagonizması nedeniyle (bkz. bölüm 4.4), Sycrest bazı antihipertansif ajanların etkilerini güçlendirebilir.
Asenapin, levodopa ve dopamin agonistlerinin etkisini antagonize edebilir.Bu kombinasyon gerekli görülürse, her tedavinin en düşük etkili dozu reçete edilmelidir.
Çalışmalar laboratuvar ortamında asenapinin CYP2D6'yı zayıf bir şekilde inhibe ettiğini gösterir. Asenapin tarafından CYP2D6 inhibisyonunun etkilerine ilişkin klinik ilaç etkileşim çalışmaları aşağıdaki sonuçları göstermiştir:
- Sağlıklı gönüllülerde dekstrometorfan ve asenapin eşzamanlı uygulamasından sonra, dekstrorfan / dekstrometorfan oranı (DX / DM), CYP2D6 aktivitesinin bir göstergesi olarak ölçüldü. Günde iki kez 5 mg, DX / DM oranında 0.43'e kadar fraksiyonel bir düşüşe neden oldu. Aynı çalışmada, günde 20 mg paroksetin dozu ile tedavi, DX/DM oranını 0.032'ye düşürdü.
- Ayrı bir çalışmada, 75 mg'lık tek doz imipramin ile 5 mg'lık tek doz asenapin'in birlikte uygulanması, metabolit desipraminin (CYP2D6'nın bir substratı) plazma konsantrasyonlarını etkilememiştir.
- 15 sağlıklı erkek denekte günde iki kez 5 mg asenapin ile tedavi sırasında tek bir 20 mg doz paroksetin (bir CYP2D6 substratı ve inhibitörü) ile birlikte uygulanması, paroksetin maruziyetinde neredeyse iki kat artışa neden olmuştur.
asenapin canlıda en iyi ihtimalle zayıf bir CYP2D6 inhibitörü gibi görünmektedir. Bununla birlikte, asenapin, paroksetinin metabolizması üzerindeki inhibitör etkilerini artırabilir.
Bu nedenle SYCrest, CYP2D6'nın hem substratları hem de inhibitörleri olan diğer tıbbi ürünlerle birlikte dikkatle uygulanmalıdır.
Optimal emilimi sağlamak için uygulamayı takiben 10 dakika boyunca içmekten ve yemek yemekten kaçının.
04.6 Hamilelik ve emzirme
Gebelik
SYCrest'in hamile kadınlarda kullanımına ilişkin veriler yetersizdir Asenapin hayvan çalışmalarında teratojenik etki göstermemiştir Hayvan çalışmaları anne ve embriyo toksisitesi göstermiştir (bkz. Bölüm 5.3).
Gebeliğin üçüncü trimesterinde antipsikotiklere (Sycrest dahil) maruz kalan bebekler, doğumdan sonra şiddeti ve süresi değişebilen ekstrapiramidal ve/veya yoksunluk semptomları dahil advers reaksiyon riski altındadır. Yenidoğanlarda huzursuzluk, hipertoni, hipotoni, tremor, somnolans, nefes almada zorluk veya beslenme bozuklukları bildirilmiştir, bu nedenle yenidoğanlar yakından izlenmelidir.
SYCrest, kesinlikle gerekli olmadıkça ve yalnızca potansiyel yararın fetusun potansiyel riskinden daha ağır basması durumunda hamilelikte kullanılmamalıdır.
Besleme zamanı
Asenapin emziren sıçanların sütüne geçmiştir Asenapin veya metabolitlerinin insan sütüne geçip geçmediği bilinmemektedir. SYCrest alan kadınların emzirmemeleri önerilir.
Doğurganlık
Klinik olmayan çalışmalarda doğurganlıkta herhangi bir bozulma gözlenmemiştir (bkz. bölüm 5.3).
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
Araç ve makine kullanımı ile ilgili herhangi bir çalışma yapılmamıştır. Asenapin somnolans ve sedasyona neden olabilir.Bu nedenle hastalar, Sycrest tedavisinin artık herhangi bir olumsuz etkisi olmayacağından makul ölçüde emin olana kadar makine kullanma veya araç kullanma konusunda dikkatli olmalıdır.
04.8 İstenmeyen etkiler
Güvenlik profilinin özeti
Asenapin tedavisi sırasında en sık bildirilen advers ilaç reaksiyonları somnolans ve anksiyete idi.
Advers reaksiyon tablosu
Asenapin tedavisi ile ilişkili advers ilaç reaksiyonlarının (ADR) insidansı aşağıdaki tabloda gösterilmektedir.Tablo, klinik denemeler ve/veya pazarlama sonrası kullanım sırasında bildirilen advers olaylara dayanmaktadır.
Tüm ADR'ler sistem organ sınıfı ve sıklığına göre listelenmiştir; çok yaygın (≥1/10), yaygın (≥1/100,
Pazarlama sonrası kullanım sırasında bildirilen advers reaksiyonların sıklığı, spontan raporlardan elde edildiği için belirlenemez, bu nedenle bu advers olayların sıklığı “bilinmiyor” olarak tanımlanmaktadır.
Seçilmiş advers reaksiyonların tanımı
Ekstrapiramidal semptomlar (SEP)
Klinik çalışmalarda, asenapin ile tedavi edilen hastalarda ekstrapiramidal semptomların insidansı plasebodan daha yüksekti (%15.4'e karşı %11.0).
Şizofrenide yapılan kısa süreli (6 haftalık) çalışmalardan, asenapin ile tedavi edilen hastalarda akatizi için bir doz-yanıt ilişkisi olduğu ve parkinsonizm için daha yüksek dozlarla artış eğilimi olduğu görülmektedir.
Kilo almak
Şizofreni ve bipolar mani ile ilgili kısa ve uzun süreli klinik çalışmalarda, asenapin için ortalama ağırlık değişimi 0.8 kg idi. Kısa süreli şizofreni klinik çalışmalarında klinik olarak anlamlı kilo artışı (başlangıçtan değerlendirmeye kadar >%7 kilo artışı) olan deneklerin oranı asenapin için %5.3 iken plasebo için %2.3 olmuştur. Kısa süreli bipolar mani klinik çalışmalarında klinik olarak anlamlı kilo artışı (başlangıçtan değerlendirmeye kadar >%7 kilo artışı) olan deneklerin oranı asenapin için %6.5 iken plasebo için %0.6 olmuştur.
Ortostatik hipotansiyon
Faz 2/3 çalışmalarının birleşik popülasyonunda %0.3'e kıyasla yaşlı hastalarda ortostatik hipotansiyon insidansı %4.1 olmuştur.
Karaciğer enzimleri
Hepatik transaminazların, alanin transferazın (ALT), aspartat transferazın (AST) geçici ve asemptomatik yükselmeleri, özellikle erken tedavide yaygın olarak gözlenmiştir.
Diğer sonuçlar
Asenapin ile tedavi edilen hastalarda serebrovasküler olaylar bildirilmiştir, ancak 18 ila 65 yaş arasındaki erişkinlerde beklenenden daha yüksek bir insidans kanıtı yoktur.
Asenapin anestezik özelliklere sahiptir. Oral hipoestezi ve oral parestezi uygulamadan hemen sonra ortaya çıkabilir ve genellikle 1 saat içinde düzelir.
Asenapin ile tedavi edilen hastalarda, anafilaktik/anafilaktoid reaksiyonlar, anjiyoödem, dilin şişmesi ve boğazın şişmesi (faringeal ödem) dahil olmak üzere ciddi aşırı duyarlılık reaksiyonlarına ilişkin pazarlama sonrası raporlar olmuştur.
04.9 Doz aşımı
Asenapin tedavi programında doz aşımı vakaları bildirilmiştir. Bildirilen tahmini dozlar 15 ila 400 mg arasında değişmektedir. Çoğu durumda, asenapinin dilaltından alınıp alınmadığı belirsizdi. İlaca bağlı advers reaksiyonlar, ajitasyon ve konfüzyon, akatizi, orofasiyal distoni, sedasyon ve asemptomatik EKG bulgularını (bradikardi, supraventriküler kompleksler, intraventriküler iletim gecikmesi) içermiştir.
Sycrest doz aşımının tedavisi hakkında özel bir bilgi mevcut değildir. Sycrest'in spesifik bir panzehiri yoktur. Birden fazla tıbbi ürünün alınmış olma olasılığı göz önünde bulundurulmalıdır. Aritmiler için kardiyovasküler monitörizasyon yapılmalı ve doz aşımı yönetimi destekleyici bakıma, yeterli hava yolu oksijenasyonunu ve ventilasyonu sürdürmeye ve semptomları yönetmeye odaklanmalıdır.Hipotansiyon ve dolaşım kollapsı, intravenöz sıvılar ve/veya sempatomimetik ajanlar gibi uygun önlemlerle tedavi edilmelidir. Epinefrin ve dopamin kullanmayın, çünkü beta-stimülasyonlar, SYCrest'in neden olduğu alfa-adrenerjik blokaj durumunda hipotansiyonu kötüleştirebilir. Şiddetli ekstrapiramidal ilaçlar, antikolinerjik tıbbi ürünler uygulanmalıdır. Hasta iyileşene kadar yakın izlemeye ve klinik gözetime devam edin. kurtarıldı.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: psikoleptikler, antipsikotikler.
ATC kodu: N05AH05.
Hareket mekanizması
Bipolar bozukluk için etkili diğer tıbbi ürünlerde olduğu gibi, asenapinin etki mekanizması tam olarak anlaşılmamıştır, ancak, reseptörlerin farmakolojisine dayanarak, asenapinin etkinliğine, D2'nin antagonist aktivitesinin bir "kombinasyonu" tarafından aracılık edildiğine inanılmaktadır. ve 5-HT2A reseptörleri. Örneğin 5-HT1A, 5-HT1B, 5-HT2C, 5-HT6, 5-HT7, D3 ve a2-adrenerjik reseptörler gibi diğer reseptörlerdeki eylemler de asenapinin klinik etkilerine katkıda bulunabilir.
Klinik etkinlik
Bipolar I bozuklukta klinik etkinlik
DSM-IV tarafından tanımlandığı gibi bipolar I bozukluğun manik veya karma epizodunun tedavisinde asenapinin etkinliği (Ruhsal Bozuklukların Tanısal ve İstatistiksel El Kitabı) psikotik belirtileri olan veya olmayan, sırasıyla 488 ve 489 hastayı içeren benzer şekilde tasarlanmış, 3 haftalık, randomize, çift kör, plasebo ve aktif madde (olanzapin) monoterapisi kontrollü iki çalışmada değerlendirilmiştir. Tüm hastalar, Ruhsal Bozuklukların Tanısal ve Sayımsal El Kitabı, dördüncü baskı (DSM-IV), mevcut manik dönem (DSM-IV 296.4x) veya karma (DSM-IV) 296.6x tarafından tanımlanan bipolar I bozukluk tanı kriterlerini karşıladı. ) ve anket puanı ≥20 olan Genç Mani Derecelendirme Ölçeği (Y-MRS) allo tarama ve temel. Hızlı siklus hastaları bu çalışmalardan çıkarıldı. Asenapin "3 hafta boyunca manik semptomları azaltmada plaseboya göre üstün etkinlik" göstermiştir. Taban çizgisinden " değerine değişim için nokta tahminleri [%95 GA]uç nokta YMRS'de LOCF analizi kullanılarak yapılan iki çalışmada şu şekildeydi:
Asenapin için -11,5 [-13,0, -10,0] ve plasebo için - 7,8 [-10,0, -5,6] ve
Asenapin için -10,8 [-12.3, -9.3] ve plasebo için -5.5 [-7.5, -3.5].
Asenapin ve plasebo arasında istatistiksel olarak anlamlı bir fark 2. gün kadar erken görüldü.
İki önemli 3 haftalık kayıt çalışmasından gelen hastalar, çalışmanın 9 haftalık bir uzantısında incelenmiştir.Bu çalışmada, epizod sırasındaki etkinin sürdürülmesi, 12 haftalık tedaviden sonra gösterilmiştir.
Manik veya mikst bipolar I bozukluğu epizodu olan, psikotik özellikleri olan veya olmayan 326 hastayı içeren 12 haftalık, plasebo kontrollü bir klinik çalışmada, kısmi sonuçlar cevap vermeyen 2 hafta boyunca terapötik serum seviyelerinde tek başına lityum veya valproata, yardımcı tedavi olarak asenapin eklenmesinin etkinlikte, 3. haftada tek başına verilen lityum veya valproata göre daha üstün olduğu bulundu (başlangıçtan değişiklik için nokta tahminleri [%95 GA]uç nokta YMRS'de asenapin için -10,3 [-11.9, -8.8] ve plasebo için -7.9 [-9.4, -6.4]) ve 12. haftada (- asenapin için - 12.7 [-14.5, -10.9] ve -9.3 [ -11.8, -7.6] plasebo için) manik semptomların azaltılmasında.
Pediatrik popülasyon
Avrupa İlaç Ajansı, bipolar I bozuklukta pediyatrik popülasyonun bir veya daha fazla alt grubunda asenapin ile yapılan çalışmaların sonuçlarını sunma yükümlülüğünü ertelemiştir (pediatrik kullanım hakkında bilgi için bkz. bölüm 4.2).
05.2 "Farmakokinetik özellikler
absorpsiyon
Dilaltı uygulamayı takiben, asenapin, 0.5 - 1.5 saat içinde doruk plazma konsantrasyonları ile hızla emilir. 5 mg'da dilaltı asenapinin mutlak biyoyararlanımı %35'tir. Yutulduğunda asenapin'in mutlak biyoyararlanımı zayıftır (asenapin uygulamasından birkaç dakika sonra (2 veya 5) su, asenapin maruziyetinde bir azalma ile sonuçlanmıştır (sırasıyla %19 ve %10).Bu nedenle, 10 dakika içinde içmekten ve yemek yemekten kaçınılmalıdır. uygulamadan sonra (bkz. bölüm 4.2).
Dağıtım
Asenapin hızla dağılır ve geniş bir dağılım hacmine sahiptir (yaklaşık 1.700 l), bu da geniş ekstravasküler dağılımı gösterir. Asenapin, albümin ve α1-asit glikoprotein dahil olmak üzere plazma proteinlerine (%95) geniş ölçüde bağlanır.
biyotransformasyon
Asenapin büyük ölçüde metabolize edilir. Doğrudan glukuronidasyon (UGT1A4 aracılı) ve sitokrom P450 (esas olarak CYP1A2, 2D6 ve 3 ° 4'ün katılımıyla) yoluyla oksidasyon ve demetilasyon, asenapinin başlıca metabolik yollarıdır. canlıda insanlarda radyoaktif izotop etiketli asenapin ile yürütülen, plazmadaki ilaçla ilgili baskın varlık asenapin N + -glukuroniddi; diğerleri küçük miktarlarda N-dismetilasenapin, N-dismetilasenapin, N-karbamoil glukuronid ve modifiye edilmemiş asenapindir. Sycrest'in aktivitesi esas olarak ana bileşiğe bağlıdır.
Asenapin, CYP2D6'nın zayıf bir inhibitörüdür. Asenapin, insan hepatosit kültürlerinde herhangi bir CYP1A2 veya CYP3A4 aktivitesini indüklemez Asenapin ile bu metabolik yolakların bilinen inhibitörleri, aktivatörleri veya substratlarının birlikte uygulanması çok sayıda klinik ilaç-ilaç etkileşim çalışmasında incelenmiştir (bkz. bölüm 4.5).
Eliminasyon
Asenapin ile bir bileşiktir Boşluk yüksek, intravenöz uygulamadan sonra 52 l / s. Bir kütle dengesi çalışmasında, radyoaktif dozun çoğu idrar (yaklaşık %50) ve feçes (yaklaşık %40) ile atılırken, sadece küçük bir miktarı (%5-16) değişmemiş bileşik olarak feçesle atılır. dağıtım aşamasında, asenapinin terminal yarı ömrü yaklaşık 24 saattir.
Doğrusallık / doğrusal olmama
Dozu günde iki kez 5 mg'dan 10 mg'a çıkarmak (çift artış), maruziyet ve maksimum konsantrasyonda daha az doğrusal (1,7 kat) artışlarla sonuçlanır. Bir dozun uygulanmasıyla Cmaks ve EAA'daki orantılı artıştan daha az artış, dilaltı uygulamadan sonra oral mukozanın absorpsiyon kapasitesindeki sınırlamalara bağlanabilir.
Çift günlük dozun uygulanması sırasında, kararlı hal 3 günde elde edilir. Genel olarak, asenapin allo'nun farmakokinetiği kararlı hal tek doza benzer.
Özel popülasyonlarda farmakokinetik özellikler
Karaciğer yetmezliği
Asenapin farmakokinetiği, hafif (Child-Pugh Sınıf A) veya orta (Child-Pugh Sınıf B) karaciğer yetmezliği olan hastalar ile normal karaciğer fonksiyonu olan hastalar arasında benzerdi. Şiddetli karaciğer yetmezliği olan hastalarda (Child-Pugh Sınıf C), asenapin maruziyetinde 7 kat artış gözlenmiştir (bkz. bölüm 4.2).
Böbrek yetmezliği
Tek bir 5 mg dozun ardından asenapin farmakokinetiği, değişen derecelerde böbrek yetmezliği olan hastalar ile normal böbrek fonksiyonu olan hastalar arasında benzerdi.
Kreatinin klerensi 15 ml/dak'nın altında olan şiddetli böbrek yetmezliği olan hastalarda asenapin ile deneyim yoktur.
Yaşlılar
Yaşlı hastalarda (65-85 yaş arası), asenapine maruziyet genç yetişkinlere göre yaklaşık %30 daha fazladır.
Pediatrik popülasyon (Ergenler)
Günde iki kez 5 mg'lık günlük dozda, ergen hastalarda (12-17 yaş) asenapin farmakokinetiği yetişkinlerde görülene benzerdir. Ergenlerde, günde iki kez 10 mg doz, günde iki kez 5 mg doza kıyasla maruziyette bir artışa neden olmadı.
Seks
Popülasyon farmakokinetik analizi, asenapin farmakokinetiğinde cinsiyete bağlı farklılıklara dair bir kanıt bulunmadığını göstermiştir.
Yarış
Popülasyon farmakokinetik analizi, asenapin farmakokinetiği üzerinde ırkın ilgili klinik etkilerinin tanımlanmadığını göstermiştir.
Sigara içmek
Bir "popülasyon farmakokinetik analizi, CYP1A2'yi indükleyen sigara içmenin Boşluk asenapina tarafından. Özel bir çalışmada, 5 mg dilaltı dozunun uygulanması sırasında sigara içmenin asenapin farmakokinetiği üzerinde hiçbir etkisi olmamıştır.
05.3 Klinik öncesi güvenlik verileri
Klinik dışı veriler, konvansiyonel çalışmalara dayalı olarak insanlar için özel bir tehlike ortaya koymamaktadır. farmakolojik güvenlik. Sıçanlarda ve köpeklerde yürütülen tekrarlanan doz toksisitesi çalışmaları, esas olarak sedasyon gibi doz sınırlayıcı farmakolojik etkiler göstermiştir. Ayrıca meme bezleri üzerinde prolaktin aracılı etkiler ve östrus döngüsü bozuklukları gözlenmiştir. Köpeklerde, oral yoldan uygulanan yüksek dozlar, kronik intravenöz uygulamadan sonra gözlenmeyen hepatotoksisite ile sonuçlanmıştır. Asenapin, melanin içeren dokular için belirli bir afiniteye sahiptir. Ancak, ne kadar test edildi laboratuvar ortamında, fototoksisiteden ari olduğu bulundu. Ayrıca, kronik olarak asenapin ile tedavi edilen köpeklerin gözlerinin histopatolojik incelemesi, herhangi bir oküler toksisite belirtisi göstermedi, bu da fototoksik bir tehlikenin olmadığını gösterdi. Asenapin bir dizi testte genotoksisite göstermedi. Sıçanlarda ve farelerde yürütülen deri altı karsinojenisite çalışmalarında, tümör insidansında herhangi bir artış gözlenmemiştir.Klinik olmayan çalışmalarda etkiler, yalnızca maksimum insan maruziyetini yeterince aştığı kabul edilen maruziyetlerde gözlenmiştir, bu da klinik kullanımla zayıf alaka düzeyine işaret etmektedir.
Asenapin, sıçanlarda fertiliteyi bozmadı ve sıçanlarda ve tavşanlarda herhangi bir teratojenik etki göstermedi. Sıçanlarda ve tavşanlarda üreme toksikolojisi çalışmalarında embriyotoksisite bulunmuştur.Asenapin hafif maternal toksisiteye ve hafif fetal iskelet gelişiminde gecikmeye neden olmuştur.Organogenez döneminde hamile tavşanlara oral uygulamadan sonra, asenapin, 15 mg yüksek doz ile ağırlığı olumsuz etkilemiştir. .kg-1 günde iki kez. Bu dozda hayvanın fetal ağırlığı azalmıştır.Asenapin hamile tavşanlara intravenöz olarak uygulandığında, embriyotoksisite belirtisi gözlenmemiştir.Sıçanlarda, oral uygulamadan sonra embriyofetal toksisite (implantasyon sonrası kayıpta artış, fetal ağırlıkta azalma ve gecikmiş kemikleşme) gözlenmiştir. veya organogenez veya gebelik sırasında intravenöz uygulama. Gebelik ve emzirme döneminde tedavi edilen dişi sıçanların yavrularında neonatal mortalitede bir artış gözlemlendi. çapraz teşvik asenapine bağlı peri- ve postnatal ölümlerin annelerin değişen emzirme davranışından ziyade bebeklerin eksikliğinden kaynaklandığı sonucuna varılmıştır.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
Jöle
Mannitol (E421)
06.2 Uyumsuzluk
İlgili değil.
06.3 Geçerlilik süresi
3 yıl.
06.4 Depolama için özel önlemler
Işıktan ve nemden korumak için orijinal ambalajında saklayınız.
Bu tıbbi ürün herhangi bir özel saklama sıcaklığı gerektirmez.
06.5 İç ambalajın yapısı ve paketin içeriği
Karton başına 20, 60 veya 100 dilaltı tabletlik kartonlarda çıkarılabilir folyolu alüminyum / alüminyum blister.
Tüm paket boyutları pazarlanmayabilir.
06.6 Kullanım ve kullanım talimatları
Kullanılmayan ilaçlar ve bu ilaçtan elde edilen atıklar yerel yönetmeliklere uygun olarak atılmalıdır.
07.0 PAZARLAMA YETKİ SAHİBİ
N.V. Organon, Kloosterstraat 6, NL-5349 AB Oss, Hollanda
08.0 PAZARLAMA YETKİ NUMARASI
AB / 1/10/640/004
040761049
AB / 1/10/640/005
040761052
AB / 1/10/640/006
040761064
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
İlk izin tarihi: 1 Eylül 2010
10.0 METİN REVİZYON TARİHİ
02/2013



















-cos-cause-e-disturbi-associati.jpg)