Aktif maddeler: Azitromisin
ZITROMAX 100 mg oral süspansiyon için toz
ZITROMAX 150 mg oral süspansiyon için toz
ZITROMAX 200 mg oral süspansiyon için toz
ZITROMAX 300 mg oral süspansiyon için toz
ZITROMAX 400 mg oral süspansiyon için toz
Paket boyutları için Zithromax paket ekleri mevcuttur: - ZITROMAX 250 mg sert kapsüller
- ZITROMAX 100 mg toz oral süspansiyon, ZITROMAX 150 mg toz oral süspansiyon, ZITROMAX 200 mg toz oral süspansiyon, ZITROMAX 300 mg toz oral süspansiyon, ZITROMAX 400 mg oral süspansiyon toz
- ZITROMAX 200 mg / 5 ml oral süspansiyon için toz
- Uzatılmış salımlı oral süspansiyon için ZITROMAX 2 g granül
- ZITROMAX 500 mg film kaplı tabletler, ZITROMAX 200 mg / 5 ml oral süspansiyon için toz
Zitromax neden kullanılır? Bu ne için?
FARMAKOTERAPÖTİK KATEGORİ
Sistemik kullanım için antibakteriyeller; makrolidler.
TEDAVİ ENDİKASYONLARI
Azitromisine duyarlı mikropların neden olduğu enfeksiyonların tedavisi.
- üst solunum yolu enfeksiyonları (orta kulak iltihabı, sinüzit, bademcik iltihabı ve farenjit dahil),
- alt solunum yolu enfeksiyonları (bronşit ve pnömoni dahil),
- odontostomatolojik enfeksiyonlar,
- cilt ve yumuşak doku enfeksiyonları,
- gonokokal olmayan üretrit (Chlamydia trachomatis'ten),
- yumuşak ülser (Haemophilus ducreyi'den).
Kontrendikasyonlar Zithromax kullanılmamalıdır
Etkin madde azitromisine, eritromisine, makrolid veya ketolid antibiyotiklerinden herhangi birine veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
Kullanım Önlemleri Zithromax'ı almadan önce bilmeniz gerekenler
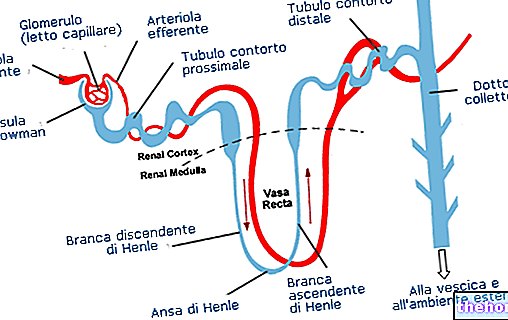
Değişen böbrek fonksiyonu
Şiddetli böbrek yetmezliği olan hastalarda (GFR <10 ml/dak), azitromisine sistemik maruziyette %33'lük bir artış gözlenmiştir.
Hafif ila orta derecede böbrek yetmezliği (GFR 10-80 mL/dak) olan hastalarda doz ayarlaması gerekli değildir, şiddetli böbrek yetmezliği olanlarda (GFR <10 mL/dak) dikkatli olunmalıdır.
hepatotoksisite
Azitromisinin başlıca eliminasyon yolu karaciğer olduğundan, majör karaciğer hastalığı olan hastalarda kullanımı dikkatle yapılmalıdır.Azitromisin ile karaciğer yetmezliği, hepatit, kolestatik sarılık, hepatik nekroz ve fulminan hepatit vakaları bildirilmiştir. Bazıları ölümcül olabilen karaciğer yetmezliği (bkz. "Yan Etkiler") Bazı hastalarda daha önce karaciğer hastalığı olmuş veya başka hepatotoksik tıbbi ürünler almış olabilir Hızlı başlangıçlı asteni gibi karaciğer fonksiyon bozukluğu belirti ve semptomlarının geliştiği durumlarda sarılık, koyu renkli idrar, kanama eğilimi veya hepatik ensefalopati ile ilişkili karaciğer fonksiyon testleri/testleri hemen yapılmalıdır.
Karaciğer fonksiyon bozukluğu belirtileri ortaya çıkarsa, azitromisin tedavisini derhal sonlandırın.
Ergotamin türevleri
Ergotamin türevleri ile tedavi edilen hastalarda makrolid antibiyotiklerin birlikte uygulanması ergotizm krizlerini hızlandırmıştır.Şu anda ergotamin ve azitromisin arasında bir etkileşim olasılığına ilişkin veri bulunmamaktadır. Ancak teorik ergotizm olasılığı nedeniyle azitromisin ve ergotamin aynı anda uygulanmamalıdır.
süperenfeksiyonlar
Diğer herhangi bir antibiyotik preparatında olduğu gibi, mantarlar dahil hassas olmayan mikroorganizmalarla olası süperenfeksiyon oluşumu için özel gözlem önerilir.
Etkileşimler Hangi ilaçlar veya yiyecekler Zithromax'ın etkisini değiştirebilir?
Yakın zamanda başka ilaçlar aldıysanız, reçetesizler de dahil olmak üzere doktorunuza veya eczacınıza söyleyiniz.
antasitler
Antasitler ve azitromisinin birlikte uygulanmasının etkilerine ilişkin bir farmakokinetik çalışmada, maksimum serum konsantrasyonlarında yaklaşık %25'lik bir azalma gözlemlenmesine rağmen, azitromisinin biyoyararlanımı üzerinde hiçbir etki gözlenmemiştir.Bu nedenle, azitromisin ve antasitler ile tedavi gören hastalar iki ilaç aynı anda.Uzun salımlı oral süspansiyon için azitromisin granüllerinin tek doz 20 ml ko-magaldrox (alüminyum hidroksit ve magnezyum hidroksit) ile birlikte uygulanması, azitromisinin emilim oranını ve derecesini etkilemedi.
setirizin
Sağlıklı gönüllülerde, kararlı durumda 5 günlük azitromisin ve 20 mg setirizin rejiminin birlikte uygulanması, QT aralığında hiçbir farmakokinetik etkileşim veya önemli değişiklik göstermedi.
didanosin
Altı HIV pozitif hastada günlük azitromisin 1200 mg/gün ve didanozin 400 mg/gün dozlarının birlikte uygulanmasının, plaseboya kıyasla didanosinin kararlı durum farmakokinetiği üzerinde hiçbir etkisi olmadığı gözlenmiştir.
Digoksin (P-glikoprotein substratları)
Azitromisin dahil olmak üzere, digoksin gibi P-glikoprotein substratları ile makrolid antibiyotiklerin alımının, P-glikoprotein substratlarının serum seviyelerinin artmasına neden olduğu bildirilmiştir. Bu nedenle, azitromisin ve digoksin gibi P-glikoprotein substratları birlikte alındığında serum digoksin düzeylerinde bir artış olasılığı göz önünde bulundurulmalıdır. Azitromisin tedavisinin kesilmesi sırasında ve sonrasında olası yüksek digoksin seviyeleri için klinik izleme ve izleme gereklidir.
Zidovudin
Azitromisinin 1000 mg'lık tek dozlarının ve çoklu 1200 mg veya 600 mg'lık dozların uygulanması, periferik mononükleer hücrelerde zidovudinin veya glukuronid metabolitinin plazma farmakokinetiğini veya idrarla atılımını önemli ölçüde değiştirmemiştir. Bu bulgunun önemi belirsizdir, ancak yine de hastaya faydalı olabilir.
Azitromisin, hepatik sitokrom P450 sistemi ile önemli ölçüde etkileşime girmez, eritromisin ve diğer makrolidlerle olduğu gibi farmakokinetik etkileşimlere dahil olması beklenmez. Aslında azitromisin ile, metabolitlerinin kompleksi yoluyla hepatik sitokrom P450'nin indüksiyonu veya inaktivasyonu yoktur.
ergotamin
Olası ergotizm başlangıcı nedeniyle, azitromisin ve ergotamin türevlerinin birlikte kullanımı önerilmez (bkz. "Kullanım Önlemleri").
Azitromisin ile önemli sitokrom P450 aracılı metabolik aktivitenin bilindiği aşağıdaki ilaçlar arasında farmakokinetik çalışmalar yapılmıştır.
HMG-CoA redüktaz inhibitörleri (Statinler)
Atorvastatin (10 mg/gün) ve azitromisinin (500 mg/gün) birlikte uygulanması, atorvastatinin plazma konsantrasyonlarını değiştirmedi (bir HMG CoA redüktaz inhibisyon testine göre) ve bu nedenle HMG CoA redüktaz aktivitesinde değişikliklere neden olmadı. Bununla birlikte, azitromisin ve statin alan hastalarda pazarlama sonrası rabdomiyoliz raporları olmuştur.
karbamazepin
Sağlıklı gönüllülerde yürütülen bir etkileşim çalışmasında, eşzamanlı azitromisin alan hastalarda karbamazepin veya aktif metabolitinin plazma seviyeleri üzerinde anlamlı bir etki gözlenmemiştir.
simetidin
Azitromisinden 2 saat sonra uygulanan tek doz simetidinin etkilerini değerlendirmek için yürütülen bir farmakokinetik çalışmada, azitromisinin farmakokinetiğinde herhangi bir değişiklik kanıtı bulunmamıştır.
siklosporin
Siklosporinin Cmax ve AUC0-5'inde önemli artışlar. Bu nedenle, iki ilacın olası eşzamanlı uygulaması dikkatli olmayı gerektirir.İki ilacın birlikte uygulanması kesinlikle gerekliyse, siklosporin seviyeleri dikkatle izlenmeli ve ikincisinin dozajı buna göre değiştirilmelidir.
Efavirenz
7 gün boyunca günde tek doz azitromisin (600 mg) ve efavirenz (400 mg) birlikte uygulanması, klinik olarak anlamlı farmakokinetik etkileşimler oluşturmadı.
flukonazol
Tek doz azitromisinin (1200 mg) birlikte uygulanması, tek doz flukonazolün (800 mg) farmakokinetiğini değiştirmemiştir. Azitromisinin toplam maruz kalma süresi ve yarı ömrü, flukonazol ile birlikte uygulamadan etkilenmezken, Cmax'ta klinik olarak önemsiz bir azalma (%18) gözlendi.
indinavir
Tek doz azitromisinin (1200 mg) birlikte uygulanması, 800 mg'lık dozlarda 5 gün boyunca günde üç kez uygulanan indinavirin farmakokinetiği üzerinde istatistiksel olarak anlamlı bir etki göstermedi.
metilprednizolon
Sağlıklı gönüllülerde yürütülen bir farmakokinetik çalışma, azitromisinin metilprednizolonun farmakokinetiğini önemli ölçüde etkilemediğini göstermiştir.
Midazolam
Sağlıklı gönüllülerde, 3 gün boyunca günde 500 mg azitromisinin birlikte uygulanması, tek bir 15 mg midazolam dozunun farmakokinetiği ve farmakodinamiğinde klinik olarak anlamlı değişikliklere yol açmamıştır.
nelfinavir
Azitromisin (1200 mg) ve nelfinavirin kararlı durumda (günde üç kez 750 mg) birlikte uygulanması, azitromisin konsantrasyonlarında artışa neden olmuştur.
rifabutin
Azitromisin ve rifabutinin birlikte uygulanması, iki ilacın serum konsantrasyonlarını değiştirmez. İki ilacı aynı anda alan bazı hastalarda nötropeni vakaları gözlenmiştir; rifabutinin nötropeniye neden olduğu bilinmesine rağmen, yukarıdaki nötropeni atakları ile rifabutinazitromisin kombinasyonu arasında nedensel bir ilişki kurmak mümkün olmamıştır (bkz. "İstenmeyen etkiler").
sildenafil
Sağlıklı erkek gönüllülerde, azitromisinin (3 gün boyunca 500 mg/gün) sildenafilin veya onun dolaşımdaki majör metabolitinin EAA ve Cmaks değerleri üzerinde hiçbir etkisi olmamıştır.
teofilin
Sağlıklı gönüllülere azitromisin ve teofilinin birlikte uygulanması, iki ilaç arasında klinik olarak anlamlı bir etkileşim göstermedi.
terfenadin
Farmakokinetik çalışmalar, azitromisin ve terfenadin arasında herhangi bir etkileşim olmadığını ortaya koymuştur. Böyle bir etkileşim olasılığının tamamen dışlanamadığı bazı nadir vakalar bildirilmiştir; ancak, etkileşimin gerçekleştiğine dair hiçbir bilimsel kanıt yoktur.
triazolam
14 sağlıklı gönüllüde, 1. günde 500 mg azitromisin ve 2. günde 250 mg ve 2. günde 0.125 mg triazolamın birlikte uygulanması, triazolam ve plaseboya kıyasla triazolamın farmakokinetik değişkenleri üzerinde anlamlı bir etkiye sahip değildi.
Trimetoprim / Sülfametoksazol
7 gün boyunca trimetoprim / sülfametoksazol (160 mg / 800 mg) ve azitromisinin (1200 mg) birlikte uygulanmasından sonra, 7. günde doruk konsantrasyonlar, maruziyet süresi veya idrarla atılım üzerinde anlamlı bir etki olmamıştır. Hem trimetoprim hem de sülfametoksazol Azitromisinin serum konsantrasyonları diğer çalışmalarda bulunanlara benzerdir.
Kumarin tipi oral antikoagülanlar
Sağlıklı gönüllülerde yapılan bir farmakokinetik çalışmada, azitromisinin 15 mg'lık tek bir varfarin dozunun antikoagülan etkisini değiştirmediği gösterilmiştir. Pazarlama sonrası aşamada, azitromisin ve kumarin tipi oral antikoagülanların birlikte uygulanmasının ardından antikoagülan etkisinin güçlenmesi vakaları rapor edilmiştir. kumarin tipi antikoagülan alan hastalara azitromisin verilirken protrombin süresini izleyin.
Uyarılar Şunları bilmek önemlidir:
Aşırı duyarlılık ve anafilaktik reaksiyonlar
Eritromisin ve diğer makrolidlerde olduğu gibi, anjiyoödem ve anafilaksi (nadiren ölümcül) dahil olmak üzere ciddi alerjik reaksiyonlar, Stevens Johnson sendromu (SJS), toksik epidermal nekroliz (TEN) (nadiren ölümcül) dahil dermatolojik reaksiyonlar ve eozinofili ve eozinofili ile ilaç erüpsiyonu gözlenmiştir. sistemik semptomlar (DRESS). Azitromisin uygulamasıyla ilişkili bu reaksiyonların bazıları nükslerle sonuçlanmıştır ve bu nedenle uzun süreli gözlem ve tedavi gerektirir.
Alerjik reaksiyon durumunda ilaç kesilmeli ve uygun tedavi başlatılmalıdır. Doktorlar, semptomatik tedavi kesildiğinde alerjik semptomların geri dönebileceğini bilmelidir.
Clostridium difficile ilişkili ishal
Azitromisin de dahil olmak üzere hemen hemen tüm antibiyotiklerin kullanımıyla, hafif diyareden ölümcül kolite kadar değişen şiddette Clostridium difficile ile ilişkili diyare (CDAD) vakaları bildirilmiştir. Antibiyotiklerle tedavi, kolonun normal florasını değiştirir ve C. difficile'nin aşırı büyümesine yol açar.
C. difficile, ishal gelişimine katkıda bulunan A ve B toksinlerini üretir. Aşırı toksin üreten C. difficile suşları, bu enfeksiyonlar tipik olarak antibakteriyel tedaviye dirençli olduğundan ve sıklıkla kolektomi gerektirdiğinden, artan morbidite ve mortalite oranlarına neden olur. Antibiyotik tedavisini takiben diyare ile başvuran tüm hastalarda C. difficile ile ilişkili diyare olasılığı düşünülmelidir. Antibiyotik uygulamasından iki ay sonra bile C. difficile ile ilişkili diyare vakaları bildirildiği için dikkatli bir tıbbi öykü gereklidir.
QT aralığının uzaması
Azitromisin dahil makrolidlerle tedavide, EKG'de kardiyak repolarizasyonda ve QT aralığında uzama bulundu, bu da kardiyak aritmi ve torsades de pointes geliştirme riskine yol açar (bkz. "İstenmeyen Etkiler"). Bu nedenle, aşağıdaki durumlar kalp durmasına yol açabilen ventriküler aritmi riskinde artışa (torsades de pointes dahil) yol açabileceğinden, eşlik eden proaritmik durumları olan hastalarda (özellikle kadınlar ve yaşlı hastalarda) azitromisin dikkatle uygulanmalıdır.
Reçete yazanlar, aşağıdakiler gibi risk altındaki hasta gruplarında azitromisinin yarar-riskini değerlendirirken, ölümcül olabilen QT aralığı uzaması riskini göz önünde bulundurmalıdır:
- QT aralığının doğuştan veya belgelenmiş uzaması olan hastalar;
- Sınıf IA antiaritmikler (kinidin ve prokainamid) ve Sınıf III (dofetilid, amiodaron ve sotalol), sisaprid ve terfenadin gibi QT aralığını uzatan diğer aktif maddeler, pimozid gibi antipsikotik ilaçlar, sitalopram gibi antidepresanlar, florokinolonlar gibi diğer aktif maddelerle tedavi edilen hastalar moksifloksasin, levofloksasin ve klorokin gibi.
- Elektrolit bozukluğu olan hastalar, özellikle hipokalemi ve hipomagnezemi vakalarında;
- Klinik olarak anlamlı bradikardisi, kardiyak aritmisi veya şiddetli kalp yetmezliği olan hastalar;
- QT aralığı değişikliğinin (ilaca bağlı) etkilerine daha duyarlı olabilecek kadınlar ve yaşlılar.
Miyastenia Gravis
Azitromisin alan hastalarda miyastenia gravis semptomlarının alevlenmesi ve miyastenik sendromun ilk başlangıcı bildirilmiştir (bkz. "İstenmeyen etkiler").
Oral süspansiyon için toz sakaroz içerir.
Eğer daha önceden doktorunuz tarafından bazı şekerlere karşı intoleransınız olduğu söylenmişse, bu tıbbi ürünü almadan önce doktorunuzla temasa geçiniz.
Ayrıca sakaroz içeriği nedeniyle diyabetik hastaların tedavisinde dikkatli olunmalıdır.
Paket başına sakaroz içeriği aşağıdaki gibidir:
- Zithromax 100 mg: her poşet 1.93 g sakaroz içerir;
- Zithromax 150 mg: her poşet 2.90 g sakaroz içerir;
- Zithromax 200 mg: her poşet 3.87 g sakaroz içerir;
- Zithromax 300 mg: her poşet 5.82 g sakaroz içerir;
- Zithromax 400 mg: her poşet 7.75 g sakaroz içerir.
Doğurganlık, hamilelik ve emzirme
Herhangi bir ilaç almadan önce doktorunuza veya eczacınıza danışınız.
Azitromisinin gebelik sırasında kadınlarda kullanımına ilişkin yeterli veri yoktur Azitromisinin gebelik sırasındaki güvenliği belirlenmemiştir. Bu nedenle azitromisin hamilelikte ancak yarar riskten fazlaysa kullanılmalıdır.
Doğurganlık
Sıçanlarda yapılan doğurganlık çalışmalarında, azitromisin uygulamasını takiben doğurganlık hızında bir azalma kaydedilmiştir. Bu bulguların insanlarla ilgisi bilinmemektedir.
Gebelik
Hayvan üreme çalışmaları, orta derecede toksik maternal konsantrasyonlara ulaşana kadar ölçekli dozlar kullanılarak yürütülmüştür.Bu çalışmalardan, azitromisine bağlı olarak fetüs için herhangi bir tehlike olduğuna dair herhangi bir kanıt bulunmamıştır.Hayvanlarda yapılan üreme toksikolojisi çalışmalarında, azitromisinin plasentayı geçtiği gösterilmiştir, ancak hiçbir teratojenik etkiler gözlendi.
Besleme zamanı
Azitromisinin anne sütüne geçtiği rapor edilmiştir.Bu nedenle, azitromisin sadece emziren kadınlarda, doktorun görüşüne göre potansiyel yararın bebeğe yönelik potansiyel riskten daha fazla olduğu durumlarda kullanılmalıdır.
Araç ve makine kullanma yeteneği üzerindeki etkiler
Azitromisinin hastaların araç veya makine kullanma yeteneğini etkileyebileceğini gösteren hiçbir veri yoktur.
Dozaj ve kullanım yöntemi Zithromax nasıl kullanılır: Dozaj
Pediyatrik popülasyon:
3 ardışık gün boyunca 10 mg / kg / gün. 45 kg veya daha ağır olan çocuklar için yetişkinlerle aynı doz (arka arkaya üç gün boyunca 500 mg / gün) kullanılabilir.
Çocuklarda akut otitis media tedavisi için önerilen doz art arda 3 gün 10 mg/kg/gün veya tek seferde 30 mg/kg'dır.
Çocuklarda streptokokal farenjit tedavisi için hem tek seferde hem de ardışık üç gün boyunca hem 10 mg/kg hem de 20 mg/kg dozunun etkili olduğu gösterilmiştir; ancak günlük 500 doz mg İki dozajla yapılan klinik çalışmalarda, örtüşen etkinlik gözlemlendi, ancak 20 mg / kg / gün'de daha fazla bakteriyel eradikasyon görüldü. Ancak Streptococcus pyogenes farenjit tedavisinde ve romatizmal ateş profilaksisinde penisilin tercih edilen ilaçtır.
Herhangi bir pediatrik tedavi için önerilen maksimum toplam doz 1500 mg'dır.
Yaşlılar
Aynı dozaj rejimi yaşlı hastalara da uygulanabilir.Yaşlı hastalar kardiyak aritmilere daha yatkın olduklarından, kardiyak aritmiler ve torsades de pointes geliştirme riskinden dolayı özellikle dikkatli olunması önerilir ("Özel uyarılar" bölümüne bakınız).
Karaciğer veya böbrek sorunları olan hastalar:
Karaciğer veya böbrek sorunları olan hastalar, normal dozun değiştirilmesi gerekebileceğinden doktorlarını bilgilendirmelidir. Hafif ila orta şiddette böbrek yetmezliği (GFR 10-80 mL/dak) olan hastalarda doz ayarlaması gerekli değildir ve şiddetli böbrek yetmezliği olanlarda (GFR <10 mL/dak) dikkatli olunmalıdır ("Kullanım Önlemleri" bölümüne bakınız). ) Hafif ila orta şiddette karaciğer yetmezliği olan hastalarda normal karaciğer fonksiyonuna sahip hastalardaki ile aynı doz kullanılabilir (bkz. "Kullanım Önlemleri").
İlaç her zaman tek bir günlük dozda uygulanmalıdır.
Oral süspansiyon için ZITROMAX (azitromisin) tozu, aç karnına veya yemeklerden sonra alınabilir. Ürünü uygulamadan önce gıda alımı, azitromisinin neden olduğu gastrointestinal yan etkileri azaltabilir.
Poşeti açın ve içindekileri yarım bardak suya dökün, kullanmadan önce iyice çalkalayın. Gerekli doz seyreltmeden hemen sonra alınmalı ve önceden hazırlanmamalıdır.
Aşırı doz Zithromax'ı çok fazla aldıysanız ne yapmalısınız?
Önerilenden daha yüksek dozlarda meydana gelen yan etkiler, normal dozlarda görülenlere benzerdi.
ZITROMAX'ın kazara yutulması/aşırı dozda alınması durumunda derhal doktorunuza haber veriniz veya size en yakın hastaneye başvurunuz.
ZITROMAX'ın kullanımıyla ilgili herhangi bir sorunuz varsa, doktorunuza veya eczacınıza sorunuz.
Yan Etkiler Zithromax'ın yan etkileri nelerdir?
Tüm ilaçlar gibi ZITROMAX da yan etkilere neden olabilir, ancak bu yan etkiler herkeste görülmez.
Aşağıdaki tablo, klinik çalışmaların yürütülmesi sırasında ve pazarlama sonrası gözetim sırasında tespit edilen advers reaksiyonları sistem organ sınıfına ve sıklığa bölünmüş olarak listelemektedir. Pazarlama sonrası gözetim sırasında tespit edilen advers reaksiyonlar italik olarak gösterilmiştir. Sıklık aşağıdaki parametreler kullanılarak tanımlanır: Çok yaygın (≥1 / 10); Yaygın (≥ 1/100,
Klinik çalışmaların ve pazarlama sonrası sürveyansın sonuçlarına göre azitromisin ile olası veya muhtemel korelasyonu olan advers reaksiyonlar.
* sadece infüzyonluk çözelti için toz için
Klinik çalışmalardan ve pazarlama sonrası gözetimden elde edilen deneyimlere dayalı olarak Mycobacterium avium Kompleksinin profilaksisi ve tedavisi ile olası veya muhtemelen ilişkili advers reaksiyonlar Bu advers reaksiyonlar, tip veya sıklık bakımından hemen salınan veya uzun süreli salınan formülasyonlarla bildirilenlerden farklıdır:
Kullanma talimatında yer alan talimatlara uyulması, istenmeyen etki riskini azaltır.
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuzla veya eczacınızla konuşun.Bu kullanma talimatında listelenmeyen olası yan etkiler de buna dahildir. İstenmeyen etkiler doğrudan "www.agenziafarmaco.it/it/responsabili" adresindeki ulusal raporlama sistemi aracılığıyla da rapor edilebilir. Yan etkileri bildirerek, bu ilacın güvenliği hakkında daha fazla bilgi sağlamaya yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
Son kullanma tarihi: paketin üzerinde belirtilen son kullanma tarihine bakın. Belirtilen son kullanma tarihi, bozulmamış ve doğru şekilde saklanmış ambalajdaki ürünü ifade eder.
Uyarı: Paket üzerinde belirtilen son kullanma tarihinden sonra ilacı kullanmayınız.
Sulandırıldıktan sonra oral süspansiyon oda sıcaklığında 10 gün stabildir.
BELLİ BOZULMA BELİRTİLERİ DURUMUNDA KULLANMAYIN.
İlaçlar atık su veya evsel atıklar yoluyla bertaraf edilmemelidir.Artık kullanmadığınız ilaçları nasıl bertaraf edeceğinizi eczacınıza sorunuz.Bu, çevrenin korunmasına yardımcı olacaktır.
Diğer bilgiler
KOMPOZİSYON
ZITROMAX 100 mg oral süspansiyon için toz
Her 2.09 gram toz poşeti şunları içerir:
- Aktif madde: Azitromisin dihidrat 104.8 mg, 100 mg azitromisin bazına eşittir
ZITROMAX 150 mg oral süspansiyon için toz
Her 3.14 gram toz poşeti şunları içerir:
- Aktif madde: Azitromisin dihidrat 157.2 mg, azitromisin baz 150 mg'a eşittir
ZITROMAX 200 mg oral süspansiyon için toz
Her 4.18 gram toz poşeti şunları içerir:
- Aktif madde: Azitromisin dihidrat 209.6 mg, 200 mg azitromisin bazına eşittir
ZITROMAX 300 mg oral süspansiyon için toz
Her 6.28 gram toz poşeti şunları içerir:
- Aktif madde: Azitromisin dihidrat 314.4 mg, 300 mg azitromisin bazına eşittir
ZITROMAX 400 mg oral süspansiyon için toz
Her 8.36 gram toz poşeti şunları içerir:
- Aktif madde: Azitromisin dihidrat 419.2 mg, azitromisin baz 400 mg'a eşittir
Yardımcı maddeler: Tribazik sodyum fosfat susuz, hidroksipropilselüloz, ksantan zamkı, kiraz aroması, vanilyalı krema, muz aroması, sakaroz.
FARMASÖTİK FORM VE İÇERİĞİ
ZITROMAX 100 mg oral süspansiyon tozu: Oral süspansiyon için 3 poşet toz içeren paket. Her poşet 100 mg azitromisin bazı içerir.
ZITROMAX 150 mg oral süspansiyon tozu: Oral süspansiyon için 3 poşet toz içeren paket. Her poşet 150 mg azitromisin bazı içerir.
ZITROMAX 200 mg oral süspansiyon tozu: Oral süspansiyon için 3 poşet toz içeren paket. Her poşet 200 mg azitromisin bazı içerir.
ZITROMAX 300 mg oral süspansiyon tozu: Oral süspansiyon için 3 poşet toz içeren paket. Her poşet 300 mg azitromisin bazı içerir.
ZITROMAX 400 mg oral süspansiyon tozu: Oral süspansiyon için 3 poşet toz içeren paket. Her poşet 400 mg azitromisin bazı içerir.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.