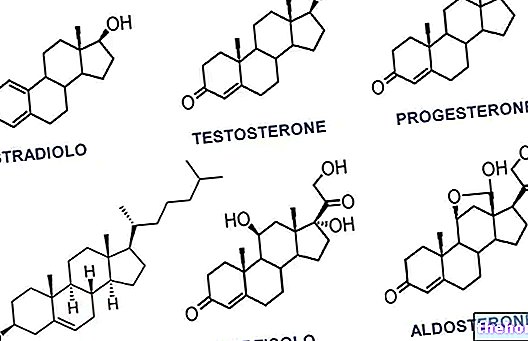
Protein yapılarını ve değiştirilmiş olanları oluşturan yirmi amino asitten bahsetmek için en az on iki özelleşmiş metabolik yolu tanımlamak gerekir.
Fakat hücreler neden amino asitleri katabolize etmek için enerji gerektiren (örneğin enzimlerin katalitik bölgelerini yeniden oluşturmak için) bu kadar çok metabolik yol kullanırlar? Hemen hemen tüm amino asitlerden, özel yollardan, küçük bir kısmı enerji üretmek için kullanılan (örneğin, glukoneogenez ve keton cisimlerinin yolu yoluyla) kullanılan, ancak her şeyden önce kompleks oluşumuna yol açan metabolitler elde etmek mümkündür. yüksek sayıda karbon atomlu moleküller (örneğin fenilalanin ve tirozinden, bu amaç için özelleşmiş adrenal bezlerde hormonlar üretilir); bir yandan amino asitlerden enerji üretmek basit olsaydı, diğer yandan küçük moleküllerden başlayarak karmaşık moleküller oluşturmak karmaşık olurdu: amino asitlerin katabolizması, daha büyük türler elde etmek için iskeletlerinden yararlanmalarına izin verir.
Sağlıklı bir birey tarafından günde iki veya üç hektogram amino asit bozulur: bunların 60-100 g'ı diyetle alınan proteinlerden elde edilir, ancak organizmanın ayrılmaz bir parçası olan proteinlerin normal döngüsünden 2 hektogramdan fazlası elde edilir ( Bu proteinlerin redoks işlemlerinden zarar gören amino asitleri başkaları ile yer değiştirir ve katabolize olur).
Amino asitler ATP açısından bir enerji katkısı sağlar: a-amino grubu çıkarıldıktan sonra, uygun dönüşümleri takiben amino asitlerin geriye kalan karbonlu iskeleti krebs döngüsüne girebilir. Ayrıca, besin kaynağı eksik olduğunda ve glikoz miktarı azaldığında, glukoneogenez aktive olur: glukoneogenetik amino asitlerin, uygun modifikasyonlardan sonra glukoneogeneze katılabilenler olduğu söylenir; glukoneogenetik amino asitler, dönüştürülebilen amino asitlerdir. piruvat veya fumarat içinde (fumarat, mitokondriyi terk eden malata dönüştürülebilir ve sitoplazmada, fosfoenol piruvatın elde edilebildiği oksaloasetata dönüştürülebilir). sirke-asetat.
Az önce açıklanan çok önemli bir husus çünkü amino asitler, hemen aç kalındığında şeker eksikliğini giderebilir; Açlık devam ederse, iki gün sonra lipid metabolizması devreye girer (çünkü protein yapılarına çok fazla saldırılamaz), bu aşamada glukoneogenez çok sınırlı olduğu için yağ asitleri asetil koenzim A ve keton cisimlerine dönüştürülür. Daha fazla açlıktan, beyin keton cisimlerini kullanmaya da adapte olur.
α-amino grubunun amino asitlerden transferi, bir transaminasyon reaksiyonu yoluyla gerçekleşir; bu reaksiyonu katalize eden enzimler, aslında derler ki, transaminazlar (veya amino transferaz). Bu enzimler, aldehit grubuna müdahale eden piridoksal fosfat adı verilen enzimatik bir kofaktör kullanır. Piridoksal fosfat, esas olarak sebzelerde bulunan bir vitamin (B6) olan piridoksinin fosforilasyon ürünüdür.
Transaminazlar aşağıdaki özelliklere sahiptir:
Bir ketoglutarat-glutamat α çifti için yüksek özgüllük;
İkinci çiftin adını taşırlar.
Transaminaz enzimleri her zaman a ketoglutarat-glutamat çiftini içerir ve ilgili ikinci çifte göre ayırt edilir.
Örnekler:
L"aspartat transaminaz yani GOT (Glutamat-Ossal asetat Transaminaz): enzim, a-amino grubunu aspartattan a-ketoglutarata aktararak oksaloasetat ve glutamat elde eder.
L"alanin transaminaz yani GTP (Glutamat-Piruvat Transaminaz): enzim, a-amino grubunu "alanin'den" a-ketoglutarata aktararak piruvat ve glutamat elde eder.
Çeşitli transaminazlar, amino asitlerin amino grubunun bir alıcısı olarak α-ketogluratı kullanır ve onu glutamata dönüştürür; oluşan amino asitler ise keton cisimlerinin yolunda kullanılır.
Bu tür bir reaksiyon, aynı enerji içeriğine sahip bağları koparıp oluşturdukları için her iki yönde de olabilir.
Transaminazlar hem sitoplazmada hem de mitokondridedir (çoğunlukla sitoplazmada aktiftirler) ve izoelektrik noktalarında farklılık gösterirler.
Transaminazlar ayrıca amino asitleri dekarboksilatlayabilir.
Glutamat'ı tekrar α-ketoglutarat'a dönüştürmenin bir yolu olmalı: bu deaminasyonla yapılır.
Orası glutamat dehidrojenaz glutamatı α-ketoglutarat'a dönüştürebilen ve dolayısıyla glutamat formunda bulunan amino asitlerin amino gruplarını amonyağa dönüştürebilen bir enzimdir. Meydana gelen, ara α-amino glutarattan geçen bir redoks işlemidir: amonyak ve α-ketoglutarat serbest bırakılır ve dolaşıma geri döner.
Daha sonra amino asitlerin amino gruplarının atılması, transaminazlardan (substrata göre farklılık gösterir) ve amonyak oluşumunu belirleyen glutamat dehidrojenazdan geçer.
İki tip glutamat dehidrojenaz vardır: sitoplazmik ve mitokondriyal; aynı zamanda bu enzimin kosubstratı olan kofaktör NAD(P)+'dır: glutamat dehidrojenaz, indirgeme gücünün bir alıcısı olarak ya NAD+ ya da NADP+ kullanır. Sitoplazmik form, münhasıran olmamakla birlikte NADP+'yı tercih ederken, mitokondriyal form NAD+'yı tercih eder. Mitokondriyal form, amino gruplarının atılması amacına sahiptir: amonyak (mitokondride özel bir enzim için bir substrat olan) ve NADH (solunum zincirine gönderilen) oluşumuna yol açar. Sitoplazmik form ters yönde çalışır, yani (biyosentetik bir hedefe sahip olan) glutamat vermek için amonyak ve a-ketoglutarat kullanır: bu reaksiyon indirgeyici bir biyosentezdir ve kullanılan kofaktör NADPH'dir.
Glutamat dehidrogenaz, amonyak (idrar yoluyla) gibi amino asitlerin amino gruplarının atılması gerektiğinde veya enerji üretmek için amino asitlerin iskeletlerine ihtiyaç duyulduğunda çalışır: bu enzim bu nedenle negatif modülatörler olarak bir gösterge olan sistemlere sahip olacaktır. iyi enerji mevcudiyeti (ATP, GTP ve NAD (P) H) ve pozitif modülatörler olarak, enerji ihtiyacını gösteren sistemler (AMP, ADP, GDP, NAD (P) +, amino asitler ve tiroid hormonları).
Amino asitler (esas olarak lösin) glutamat dehidrojenazın pozitif modülatörleridir: eğer sitoplazmada amino asitler varsa, protein sentezi için kullanılabilirler veya biriktirilemeyecekleri için atılmaları gerekir (bu, amino asitlerin neden pozitif modülatörler olduğunu açıklar). ) .
Amonyak bertarafı: üre döngüsü
Balıklar amonyağı solungaçları yoluyla suya sokarak atarlar, kuşlar onu ürik aside (yoğuşma ürünü olan) dönüştürür ve dışkıyla ortadan kaldırır.İnsanlarda neler olduğunu görelim: glutamat dehidrojenazın glutamatı α-'ya dönüştürdüğünü söylemiştik. ketoglutarat ve amonyak ama bunun sadece karaciğerin mitokondrilerinde meydana geldiğini söylemedik.
Üre döngüsü boyunca amonyak bertarafının temel bir rolü mitokondriyal transaminazlar tarafından oynanır.

Bikarbonat iyonu (HCO3-) formundaki karbon dioksit, karbamik asit vermek üzere amonyak ile reaksiyona giren karboksi biyotin oluşturan biyotin kofaktörü tarafından aktive edilir; sonraki reaksiyon, karbamik asit oluşturan karbamil fosfat ve ADP üzerine bir fosfat aktarmak için ATP kullanır (ATP'nin ADP'ye dönüştürülmesi, karboksibiyotinin elde edilmesi için itici güçtür.) Bu faz tarafından katalize edilir. karbamil fosfat sentetaz ve mitokondride gerçekleşir. Karbamil fosfat ve ornitin, enzim için substratlardır. ornitin trans karbamilaz onları sitrüline dönüştüren; bu reaksiyon mitokondride (hepatositler) meydana gelir. Üretilen sitrülin mitokondriyi terk eder ve sitoplazmada "etkisi" altına girer.arginin süksinat sentetaz: sitrülinin karbonlu iskeleti ile bir aspartatınki arasında nükleofilik bir saldırı ve ardından suyun eliminasyonu yoluyla füzyon vardır. Arginin süksinat sentetaz enzimi bir ATP molekülü gerektirir, bu nedenle enerjik bir eşleşme vardır: ATP'nin AMP'ye hidrolizi ve pirofosfat (ikincisi daha sonra iki ortofosfat molekülüne dönüştürülür) substrattan bir su molekülünün atılmasıyla gerçekleşir. ve ortamın suyunun etkisiyle değil.
"Bir sonraki enzim"arginin süksinaz: bu enzim arginin süksinatı sitoplazma içinde arginin ve fumarata bölebilir.
Üre döngüsü enzim tarafından tamamlanır. arginaz: üre ve ornitin elde edilir; üre böbrekler (idrar) tarafından atılırken ornitin mitokondriye döner ve döngüyü sürdürür.
Üre döngüsü arginin tarafından dolaylı modülasyona tabidir: arginin birikimi üre döngüsünün hızlandırılması gerektiğini gösterir; arginin modülasyonu dolaylıdır çünkü arginin asetil glutamat sentetaz enzimini pozitif olarak modüle eder. İkincisi, bir glutamatın nitrojeni üzerinde bir asetil grubunu transfer edebilir: karbamil-fosfo sentetaz enziminin doğrudan bir modülatörü olan N-asetil glutamat oluşur.
Arginin, karbamil fosfat üretimi ornitinin atılması için yeterli değilse, üre döngüsünün bir metaboliti olarak birikir.
Üre sadece karaciğerde üretilir ancak ilk reaksiyonların gerçekleştiği başka yerler de vardır.
Beyin ve kaslar, amino gruplarını ortadan kaldırmak için özel stratejiler kullanır. Beyin, bir enzimin kullanıldığı çok verimli bir yöntem kullanır. glutamin sentetaz ve bir enzim glutamaz: birincisi nöronlarda bulunur, ikincisi ise karaciğerde bulunur. Bu mekanizma iki nedenden dolayı çok verimlidir:
Tek bir araçta iki amino grubu beyinden karaciğere taşınır;
Glutamin, glutamattan çok daha az toksiktir (glutamat ayrıca nöronal transfer gerçekleştirir ve fizyolojik konsantrasyonu aşmamalıdır).
Balıklarda da benzer bir mekanizma amino asitlerin amino grubunu solungaçlara getirir.
Amino grupları kastan (iskelet ve kalp), glukoz-alanin döngüsü yoluyla karaciğere ulaşır; ilgili enzim glutamin-piruvat transaminazdır: (glutamat formunda olan) amino gruplarının transpozisyonuna izin verir, piruvatı alanine ve aynı zamanda glutamatı kasta α-ketoglutarat'a dönüştürür ve karaciğerde ters süreç.
Farklı görevleri veya konumları olan transaminazların da yapısal farklılıkları vardır ve elektroforez ile belirlenebilir (farklı izoelektrik noktaları vardır).
Kandaki transaminazların varlığı, karaciğer veya kalp hasarının bir belirtisi olabilir (yani karaciğer veya kalp hücrelerinde doku hasarı); transaminazlar hem karaciğerde hem de kalpte çok yüksek konsantrasyonlardadır: elektroforez yoluyla hasarın karaciğerde mi yoksa kalp hücrelerinde mi meydana geldiğini belirlemek mümkündür.