LÜTFEN AKLINIZDA BULUNDURUN: TIBBİ ÜRÜN ARTIK İZİN VERİLMEMEKTEDİR
Vistide nedir?
Vistide, bir infüzyon çözeltisi içinde seyreltilecek bir konsantredir (damar içine damlama). Aktif bileşen cidofovir (75 mg/ml) içerir.
Vistide ne için kullanılır?
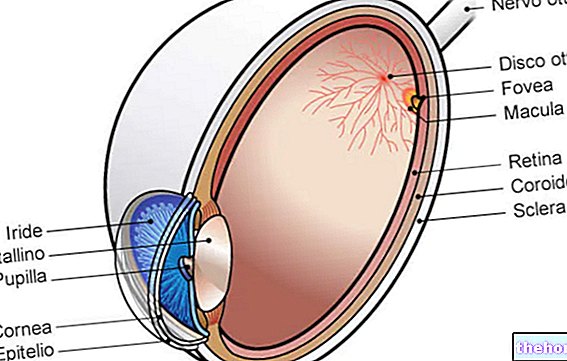
Vistide, retinanın (gözün en iç kısmını kaplayan ışığa duyarlı zar) viral bir enfeksiyonu olan sitomegalovirüs (CMV) retinitini tedavi etmek için kullanılır. Bu hastalık görme kaybına neden olabilir. Vistide, böbrek hastalığı olmayan edinilmiş immün yetmezlik sendromu (AIDS) olan hastalarda kullanılır ve yalnızca başka ilaçlarla tedavi mümkün olmadığında kullanılmalıdır.
İlaç sadece reçete ile alınabilir.
Vistide nasıl kullanılır?
Vistide tedavisi, insan immün yetmezlik virüsü (HIV) enfeksiyonunun yönetiminde deneyimli bir doktor tarafından reçete edilmelidir. İlaç böbrek hastalığı olan hastalara verilmemesi gerektiğinden, Vistide almadan önce hastanın böbrek fonksiyonu değerlendirilmelidir. "İndüksiyon" aşamasında, ilk iki hafta boyunca haftada bir "bir saatlik infüzyon" olarak vücut ağırlığının kilogramı başına 5 mg Vistide verilmelidir. Daha sonra, "bakım" aşamasında, uygulama iki haftada bir yapılmalıdır. Bu nedenle tedaviye, HIV enfeksiyonu olan hastaların yönetimine ilişkin yerel kılavuzlarda önerilen süre boyunca devam edilmelidir.
Böbrek hasarı riskini sınırlamak için, hastalar ayrıca başka bir ilaç, probenesid (infüzyondan üç saat önce 2 g, infüzyondan iki ve sekiz saat sonra 1 g) almalı ve bir saat önce bir litre salin infüzyonu verilmelidir. Vistide infüzyonu Probenesid böbreklerde cidofovir birikmesini önlemek için kullanılırken, salin dehidrasyonu önlemek için kullanılır.
Vistide nasıl çalışır?
Vistide'deki aktif madde, cidofovir, virüsün DNA yapmak için kullandığı CMV'nin "DNA polimerazı" adı verilen belirli bir enzimin aktivitesini bloke eden "nükleozid analogları" sınıfından bir antiviral ilaçtır. , enfeksiyonun yayılmasını yavaşlatan çoğalamaz.
Vistide nasıl çalışılmıştır?
CMV retiniti olan AIDS hastalarında Vistide'nin etkileri, bir tedavi çalışmasının ve bir idame çalışmasının konusu olmuştur. Daha önce CMV retiniti için herhangi bir ilaçla tedavi edilmemiş 48 hastada yürütülen tedavi çalışması, Vistide'in etkilerini tedavi uygulanmamasına karşı karşılaştırdı. Bakım çalışması, CMV retiniti için diğer ilaçlara (gansiklovir veya foskarnet) artık yanıt vermeyen veya bu ilaçları alamayan 100 hastada iki idame dozu (5 ve 3 mg/kg vücut ağırlığı) karşılaştırdı. Her iki çalışmada da etkililiğin ana ölçüsü, hastalığın kötüleşmeden önce ne kadar zaman geçtiğiydi.
Vistide'in çalışmalar sırasında ne gibi yararları oldu?
Tedavi çalışmasında, Vistide'in tedavi edilmeyen vakalara göre daha etkili olduğu gösterilmiştir. CMV retinitinde kötüleşme Vistide ile tedavi edilen hastalarda ortalama 120 gün sonra meydana gelirken, tedavi edilmeyen hastalarda 22 gün sonra kötüleşme meydana geldi. İdame çalışmasında 5 mg/kg dozu, 3 mg/kg dozundan (sırasıyla 115 ve 49 gün) daha etkili olmuştur.
Vistide ile ilişkili risk nedir?
Vistide ile ilişkili en yaygın yan etkiler (yani 10 hastada 1'den fazlasında görülen) nötropeni (düşük beyaz kan hücresi sayısı), baş ağrısı, bulantı, kusma, alopesi (saç dökülmesi), döküntü, proteinüridir (protein idrarı varlığı) , kanda artan kreatinin seviyeleri (kas metabolizmasının atık ürünü), asteni (zayıflık) ve ateş. Vistide ile bildirilen yan etkilerin tam listesi için paket broşürüne bakın.
Vistide, cidofovir veya diğer bileşenlerden herhangi birine karşı potansiyel olarak aşırı duyarlı (alerjik) hastalarda kullanılmamalıdır. Ayrıca böbrek hastalığı olan veya böbreklere zarar verebilecek diğer ilaçları alan hastalarda veya probenesid veya diğer kükürt içeren ilaçlarla tedavi edilemeyen hastalarda kullanılmamalıdır. Vistide doğrudan göze enjekte edilmemelidir.
Vistide neden onaylandı?
İnsan Ürünleri Tıbbi Ürünleri Komitesi (CHMP), AIDS'li ve böbrek hastalığı olmayan hastalarda CMV retiniti tedavisi için Vistide'in yararlarının risklerinden daha fazla olduğuna karar vermiş ve bu nedenle ona bir "pazarlama izni" verilmesini tavsiye etmiştir. Ziyaret edin.
Vistide hakkında daha fazla bilgi edinin
23 Nisan 1997'de Avrupa Komisyonu, Vistide için Avrupa Birliği genelinde geçerli olan bir "pazarlama izni" yayınladı.Bu yetki 23 Nisan 2002 ve 23 Nisan 2007'de yenilendi. Pazarlama "yetkisinin" sahibi Gilead Sciences International'dır.
Vistide's EPAR'ın tam sürümü için buraya tıklayın.
Bu özetin son güncellemesi: 01-2009.
Bu sayfada yayınlanan Vistide - cidofovir ile ilgili bilgiler güncelliğini yitirmiş veya eksik olabilir. Bu bilgilerin doğru kullanımı için Sorumluluk Reddi ve faydalı bilgiler sayfasına bakın.