Beromun nedir?
Beromun, infüzyon için bir çözelti hazırlamak için bir toz ve bir çözücüden oluşur. Etkin madde tasonermin içerir.
Beromun ne için kullanılır?
Beromun, uzuvların yumuşak doku sarkomu (bir tür kanser) olan hastalarda, melfalan (bir antikanser ilacı) ile kombinasyon halinde, "uzuvun bölgesel perfüzyonu" (ILP) adı verilen bir teknikle kullanılır: her iki ilaç da " uzuv, yerel kan dolaşımı ise vücudun geri kalanından izole tutulur. Bu teknik, bir tümörün kütlesini azaltmak için ameliyattan önce veya ameliyatın tek başına tümörü çıkarmak için yeterli olmadığı durumlarda ameliyatın yerine kullanılabilir.
İlaç sadece reçete ile alınabilir.
Beromun nasıl kullanılır?
Beromun ile tedavi sadece uzmanlaşmış merkezlerde, bu tip tümörün tedavisinde uzmanlaşmış cerrah grupları tarafından ve bölgesel uzuv perfüzyon tekniklerinde yapılmalıdır. Yoğun bakım üniteleri, radyoaktif izleyiciler kullanarak, ilacın vücudun geri kalanına kaybını sürekli olarak izleyecek donanıma sahip bu merkezlerde her zaman hazır bulundurulmalıdır.
Beromun'u uygulamadan önce uzvun izole edilmesi gerekir: hasta genel anestezi altındayken, kan akışını izole etmek ve ilacın dolaşım sistemine (genel) girmesini önlemek için etkilenen uzvun yukarısına sıkı bir dantel uygulanır. uzuvdaki kan dolaşımı daha sonra özel bir sıvının "perfüzyonu" ile değiştirilir ve uzuv 38 ° ila 39 ° arasında bir sıcaklığa ısıtılır.Daha sonra, bir kol için 3 mg'lık bir dozda perfüzyon çözeltisine Beromun enjekte edilir. ve 90 dakika boyunca bir bacak için 4 mg. Melphalan, sıcaklığın 39-40 ° C'ye yükseltilmesi gerektiğinde, yalnızca 30 dakikalık Beromun perfüzyonundan sonra, 60 dakika boyunca eşzamanlı olarak uygulanır. Malphalan dozu, kol veya bacağın boyutuna bağlıdır. perfüzyon (yani 90 dakika sonra), ilaçlar özel bir yıkama sıvısı yardımıyla uzuvdan çıkarılır.Mümkün olduğunda (genellikle birkaç hafta sonra), kalan tümör cerrahi olarak çıkarılmalıdır.
Beromun genellikle sadece bir kez kullanılır. Gerekirse, ilk tedaviden 6-8 hafta sonra ikinci bir perfüzyon yapılabilir. Ürünün bu yaş grubu için güvenliliği ve etkinliği hakkında bilgi bulunmadığından 18 yaş altı hastalarda kullanılması önerilmemektedir.
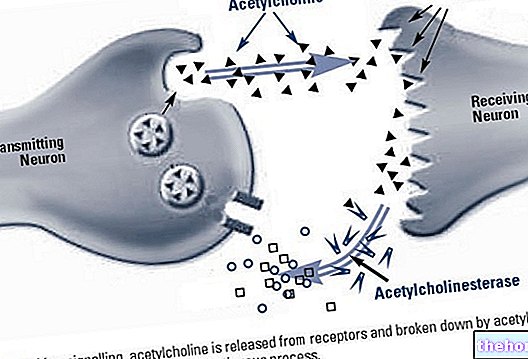
Beromun nasıl çalışır?
Beromun'daki aktif madde olan tasonermin, tümör nekroz faktörü alfa1a (TNFa) olarak adlandırılan insan proteininin bir kopyasıdır. TNFa'nın bazı kanser türlerine karşı kesin etki mekanizması tam olarak bilinmemekle birlikte, kanser hücrelerini doğrudan ortadan kaldırabildiğine ve tümör kütlesini besleyen kan damarlarını yok ettiğine ve bu şekilde sistemi uyararak tümörün gerileyeceğine inanılmaktadır. ve boyutu küçülür, özellikle ilaç diğer sitotoksik ilaçlarla (yani hücreleri yok edebilen) kombine edilirse ve sıcaklıkta bir artış indüklenirse.
Beromun'daki aktif madde olan tasonermin, 'rekombinant DNA teknolojisi' olarak bilinen bir yöntemle üretilir: TNFa üretmelerini sağlayan bir gen (DNA) almış bakteriler tarafından yapılır. Sentetik TNFa, doğal olarak üretilen protein gibi davranır.
Beromun nasıl incelendi?
Beromun, ilacı melfalan ile kombinasyon halinde verilen toplam 188 hastayı içeren dört ana çalışmada incelenmiştir. 62 hastaya ayrıca interferon gama (başka bir antikanser ilacı) verildi. Üç bağımsız uzman tarafından yapılan çalışmaların gözden geçirilmesi, bu deneklerin yalnızca 145'inin, önemli işlev kaybı (sakatlık) ile sonuçlanacak olan tümör amputasyonu veya cerrahi olarak çıkarılması için aday olduğunu buldu. Bu nedenle, etkililiğin ana ölçüsü, bu 145 hasta için tedavinin sonucunun, Beromun kullanılmamış olması durumunda beklenen sonuca kıyasla uzmanlar tarafından değerlendirilmesiydi.
Beromun'un çalışmalar sırasında ne gibi yararları oldu?
Bağımsız uzmanlar, Beromun ve melfalan ile tedavi edilen hastaların %62'sinin (145 hastanın 90'ı) beklenenden daha iyi bir sonuç elde ettiği konusunda hemfikirdi, çünkü önemli bir işlevselliğe neden olmadan tümörü çıkarmak veya tümörü çıkarmak için cerrahiye başvurmadan uzuv kurtarmak mümkündü. kayıp. Gama interferonla da tedavi edilen hasta sayısı, bu tedavinin terapötik sonucu daha da iyileştirip iyileştirmediğini belirlemek için yetersizdi.
Beromun ile ilişkili risk nedir?
Beromun ile tedavi edilen hastaların çoğunda, genellikle hafif veya orta derecede ateş görülür. Diğer çok yaygın yan etkiler (10 hastada 1'den fazlasında görülür) enfeksiyon, kardiyak aritmi (kalbin normal ritminde değişiklik), bulantı, kusma, karaciğer hasarı, yorgunluk, titreme, uzuvda ağrı, sinir hasarıdır. , cilt reaksiyonları, yarada ödem (şişme) ve enfeksiyon.Beromun'un bazı yan etkileri ciddidir ve tedavi sonrası yoğun bakım ünitesine sevk edilmesini gerektirebilir. Beromun ile bildirilen yan etkilerin tam listesi için paket broşürüne bakın.
Beromun, tasonermin veya diğer bileşenlerden herhangi birine aşırı duyarlı (alerjik) olabilecek kişilerde kullanılmamalıdır. Şiddetli kardiyovasküler hastalığı (kalbi ve kan damarlarını etkileyen), şiddetli akciğer hastalığı olan, yakın zamanda peptik ülser öyküsü olan veya aktif peptik ülseri olan, şiddetli asit formları (karın bölgesinde sıvı toplanması) olan hastalarda kullanılmamalıdır. kavite), kan bozuklukları, böbrek veya karaciğer hastalığı veya hiperkalsemi (kanda artan kalsiyum miktarı) veya hamile veya emziren kadınlarda. Ayrıca vazopressör ilaçlar (tansiyonu yükseltici özelliği olan ilaçlar), antikoagülan (kanın pıhtılaşmasını engelleyen ilaçlar) veya kalbe zarar verebilecek ilaçların kullanımı kontrendike olan hastalara da verilmemelidir. melfalan kullanımının kontrendike olduğu veya ILP'ye giremeyecek kişilerde kullanılabilir. Daha fazla ayrıntı için lütfen EPAR'da bulunan Ürün Özellikleri Özetine bakın.
Beromun neden onaylandı?
İnsan Kullanımına İlişkin Tıbbi Ürünler Komitesi (CHMP), uzuv amputasyonunu önlemek veya geciktirmek için tümörü çıkarmak için cerrahiye ek olarak veya ameliyat edilemeyen sarkomların varlığında palyatif tedavi olarak Beromun'un yararlarının risklerinden daha büyük olduğuna karar verdi. uzuvların orta derecede hipertermik lokorejyonel perfüzyonu (ILP) için melfalan ile kombinasyon halinde uygulanan uzuvların yumuşak dokuları Bu nedenle komite, ürün için bir pazarlama izni verilmesini tavsiye etti.
Beromun hakkında daha fazla bilgi
13 Nisan 1999'da Avrupa Komisyonu, Boehringer Ingelheim International GmbH'ye Beromun için Avrupa Birliği genelinde geçerli bir "Pazarlama İzni" verdi. "Pazarlama İzni" 13 Nisan 2004 ve 13 Nisan 2009'da yenilendi.
Beromun EPAR'ın tam sürümü için tıklayın quNS
Bu özetin son güncellemesi: 4-2009
Bu sayfada yayınlanan Beromun - tasonermina ile ilgili bilgiler güncelliğini yitirmiş veya eksik olabilir. Bu bilgilerin doğru kullanımı için Sorumluluk Reddi ve faydalı bilgiler sayfasına bakın.