Aktif maddeler: Sumatriptan (sumatriptan süksinat)
Imigran 10 mg ve 20 mg Burun Spreyi
Paketler için Imigran prospektüsleri mevcuttur:- IMIGRAN 6 mg / 0.5 ml Deri altı kullanım için enjeksiyonluk çözelti, IMIGRAN 50 mg Film kaplı tabletler, IMIGRAN 100 mg Film kaplı tabletler
- Imigran 25 mg Fitiller
- Imigran 10 mg ve 20 mg Burun Spreyi
Endikasyonları Imigran neden kullanılır? Bu ne için?
Her Imigran Burun Spreyi, triptanlar (5-HT1 reseptör agonistleri olarak da bilinir) adı verilen bir ilaç grubuna ait olan tek doz sumatriptan içerir.
Imigran Fitiller migren tedavisinde kullanılır.
Migren semptomlarına kafadaki kan damarlarının geçici olarak genişlemesi neden olabilir.Imigran Nazal Sprey'in bu kan damarlarının genişlemesini azalttığına inanılır.Bu, baş ağrılarını ve migren atağının mide bulantısı gibi diğer semptomlarını ortadan kaldırmaya yardımcı olur. kusma ve ışığa ve gürültüye duyarlılık.
Kontrendikasyonlar Imigran kullanılmamalıdır
IMIGRAN'ı aşağıdaki durumlarda KULLANMAYINIZ
- Sumatriptana veya bu ilacın içerdiği diğer maddelerden herhangi birine karşı alerjiniz varsa
- Arterlerin daralması (iskemik kalp hastalığı) veya göğüs ağrısı (anjina) gibi kalp problemleriniz varsa veya daha önce kalp krizi geçirdiyseniz.
- Bacaklarınızda yürürken kramp benzeri ağrılara neden olan kan dolaşımı sorunlarınız varsa (periferik damar hastalığı).
- Bir inme veya küçük bir inme geçirdiyseniz (geçici iskemik atak veya TIA olarak da adlandırılır).
- Yüksek tansiyonunuz varsa. Tansiyonunuz hafif yükselmişse ve tedavi ediliyorsa Imigran'ı kullanabilirsiniz.
- Şiddetli karaciğer hastalığınız varsa.
- Ergotamin içerenler dahil migren tedavisinde kullanılan diğer ilaçlar veya metisergit veya herhangi bir triptan / 5-HT1 reseptör agonisti (migren tedavisinde de kullanılan ilaçlar) gibi benzer ilaçlarla birlikte.
- MAOI (monoamin oksidaz inhibitörleri) adı verilen antidepresanlarla birlikte veya bu ilaçları son 2 hafta içinde kullandıysanız.
Bunlardan herhangi biri sizin için geçerliyse: ⇒ Doktorunuza söyleyiniz ve Imigran Burun Spreyi kullanmayınız.
Kullanım Önlemleri Imigran'ı almadan önce bilmeniz gerekenler
Imigran'ı kullanmadan önce doktorunuzla konuşun:
Herhangi bir ek risk faktörünüz varsa
- Çok sigara içiyorsanız veya nikotin yerine koyma tedavisi kullanıyorsanız ve özellikle
- 40 yaşını doldurmuş bir erkek ise,
- Menopozdaki bir kadınsanız.
Çok nadir durumlarda, bazı hastalarda daha önce kalp hastalığı belirtileri göstermemiş olsalar bile Imigran aldıktan sonra ciddi kalp rahatsızlıkları gelişmiştir. Yukarıdakilerden herhangi biri size atıfta bulunuyorsa, kalp hastalığı geliştirme riskiniz daha yüksek demektir - bu nedenle:
⇒ Imigran'ı reçete etmeden önce kalp fonksiyonunuzu kontrol edebilmesi için doktorunuza söyleyiniz.
Epilepsiniz varsa veya nöbet öykünüz varsa (uyuyorsa)
Veya nöbetleri daha olası hale getirebilecek başka koşullarınız varsa - örneğin, kafa travması veya alkolizm.
⇒ Doktorunuza söyleyin ki sizi daha dikkatli izlesin.
Böbrek veya karaciğer hastalığınız varsa
⇒ Doktorunuza söyleyin ki sizi daha dikkatli izlesin.
Sülfonamid adı verilen antibiyotiklere alerjiniz varsa
Bu durumda Imigran'a da alerjisi olabilir. Bir antibiyotiğe alerjiniz olduğunu biliyor ancak sülfonamid olup olmadığından emin değilseniz:
⇒ Imigran'ı kullanmadan önce doktorunuza veya eczacınıza söyleyiniz.
SSRI (Seçici Serotonin Geri Alım İnhibitörleri) veya SNRI (Serotonin ve Norepinefrin Geri Alım İnhibitörleri) adı verilen antidepresanlar alıyorsanız
⇒ Imigran'ı kullanmadan önce doktorunuza veya eczacınıza söyleyiniz. Ayrıca aşağıdaki Imigran'ı diğer ilaçlarla birlikte almak bölümüne bakınız.
Imigran'ı sık kullanıyorsanız.
Imigran'ı çok sık kullanmak baş ağrınızı daha da kötüleştirebilir.
⇒ Bu başınıza gelirse doktorunuza söyleyiniz. Doktorunuz Imigran kullanmayı bırakmanızı önerebilir.
Imigran'ı kullandıktan sonra göğüs ağrısı veya sıkışması hissederseniz
Bu etkiler yoğun olabilir ancak genellikle çabuk geçer. Çabuk geçmezlerse veya kötüleşirlerse:
⇒ Derhal tıbbi yardım alın. Bu broşürün bölümü, bu olası yan etkiler hakkında daha fazla bilgi sağlar.
Etkileşimler Hangi ilaçlar veya yiyecekler Imigran'ın etkisini değiştirebilir
Başka ilaçlar alıyorsanız, yakın zamanda aldıysanız veya alma ihtimaliniz varsa doktorunuza veya eczacınıza söyleyiniz. Bu, reçetesiz satın alınan herhangi bir bitkisel veya tıbbi ürünü içerir.
Bazı ilaçlar Imigran ile birlikte alınmamalıdır ve diğerleri Imigran ile birlikte alındığında yan etkilere neden olabilir. Aşağıdakileri alıyorsanız, bunu doktorunuzla konuşmalısınız:
- migren tedavisinde de kullanılan ergotamin veya metisergit gibi benzer ilaçlar (bkz. Imigran'ı bu ilaçlarla birlikte kullanmayınız. Imigran'ı kullanmadan en az 24 saat önce bu ilaçları almayı bırakın.Imigran'ı aldıktan sonra en az 6 saat boyunca ergotamin veya ergotamin benzeri bileşikler içeren ilaçlara devam etmeyin.
- Diğer triptanlar / 5-HT1 reseptör agonistleri (naratriptan, rizatriptan, zolmitriptan gibi) de migren tedavisinde kullanılır (bkz. bölüm 2 Imigran'ı kullanmayınız). Imigran'ı bu ilaçlarla birlikte kullanmayınız. Imigran'ı almadan en az 24 saat önce bu ilaçları almayı bırakın.Imigran'ı aldıktan sonra en az 24 saat boyunca başka bir triptan / 5-HT1 reseptör agonistini yeniden başlatmayın.
- Depresyon tedavisinde kullanılan SSRI'lar (Seçici Serotonin Geri Alım İnhibitörleri) veya SNRI'ler (Serotonin ve Noradrenalin Geri Alım İnhibitörleri). Imigran'ı bu ilaçlarla birlikte kullanmak serotonin sendromuna (ajitasyon, kafa karışıklığı, terleme, halüsinasyonlar, reflekslerde artış, kas spazmları, titreme, kalp hızında artış ve titremeleri içeren bir dizi semptom) neden olabilir.
- Depresyon tedavisinde kullanılan MAOI'ler (monoamin oksidaz inhibitörleri). Son 2 hafta içinde herhangi bir ilaç aldıysanız Imigran'ı kullanmayınız.
- Hypericum (Hypericum perforatum). Imigran alırken sarı kantaron içeren bitkisel ürünler kullanmak yan etkilerin görülme olasılığını artırabilir.
Uyarılar Şunları bilmek önemlidir:
- Hamileyseniz, hamile olabileceğinizi düşünüyorsanız veya bebek sahibi olmayı planlıyorsanız, bu ilacı almadan önce doktorunuza danışınız. Bugüne kadar doğum kusurları riskinde artış olduğuna dair herhangi bir kanıt olmamasına rağmen, Imigran'ın hamile kadınlarda güvenliğine ilişkin yalnızca sınırlı veri bulunmaktadır. Imigran'ı hamileyken alıp almayacağınıza doktorunuz sizinle birlikte karar verecektir.
- Imigran aldıktan sonra bebeğinizi en az 12 saat emzirmemelisiniz, bu süre içinde elde edilen anne sütü bebeğe verilmemeli ve atılmalıdır.
Araç ve makine kullanma
Hem migren semptomları hem de ilaç sizi uykulu yapabilir.Bunlardan muzdaripseniz araç veya makine kullanmamalısınız.
Doz, Yöntem ve Uygulama Süresi Imigran nasıl kullanılır: Pozoloji
Imigran'ı sadece migren atağı başladıktan sonra kullanın.
Saldırıyı önlemek için Imigran'ı kullanmayın.
Bu ilacı her zaman tam olarak doktorunuzun size söylediği şekilde kullanın. Şüpheniz varsa, doktorunuza veya eczacınıza danışmalısınız.
Bu broşürün sonunda, spreyi kullanma konusunda size adım adım rehberlik edecek talimatları bulacaksınız.
ne kadar kullanılır
18 ila 65 yaş arası yetişkinler
- 18 ila 65 yaş arası yetişkinler için olağan doz
bir burun deliğine bir sprey Imigran 20 mg spreydir.
Bununla birlikte, bazı insanlarda, bir burun deliğine Imigran 10 mg sprey sprey etkilidir.
Spreyi 24 saat içinde iki defadan fazla kullanmayın.
12 ila 17 yaş arasındaki ergenler
- 12 ila 17 yaş arası ergenler için olağan doz, bir burun deliğine 10 mg Imigran spreyidir.
12 yaşın altındaki çocuklar
- Imigran Burun Spreyi 12 yaşından küçük çocuklara önerilmemektedir.
Yaşlı (65 yaş üstü)
- Imigran Burun Spreyi 65 yaş üstü kişilere önerilmemektedir.
Imigran ne zaman kullanılır?
- Imigran'ı kullanmanın en iyi yolu, migren atağının başladığını hissettiğiniz anda kullanmaktır, ancak atak sırasında herhangi bir zamanda kullanılabilir.
Semptomlar tekrarlamaya başlarsa
- 2 saat sonra ikinci bir Imigran spreyi kullanabilirsiniz, ancak 24 saat içinde ikiden fazla sprey kullanmayın.
İlk spreyin etkisi yoksa
- Aynı saldırı için ikinci bir sprey veya başka bir Imigran preparatı kullanmayın.
Imigran sizi rahatlatmazsa:
- Tavsiye için doktorunuza veya eczacınıza danışınız.
Aşırı doz Çok fazla Imigran aldıysanız ne yapmalısınız?
Kullanmanız gerekenden daha fazla Imigran kullandıysanız
- 24 saat içinde iki puftan fazla Imigran Nazal Sprey kullanmayın.
Çok fazla Imigran alırsanız hasta hissedebilirsiniz. 24 saat içinde ikiden fazla sprey kullandıysanız: tavsiye için doktorunuza başvurun.
Bu ilacın kullanımıyla ilgili başka sorularınız varsa, doktorunuza veya eczacınıza sorunuz.
Yan Etkiler Imigran'ın yan etkileri nelerdir?
Tüm ilaçlar gibi, Imigran Fitilleri de yan etkilere neden olabilir, ancak bunları herkes almayabilir. Bazı semptomlar migrenin kendisinden kaynaklanabilir.
Erişkinlerde bildirilen yan etkiler ergenlerde de görülmüştür. Bu etkiler, çok nadir görülen kalp krizi raporlarını içerir.
Alerjik reaksiyonlar: hemen tıbbi yardım alın
Aşağıdaki yan etkiler meydana gelmiştir ancak bunların kesin sıklığı bilinmemektedir:
- Alerji belirtileri arasında deri döküntüsü, kurdeşen (kaşıntılı döküntü), hırıltılı solunum, göz kapaklarının, yüzün veya dudakların şişmesi ve hatta tamamen çökme bulunur.
Imigran kullandıktan hemen sonra bu belirtilerden herhangi biri ortaya çıkarsa:
⇒ Artık kullanmıyorsunuz. Derhal bir doktora başvurun.
Çok yaygın yan etkiler
(10 kişiden 1'inden fazlasını etkiler)
- Hoş olmayan tat.
Yaygın yan etkiler
(10 kişiden 1'ini etkiler)
- Göğüste, boğazda veya vücudun diğer bölümlerinde ağrı, ağırlık, basınç, sıkışma veya ağrı hissi veya uyuşma, karıncalanma ve sıcaklık veya soğukluk dahil anormal duyumlar. Bu etkiler yoğun olabilir ancak genellikle çabuk geçer.
Bu etkiler devam ederse veya kötüleşirse (özellikle göğüs ağrısı):
⇒ Acilen tıbbi yardım arıyorsunuz. Çok az sayıda insanda bu semptomlara kalp krizi neden olabilir.
Diğer yaygın yan etkiler şunlardır:
- Burun veya boğazda tahriş veya yanma hissi; burun kanaması
- Mide bulantısı veya kusma, ancak bu etkiler migrenin kendisinden kaynaklanabilir.
- Yorgunluk veya uyku hali.
- Baş dönmesi, halsizlik veya kızarma hissi.
- Kan basıncında geçici artış.
- Nefes darlığı.
- Kas ağrısı.
Çok seyrek yan etkiler
(10.000 kişiden 1'ini etkiler)
- Karaciğer fonksiyonundaki değişiklikler. Karaciğer fonksiyonunuzu kontrol etmek için bir kan testiniz varsa, lütfen doktorunuza veya hemşirenize MİGRAN kullandığınızı söyleyiniz.
Bazı hastalarda aşağıdaki yan etkiler görülebilir, ancak bunların ne sıklıkta ortaya çıktığı bilinmemektedir.
- Konvülsiyonlar / nöbetler, titreme, kas spazmları, boyun sertliği.
- Titreme, görme azalması, çift görme, görme kaybı ve hatta bazı durumlarda kalıcı kusurlar gibi görme bozuklukları (ancak bunlar migren atağının kendisinden kaynaklanabilir).
- Kalp sorunları, kalp atışları hızlanabilir, yavaşlayabilir veya ritmi değiştirebilir, göğüs ağrısı (anjina) veya kalp krizleri olabilir.
- Soluk veya mavi renkli cilt ve/veya soğuk veya strese tepki olarak parmaklarda, ayak parmaklarında, kulaklarda, burunda veya çenede ağrı (Raynaud fenomeni).
- Baygınlık hissi (tansiyon düşebilir).
- Midenin sol alt tarafında ağrı ve kanlı ishal (iskemik kolit).
- İshal
- Eklemlerde ağrı
- Kaygı hissi
- Asiri terleme
Yan etkilerin raporlanması
Bu kullanma talimatında listelenmeyen olası yan etkiler de dahil olmak üzere herhangi bir yan etki yaşarsanız, doktorunuza veya eczacınıza danışınız. Yan etkiler ayrıca https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse adresindeki ulusal raporlama sistemi aracılığıyla da doğrudan bildirilebilir.Yan etkileri bildirerek bu ilacın güvenliği hakkında daha fazla bilgi sağlamaya yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
Bu ilacı ışıktan korumak için kartonun içindeki kapalı blisterde saklayın.
30°C'nin üzerinde saklamayın ve dondurmayın.
Bu ilacı karton üzerinde belirtilen son kullanma tarihinden sonra kullanmayınız. Son kullanma tarihi, ayın son gününü ifade eder.
Herhangi bir ilacı atık su veya evsel atık yoluyla atmayın.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorun.Bu çevrenin korunmasına yardımcı olacaktır.
Imigran Burun Spreyi ne içerir?
Etkin madde sumatriptandır (10 mg veya 20 mg)
Diğer bileşenler monobazik potasyum fosfat, susuz disodyum fosfat, sülfürik asit, sodyum hidroksit ve arıtılmış sudur.
Imigran Burun Spreyi neye benziyor ve paketin içeriği
Bu ilaç, önceden dağıtılmış bir burun spreyi cihazı olarak sağlanır ve 0.1 ml sarı çözelti içinde sumatriptan içerir.
Imigran Burun Spreyi, blister ambalajlarda ayrı ayrı kapatılmış burun spreyleri içeren bir kutuda paketlenmiştir. 1, 2, 4, 6, 12 veya 18 adet önceden dağıtılmış burun spreyi cihazından oluşan paketler halinde mevcutturlar, ancak ülkenizde tüm paket boyutları pazarlanmayabilir. Her bir burun spreyi nefesi bir doz Imigran içerir.
Imigran Burun Spreyi kullanımında size adım adım rehberlik edecek talimatlar
Spreyi kullanmaya hazır olana kadar blisteri açmayın. Her sprey, temiz ve güvenli kalmasına yardımcı olmak için bir blisterde kapatılmıştır. Blister paketinden bir sprey taşırsanız veya blister açıkken, ihtiyacınız olduğunda sprey düzgün çalışmayabilir.
Her sprey sadece bir doz Imigran içerir.
Pistonu çok erken basmayın, aksi takdirde doz kaybolacaktır.
Imigran Burun Spreyi üç kısımdan oluşur:
emzik
Burun deliğine soktuğu kısımdır. Sprey üst kısımdaki çok küçük bir delikten çıkıyor.
sap
Spreyi kullanırken bu kısmı elinizde tutun.
mavi piston
Tüm dozu bir kerede burun deliğine iletmek için bastırın Piston sadece bir kez çalışır - memeyi burun deliğine sokana kadar pistonu itmeyin, aksi takdirde doz kaybolur.
burun spreyi nasıl kullanılır
1. Kullanmadan hemen önce burun spreyini blister ambalajından çıkarın.
2. Rahat bir pozisyon alın. Dilerseniz oturabilirsiniz.
3. Tıkanmış hissediyorsanız veya soğuk algınlığınız varsa burnunuzu üfleyin.
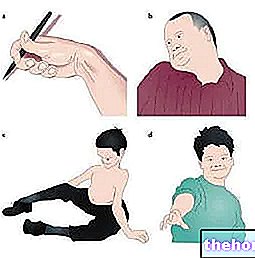
4. Burun spreyini parmaklarınız ve başparmağınızla şekil A'da gösterildiği gibi nazikçe tutun. Henüz mavi pistona basmayın.
5. Parmağınızla burnun bir tarafına sıkıca bastırarak bir burun deliğini kapatın. Hangi burun deliğinin kullanıldığı önemli değildir.
6. Nazal spreyin ucunu, yeterli olana kadar (yaklaşık 1 cm) diğer burun deliğine sokun (şekil B)
Ağzınızdan nazikçe nefes verin.
Resimde görüldüğü gibi başınızı dik tutun ve ağzınızı kapatın.
7. Burnunuzdan nazikçe nefes almaya başlayın
Ve nefes alırken:
Baş parmağınızla mavi pistona sıkıca bastırın
Piston biraz dirençli olabilir ve bir "klik" duyabilirsiniz. Pistona basarken nefes almaya devam edin (şekil C).
8. Spreyi burnunuzdan ve parmağınızı burnunuzun diğer tarafında çıkarın.
Başınızı yaklaşık 10-20 saniye dik tutun ve burnunuzdan nazikçe nefes alın ve ağzınızdan nefes verin. Bu, ilacın burunda kalmasına yardımcı olur. Spreyi kullandıktan sonra burun içinde nemli bir his ve hafif bir tat hissedebilirsiniz - bu normaldir ve kısa sürede geçer.
9. Burun spreyi artık boştur. Güvenli ve hijyenik bir şekilde imha edilmelidir.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
IMIGRAN NAZAL SPREY
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Imigran 10 mg Nazal Sprey: intranazal uygulama için birim doz sprey dispenseri. Dağıtıcı, 0.1 ml tamponlu sulu çözelti içinde 10 mg sumatriptan verir.
Imigran 20 mg Nazal Sprey: intranazal uygulama için birim doz sprey dispenseri. Dağıtıcı, 0.1 ml tamponlu sulu çözelti içinde 20 mg sumatriptan verir.
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakın.
03.0 FARMASÖTİK FORM
Burun spreyi, solüsyon.
Tek doz burun spreyi uygulaması için aplikatörlü cam şişelerde soluk sarı ila koyu sarı sıvı.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Imigran Nazal Sprey, auralı veya aurasız akut migren atağının tedavisinde endikedir.
04.2 Pozoloji ve uygulama yöntemi
Profilakside Imigran Nazal Sprey kullanılmamalıdır.
Imigran, akut migren atağının tedavisi için monoterapi olarak önerilir ve ergotamin veya ergotamin türevleri (metisergit dahil) ile birlikte uygulanmamalıdır (bkz. bölüm 4.3).
Migren atağının başlangıcından sonra mümkün olan en kısa sürede Imigran'ın alınması tavsiye edilir. İlaç, atak sırasında alındığında eşit derecede etkilidir.
Yetişkinler (18 yaş ve üstü)
Imigran Nazal Sprey'in optimal dozu, bir burun deliğine uygulanacak 20 mg'dır.Bununla birlikte, migren ataklarının değişkenliği ve sumatriptanın hem bireysel olarak hem de hastalar arasında emilimi nedeniyle bazı kişilerde 10 mg etkili olabilir.
Hasta Imigran'ın ilk dozuna yanıt vermiyorsa, aynı atak için ikinci bir doz alınmamalıdır. Bu durumlarda atak parasetamol, asetilsalisilik asit veya nonsteroid antiinflamatuar ilaçlar ile tedavi edilebilir.İmigran sonraki ataklar için kullanılabilir.
Hasta ilk doza yanıt verdiyse ancak semptomlar tekrarlıyorsa, iki doz arasında en az 2 saatlik bir aralık olması koşuluyla sonraki 24 saat içinde ikinci bir doz alınabilir.
24 saat içinde 2 inhalasyon 20 mg Imigran Nazal Sprey dozunu aşmayın.
Gençler (12-17 yaş)
Sumatriptanın adolesanlarda kullanımı, yerel kılavuzlar dikkate alınarak migren tedavisinde özel deneyime sahip bir uzman veya doktorun tavsiyesi üzerine olmalıdır.
Önerilen Imigran Nazal Sprey dozu bir burun deliğine uygulanmak üzere 10 mg'dır.
Hasta Imigran'ın ilk dozuna yanıt vermiyorsa, aynı atak için ikinci bir doz alınmamalıdır. Bu durumlarda atak parasetamol, asetilsalisilik asit veya nonsteroid antiinflamatuar ilaçlarla tedavi edilebilir.
Imigran sonraki saldırılar için kullanılabilir.
Hasta ilk doza yanıt verdiyse, ancak semptomlar tekrarlıyorsa, iki doz arasında en az 2 saatlik bir aralık olması koşuluyla sonraki 24 saat içinde ikinci bir doz alınabilir.
24 saat içinde 2 inhalasyon 10 mg Imigran Nazal Sprey dozunu aşmayın.
Çocuklar (12 yaş altı)
Güvenlilik ve etkililiğe ilişkin verilerin yetersiz olması nedeniyle 12 yaşın altındaki çocuklarda Imigran Nazal Sprey kullanılması önerilmez.
Yaşlı (65 yaş üstü)
65 yaş üstü hastalarda Imigran Nazal Sprey kullanımına ilişkin deneyim bulunmamaktadır.Yaşlı hastalarda farmakokinetiği yeterince çalışılmamıştır.Bu nedenle daha fazla veri elde edilene kadar sumatriptan kullanımı önerilmemektedir.
04.3 Kontrendikasyonlar
Sumatriptan veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
Sumatriptan, miyokard enfarktüsü geçirmiş veya iskemik kalp hastalığı, koroner vazospazmı (Prinzmetal's angina), periferik vasküler hastalığı veya iskemik kalp hastalığına ilişkin belirti veya semptomları olan hastalarda kullanılmamalıdır.
Sumatriptan, serebrovasküler olay (CVA) veya geçici iskemik atak (TIA) öyküsü olan hastalara verilmemelidir.
Şiddetli karaciğer yetmezliği olan hastalara sumatriptan verilmemelidir.
Sumatriptan kullanımı orta ve şiddetli hipertansiyonu olan hastalarda ve hafif kontrol edilemeyen hipertansiyonu olan hastalarda kontrendikedir.
Ergotamin veya ergotamin türevlerinin (metisergit dahil) veya herhangi bir triptan / 5-hidroksitriptamin1 (5-HT1) reseptör agonistinin birlikte uygulanması kontrendikedir (bkz. bölüm 4.5).
Monoamin oksidaz inhibitörlerinin (MAOI'ler) ve sumatriptanın birlikte uygulanması kontrendikedir.
Imigran, monoamin oksidaz inhibitörü tedavisinin kesilmesinden sonraki 2 hafta içinde kullanılmamalıdır.
04.4 Özel uyarılar ve uygun kullanım önlemleri
Imigran, ancak net bir migren teşhisi konulduktan sonra kullanılmalıdır.
Sumatriptan hemiplejik, baziler veya oftalmoplejik migren tedavisinde endike değildir.
Akut migren atağının tedavisine yönelik diğer tedavilerde olduğu gibi, diğer potansiyel olarak ciddi nörolojik durumları dışlamak için özen gösterilmelidir.
Migrenlilerin bazı serebrovasküler olaylar (örn. serebrovasküler kazalar, geçici iskemik ataklar) için artmış risk gösterebileceği akılda tutulmalıdır.
Sumatriptan uygulaması, yoğun olabilen ve boğazı etkileyen göğüs ağrısı ve sıkışma gibi geçici semptomlarla ilişkili olabilir (bkz. bölüm 4.8). Bu semptomların iskemik kalp hastalığının göstergesi olduğuna inanılıyorsa, daha fazla sumatriptan dozu verilmemeli ve uygun değerlendirme yapılmalıdır.
Sumatriptan, çok sigara içenler veya nikotin replasman tedavisi kullananlar da dahil olmak üzere kardiyak iskemi için risk faktörleri olan hastalara, önce kardiyovasküler değerlendirme yapılmadan uygulanmamalıdır (bkz. bölüm 4.3). Bu risk faktörlerinin mevcut olduğu menopoz sonrası kadınlara ve 40 yaş üstü erkeklere özel önem verilmelidir. Bununla birlikte, bu tür değerlendirmeler, kalp hastalığı olan her hastayı tanımlayamayabilir ve çok nadir durumlarda, altta yatan kardiyovasküler hastalığı olmayan hastalarda ve adolesanlarda ciddi kardiyak olaylar meydana gelmiştir (bkz. bölüm 4.8).
Sumatriptan, hafif kontrollü hipertansiyonu olan hastalarda dikkatli bir şekilde uygulanmalıdır, çünkü hastaların küçük bir kısmında kan basıncında ve periferik vasküler dirençte geçici artışlar gözlenmiştir (bkz. bölüm 4.3).
Selektif bir serotonin geri alım inhibitörü (SSRI) ve sumatriptan kullanımını takiben serotonin sendromu (mental durumda değişiklik, otonomik instabilite ve nöromüsküler anormallikler dahil) olan hastalara ilişkin ender pazarlama sonrası raporlar olmuştur. triptanlar ve serotonin norepinefrin geri alım inhibitörleri (SNRI'ler).
Sumatriptanın bir SSRI / SNRI ile eşzamanlı tedavisi klinik olarak gerekliyse, hastanın uygun şekilde gözlemlenmesi önerilir (bkz. bölüm 4.5).
Sumatriptan, karaciğer veya böbrek yetmezliği gibi, ilacın emilimini, metabolizmasını ve atılımını önemli ölçüde değiştirebilecek durumları olan hastalara dikkatle uygulanmalıdır.
Sumatriptan ile ilişkili nöbetler bildirildiğinden, epilepsisi ve/veya nöbet öyküsü veya nöbet eşik düzeyini düşüren diğer risk faktörleri olan hastalarda sumatriptan dikkatli kullanılmalıdır (bkz. bölüm 4.8).
Sülfonamidlere karşı aşırı duyarlılığı olduğu bilinen hastalar, sumatriptan uygulamasını takiben alerjik reaksiyon yaşayabilir. Reaksiyonlar kutanöz aşırı duyarlılıktan anafilaksiye kadar değişebilir.
Çapraz reaktivite kanıtı sınırlıdır, ancak kullanmadan önce dikkatli olunmalıdır.
Bu hastalarda sumatriptan
İstenmeyen etkiler, triptanlar ve sarı kantaron içeren bitkisel preparatların birlikte kullanımı sırasında daha yaygın olarak ortaya çıkabilir (hipericum perforatum).
Baş ağrısı için herhangi bir tür ağrı kesicinin uzun süreli kullanımı durumu daha da kötüleştirebilir.Bu meydana gelirse veya şüpheleniliyorsa, tıbbi yardım aranmalı ve tedavi kesilmelidir. baş ağrısı ilaçlarının düzenli kullanımına rağmen (veya bu nedenle).
Önerilen Imigran dozları aşılmamalıdır.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Propranolol, flunarizin, pizotifen veya alkol ile etkileşime dair kanıt yoktur.
Ergotamin içeren müstahzarlar veya diğer triptanlar / 5-HT1 reseptör agonistleri ile etkileşimlere ilişkin veriler sınırlıdır. Koroner vazospazm riskinde artışa ilişkin teorik bir olasılık vardır ve eşzamanlı uygulama kontrendikedir (bkz. bölüm 4.3).
Sumatriptan ile ergotamin veya diğer triptanlar / 5-HT1 reseptör agonistleri içeren preparatların kullanımı arasında geçmesi gereken süre bilinmemektedir.Bu, kullanılan ürünlerin dozlarına ve türlerine de bağlıdır.Etkiler aditif olabilir.Evet.tavsiye edilir. sumatriptan uygulamadan önce ergotamin preparatları veya diğer triptan / 5-HT1 reseptör agonistlerini aldıktan sonra en az 24 saat beklemek. Tersine, sumatriptan kullandıktan sonra ergotamin içeren ürünleri almadan önce 6 saat ve başka bir triptan / 5-HT1 reseptör agonisti almadan önce en az 24 saat beklemek gerekir.
Sumatriptan ve MAOI'ler arasında etkileşimler meydana gelebilir ve birlikte uygulama kontrendikedir (bkz. bölüm 4.3).
Bir SSRI ve sumatriptan kullanımını takiben serotonin sendromlu (mental durumda değişiklik, otonomik instabilite ve nöromüsküler anormallikleri içeren) hastalarda nadiren pazarlama sonrası raporlar olmuştur. bölüm 4.4).
04.6 Hamilelik ve emzirme
Gebelik
1000'den fazla kadında gebeliğin ilk trimesterinde sumatriptanın kullanımına ilişkin pazarlama sonrası veriler vardır.Bu veriler kesin sonuçlara varmak için yeterli bilgi içermese de, konjenital defekt riskinde bir artış göstermediler. sumatriptanın ikinci ve üçüncü trimesterlerde kullanımı sınırlıdır.
Deneysel hayvan çalışmalarının değerlendirilmesi, perinatal veya postnatal gelişim üzerinde doğrudan teratojenik etkiler veya zararlı etkiler göstermez. Ancak tavşanlarda embriyo-fetal canlılığı değiştirebilir (bkz. bölüm 5.3). Sumatriptan uygulaması, ancak anne için beklenen yararlar, fetüs için olası herhangi bir riskten ağır basıyorsa düşünülmelidir.
Besleme zamanı
Subkutan uygulamayı takiben sumatriptanın insan sütüne geçtiği gösterilmiştir. Bebeklerin ilaca maruz kalması, tedaviyi takip eden 12 saat boyunca emzirmeden kaçınılarak en aza indirilebilir ve bu süre zarfında üretilen anne sütü miktarı ortadan kaldırılmalıdır.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
Araç veya makine kullanma yeteneği üzerindeki etkilerle ilgili herhangi bir çalışma yapılmamıştır. Migren veya sumatriptan ile tedavisi uyuşukluğa neden olabilir.Bu, araç veya makine kullanma yeteneğini etkileyebilir.
04.8 İstenmeyen etkiler
İstenmeyen etkiler aşağıda sistem organ sınıfına ve sıklığa göre bölünmüş olarak listelenmiştir. Sıklıklar şu şekilde tanımlanmıştır: çok yaygın (≥1/10), yaygın (≥1/100,
Erişkinlerde bildirilen yan etkiler ergenlerde de görülmüştür. Bunlara çok seyrek olarak koroner arter vazospazmı ve miyokard enfarktüsü raporları dahildir (bkz. bölüm 4.4).
Bağışıklık sistemi bozuklukları
Bilinmiyor: kutanöz aşırı duyarlılıktan (kurdeşen gibi) anafilaksiye kadar değişen aşırı duyarlılık reaksiyonları.
Sinir sistemi bozuklukları
Çok yaygın: tat alma bozukluğu / hoş olmayan tat.
Yaygın: Baş dönmesi, uyuşukluk, parestezi ve hipoestezi dahil duyusal rahatsızlıklar.
Bilinmiyor: Nöbetler, ancak bu vakalardan bazıları, nöbet öyküsü olan veya nöbetlere yatkınlık yaratan eşlik eden durumlar olan hastalarda meydana gelmiştir. Bu tür predispozan faktörlerin belirgin olmadığı hasta raporları da vardır. Titreme, distoni, nistagmus, skotom.
Göz bozuklukları
Bilinmiyor: Görmede titreme, çift görme, görme bozukluğu. Kalıcı kusurlar da dahil olmak üzere görme kaybı. Bununla birlikte, migren atakları sırasında göz bozuklukları ortaya çıkabilir.
Kardiyak patolojiler
Bilinmiyor: bradikardi, taşikardi, çarpıntı, kardiyak aritmiler, geçici iskemik tip EKG değişiklikleri, koroner vazospazm, anjina, miyokard enfarktüsü (bkz. bölüm 4.3 ve 4.4).
Vasküler patolojiler
Yaygın: Uygulamadan hemen sonra oluşan kan basıncında geçici artış. Kırmızılık.
Bilinmiyor: Hipotansiyon, Raynaud fenomeni.
Solunum, göğüs ve mediastinal bozukluklar
Yaygın: Sumatriptan burun spreyi uygulamasını takiben burun veya boğazda veya burun kanamasında hafif ve geçici tahriş veya yanma hissi bildirilmiştir. nefes darlığı.
Gastrointestinal bozukluklar
Yaygın: Bazı hastalarda bulantı ve kusma meydana gelmiştir, ancak bunun sumatriptanla mı yoksa önceden var olan koşullarla mı ilgili olduğu belirsizdir.
Bilinmiyor: iskemik kolit
Bilinmiyor: ishal
Kas-iskelet ve bağ dokusu bozuklukları
Yaygın: ağırlık hissi (genellikle geçicidir, yoğun olabilir ve göğüs ve boğaz dahil vücudun herhangi bir bölümünü etkileyebilir). miyalji.
Bilinmiyor: boyun sertliği
Bilinmiyor: artralji
Genel bozukluklar ve uygulama yeri koşulları
Yaygın: Ağrı, sıcaklık veya soğukluk hissi, basınç veya sıkışma (bu semptomlar genellikle geçicidir ve yoğun olabilir ve göğüs ve boğaz dahil vücudun herhangi bir bölümünü etkileyebilir); halsizlik, bitkinlik hissi (her iki semptom da çoğunlukla geçicidir ve hafif ila orta şiddettedir).
tanı testleri
Çok seyrek: Karaciğer fonksiyon testlerinde ara sıra hafif değişiklikler gözlenmiştir.
Psikolojik bozukluklar
Bilinmiyor: Anksiyete.
Deri ve deri altı doku bozuklukları
Bilinmiyor: hiperhidroz
04.9 Doz aşımı
Nazal olarak 40 mg'a kadar ve subkutan olarak 16 mg'dan yüksek ve oral olarak 400 mg'a kadar tekli sumatriptan dozları, yukarıda belirtilenler dışında yan etkilerle ilişkilendirilmemiştir.
Klinik deney gönüllüleri, 4 gün boyunca günde üç kez nazal 20 mg sumatriptan aldı ve hiçbir önemli yan etki olmadı.
Doz aşımı durumunda hasta en az 10 saat izlenmeli ve gerekirse uygun destekleyici bakım başlatılmalıdır Hemodiyaliz veya periton diyalizinin plazma sumatripta konsantrasyonları üzerindeki etkileri bilinmemektedir.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: Seçici 5-HT1 reseptör agonistleri, ATC kodu: N02CC01.
Sumatriptan, diğer 5-HT reseptör alt tipleri (5-HT2 - 5-HT7) üzerinde hiçbir etkisi olmayan seçici bir vasküler 5-hidroksitriptamin-1- (5-HT1d) reseptör agonistidir. Vasküler 5-HT1d reseptörü esas olarak kraniyal damarlarda tanımlanmıştır ve vazokonstriksiyon aracısıdır. Hayvanlarda sumatriptan, meninksler gibi ekstra ve intrakraniyal dokuları sulayan karotis dolaşımını seçici olarak zorlayarak etki eder.İnsanlarda migrenin patogenetik mekanizmasının temelinde bu damarlarda genişleme ve/veya ödem oluşmasının yattığına inanılmaktadır. Ayrıca, hayvan çalışmalarından elde edilen deneysel kanıtlar, sumatriptanın trigeminal sinir aktivitesini inhibe ettiğini göstermektedir. Hem kranyal vazokonstriksiyon hem de trigeminal sinir aktivitesinin inhibisyonu, insanlarda sumatriptanın anti-migren etkisine katkıda bulunabilir.
Klinik yanıt, 20 mg dozun intranazal uygulamasından 15 dakika sonra başlar.
Imigran Burun Spreyi, uygulama yolu sayesinde özellikle atak sırasında bulantı ve kusma şikayeti olan hastaların tedavisi için uygundur.
Tedavi etkisi ergenlerde yetişkinlere göre daha azdır.
05.2 Farmakokinetik özellikler
Sumatriptan, intranazal uygulamadan sonra hızla emilir ve maksimum plazma konsantrasyonlarına ulaşmak için medyan süre yetişkinlerde 1.5 saat (aralık: 0.25-3) ve yetişkinlerde 2 saattir (aralık: 0.5-3). 20 mg'lık bir dozdan sonra ortalama maksimum konsantrasyon 13 ng / ml'dir. Subkutan uygulamaya göre ortalama intranazal biyoyararlanım, kısmen presistemik metabolizma nedeniyle yaklaşık %16'dır.
Karaciğer yetmezliği olan hastalarda, Boşluk oral uygulamayı takiben pre-sistemik azalır ve plazma sumatriptanın seviyelerinde artışa neden olur. Benzer bir artış, intranazal uygulamadan sonra beklenir.
Plazma protein bağlanması düşüktür (%14-21), ortalama dağılım hacmi 170 litredir. Eliminasyon yarı ömrü yaklaşık 2 saattir. Boşluk toplam plazma yaklaşık 1160 mL/dk'dır ve ortalama Boşluk böbrek plazması yaklaşık 260 ml / dak.
Adolesan deneklerde (12-17 yaş) yapılan bir farmakokinetik çalışma, 20 mg'lık bir dozun intranazal uygulamasını takiben, ortalama maksimum plazma konsantrasyonlarının 13.9 ng/ml olduğunu ve ortalama eliminasyon yarı ömrünün yaklaşık 2 saat olduğunu göstermiştir. Boşluk adolesan popülasyonunda vücut kütlesi arttıkça dağılım hacmi de artar, bu da daha düşük vücut ağırlıklı ergenlerde daha yüksek maruziyete neden olur.
Orası Boşluk renal olmayan toplamın yaklaşık %80'idir Sumatriptan esas olarak monoamin oksidaz A'nın aracılık ettiği oksidatif metabolizma ile elimine edilir. serbest asit ve glukuronid formu 5-HT1 veya 5-HT2 aktivitesi bilinmiyor Tanımlanmış minör metabolitler yok.
Sumatriptanın intranazal uygulamayı takiben farmakokinetik profilinin migren ataklarından önemli ölçüde etkilendiği gösterilmemiştir.
Yaşlılardaki kinetik, genç ve yaşlı gönüllüler arasında olası kinetik farklılıkları belirlemek için yeterince çalışılmamıştır.
05.3 Klinik öncesi güvenlik verileri
Sumatriptan burun spreyi formülasyonunun lokal ve oküler tahriş potansiyelini araştırmak için yürütülen klinik öncesi çalışmalarda, sprey tavşanların gözlerine doğrudan uygulandığında laboratuvar hayvanlarında hiçbir burun tahrişi veya göz tahrişi gözlemlenmemiştir.
Akut ve kronik toksisiteye ilişkin deneysel çalışmalar, insanlarda kullanılan terapötik doz aralığında hiçbir toksik etki kanıtı göstermemiştir. Bir sıçan doğurganlık çalışmasında, maksimum insan maruziyetini yeterince aşan maruziyet seviyelerinde tohumlama başarısında bir azalma gözlemlenmiştir. Tavşanlarda belirgin teratojenik kusurlar olmaksızın embriyoletalite gözlenmiştir.
provalarda laboratuvar ortamında ve hayvan çalışmalarında, sumatriptan genotoksik ve kanserojen aktiviteden yoksundur.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
monobazik potasyum fosfat
Susuz dibazik sodyum fosfat
Sülfürik asit
Sodyum hidroksit
Arıtılmış su.
06.2 Uyumsuzluk
İlgili değil.
06.3 Geçerlilik süresi
3 yıl
06.4 Depolama için özel önlemler
30°C'nin üzerinde saklamayın. Dondurmayın.
Imigran Burun Spreyi, ışıktan korumak için kapalı blisterde, tercihen karton kutuda saklanmalıdır.
06.5 İç ambalajın yapısı ve paketin içeriği
Kap, bir tip I Ph.Eur cam şişe içerir. kauçuk tıpa ve aplikatör ile.
Imigran 10 mg Nazal Sprey: 0.1 ml solüsyon içeren birim doz sprey dispenseri.
1, 2, 4, 6, 12 veya 18 sprey paketi.
Imigran 20 mg Nazal Sprey: 0.1 ml solüsyon içeren birim doz sprey dispenseri.
1, 2, 4, 6, 12 veya 18 sprey paketi.
Tüm paket boyutları pazarlanmayabilir.
06.6 Kullanım ve kullanım talimatları
Özel talimat yok.
07.0 PAZARLAMA YETKİ SAHİBİ
GlaxoSmithKline S.p.A. - Via A. Fleming, 2 - Verona
08.0 PAZARLAMA YETKİ NUMARASI
10 mg A.I.C.'lik 2 tek doz sprey: 027975123 / M
20 mg A.I.C.'lik 2 tek doz sprey: 027975135 / M
6 20 mg tek doz sprey A.I.C.: 027975147 / M
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
18 Şubat 1997 / Mart 2006
10.0 METİN REVİZYON TARİHİ
10 Mayıs 2013



















-cos-cause-e-disturbi-associati.jpg)