Aktif maddeler: Fluoksetin
AZUR 20 mg sert kapsüller Fluoksetin
Azur neden kullanılır? Bu ne için?
FARMAKOTERAPÖTİK KATEGORİ
Antidepresanlar. Seçici serotonin geri alım inhibitörleri.
TEDAVİ ENDİKASYONLARI
AZUR, depresyon, obsesif kompulsif bozukluk ve bulimia nervoza tedavisinde endikedir.
Kontrendikasyonlar Azur ne zaman kullanılmamalıdır?
Nadir durumlarda, özellikle fluoksetin diğer serotonerjik ilaçlarla (diğerlerinin yanı sıra L-triptofan) ve/veya nöroleptiklerle birlikte uygulandığında, fluoksetin tedavisiyle ilişkili olarak bir serotonin sendromu veya nöroleptik malign sendrom benzeri olayların gelişimi bildirilmiştir. Bu sendromlar hasta için potansiyel olarak yaşamı tehdit eden durumlara yol açabileceğinden, bu tür olaylar meydana gelirse (hipertermi, rijidite, miyoklonus, otonom sinir sistemi dengesizliği ve hayati belirtilerde olası hızlı dalgalanmalar gibi semptom grupları ile karakterize edilir, konfüzyon, sinirlilik ve deliryum ve komaya varan aşırı ajitasyon) fluoksetin tedavisi kesilmeli ve semptomatik destekleyici tedavi başlatılmalıdır.
Kullanım Önlemleri Azur'u almadan önce bilmeniz gerekenler
18 yaşın altındaki çocuklar ve ergenler tarafından kullanım için
Antidepresanlarla tedavi edilen çocuk ve ergenlerde yapılan klinik çalışmalarda, intiharla ilgili davranışlar (intihar girişimi ve intihar düşünceleri) ve düşmanca tutum (özellikle saldırgan, muhalif ve öfkeli davranışlar), plasebo ile tedavi edilenlere göre daha sık gözlenmiştir. Azur, 8 ila 18 yaş arası çocuklarda ve ergenlerde yalnızca orta ila şiddetli majör depresif atakların tedavisinde kullanım içindir ve diğer endikasyonlarda kullanılmamalıdır. Tıbbi ihtiyaca göre tedavi kararı verilirse, hasta intihar semptomlarının ortaya çıkması açısından dikkatle izlenmelidir. Ayrıca, büyüme, cinsel olgunlaşma ve bilişsel, duygusal ve davranışsal gelişim üzerindeki etkiler de dahil olmak üzere güvenlik üzerindeki uzun vadeli etkilere ilişkin çocuklarda ve ergenlerde yalnızca sınırlı veriler mevcuttur.
19 haftalık bir klinik çalışmada, fluoksetin ile tedavi edilen çocuk ve adolesanlarda boy ve kilo artışında azalma gözlenmiştir (bkz. bölüm İstenmeyen etkiler). yetişkin". Ergenlikte gecikme olasılığı göz ardı edilemez (bkz. İstenmeyen etkiler). Bu nedenle fluoksetin tedavisi sırasında ve sonrasında pubertal büyüme ve gelişme (boy, kilo ve TANNER evrelemesi) izlenmelidir. Her ikisi de yavaşlarsa, bir pediatrik değerlendirme istenmelidir.
Pediyatrik klinik çalışmalarda, mani ve hipomani sıklıkla rapor edilmiştir (bkz. İstenmeyen etkiler). Bu nedenle mani/hipomani başlangıcı için düzenli izleme önerilir. Manik faza giren herhangi bir hastada fluoksetin kesilmelidir.
Doktorun çocuk veya genç ve/veya ebeveynleri ile tedavinin risklerini ve yararlarını dikkatlice tartışması önemlidir.
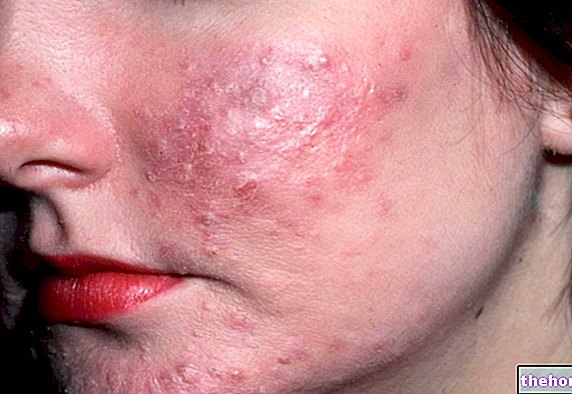
Döküntü ve alerjik reaksiyonlar: Döküntü, anafilaktoid olaylar ve bazen ciddi (cilt, böbrek, karaciğer veya akciğeri içeren) ilerleyici sistemik olaylar bildirilmiştir. Farklı bir etiyolojisi tanımlanamayan deri döküntüsü veya diğer alerjik fenomenlerin ortaya çıkması üzerine fluoksetin uygulaması kesilmelidir.
Önlemler
Nöbetler: Nöbetler, antidepresan ilaçlarla potansiyel bir risk oluşturur. Bu nedenle, diğer antidepresanlarda olduğu gibi, fluoksetin nöbet öyküsü olan hastalara dikkatle uygulanmalıdır. Nöbet gelişen veya nöbet sıklığında artış görülen herhangi bir hastada tedavi kesilmelidir. Stabil olmayan nöbet bozuklukları / epilepsisi olan hastalarda fluoksetin uygulamasından kaçınılmalı ve kontrollü epilepsisi olan hastalar dikkatle izlenmelidir.
Mani: Mani/hipomani öyküsü olan hastalarda antidepresanlar dikkatli kullanılmalıdır. Tüm antidepresan ilaçlar gibi, manik faza giren herhangi bir hastada fluoksetin kesilmelidir.
Karaciğer / Böbrek Fonksiyonu: Fluoksetin, karaciğer tarafından büyük ölçüde metabolize edilir ve böbrekler tarafından elimine edilir. Önemli karaciğer fonksiyon bozukluğu olan hastalarda günde 20 mg'lık daha düşük bir doz önerilir, örn. alternatif bir gün dozu. 2 ay boyunca günde 20 mg fluoksetin uygulandığında, diyaliz gerektiren şiddetli böbrek yetmezliği (GFR <10 mL/dk) olan hastalar, normal böbrek fonksiyonu olan kontrollere kıyasla fluoksetin veya norfluoksetinin plazma seviyelerinde hiçbir fark göstermedi.
Kardiyak Hastalık: Çift kör klinik çalışmalarda fluoksetin alan 312 hastada EKG'de kardiyak arreste yol açan iletim değişikliklerinin hiçbiri gözlenmemiştir.Ancak, akut kalp hastalığında klinik deneyim sınırlıdır, bu nedenle dikkatli olunması önerilir.
Kilo kaybı: Fluoksetin alan hastalarda kilo kaybı olabilir, ancak bu genellikle başlangıç vücut ağırlığı ile orantılıdır.
Diyabet: Diyabetik hastalarda SSRI tedavisi glisemik kontrolü değiştirebilir. Fluoksetin tedavisi sırasında hipoglisemi meydana gelirken, ilacın kesilmesinden sonra hiperglisemi gelişti. İnsülin ve/veya oral hipoglisemik ajanın doz ayarlaması gerekebilir.
İntihar / intihar düşünceleri veya klinik kötüleşme: Depresyon, intihar düşünceleri, kendine zarar verme ve intihar (intiharla ilgili olaylar) riskinde artış ile ilişkilidir. Bu risk, hastalıkta belirgin bir remisyon gerçekleşene kadar devam eder. Tedavinin ilk veya sonraki haftalarında düzelme olmayabileceğinden, hastalar iyileşme gerçekleşene kadar yakından izlenmelidir. İyileşme sürecinin erken dönemlerinde intihar riskinin artabileceği genel klinik deneyimdir.
Azur'un reçete edildiği diğer psikiyatrik durumlar da intiharla ilgili olayların riskinin artmasıyla ilişkilendirilebilir. Ayrıca, bu durumlar majör depresif bozuklukla birlikte olabilir. Bu nedenle, majör depresif bozukluğu olan hastaları tedavi ederken gözlemlenen önlemlerin aynıları, diğer psikiyatrik bozuklukları olan hastaları tedavi ederken de uygulanmalıdır.
İntiharla ilgili olay öyküsü olan hastalar arasında, tedaviye başlamadan önce önemli derecede intihar düşüncesi olanlar, artan intihar düşüncesi ve intihar girişimi riskine sahiptir ve tedavi sırasında yakından izlenmelidir. Psikiyatrik bozuklukların tedavisinde plaseboya kıyasla antidepresan ilaçlarla yürütülen çalışmalar, plaseboya kıyasla antidepresanlarla tedavi edilen 25 yaşın altındaki hastalarda intihar davranışı riskinde artış göstermiştir.
Hastaların ve özellikle yüksek risk altındakilerin yakın gözetimi, özellikle tedavinin ilk aşamalarında ve doz değişikliklerinden sonra ilaç tedavisine eşlik etmelidir. Hastalar (veya bakıcıları), bu semptomlar ortaya çıkarsa, klinik tablodaki herhangi bir kötüleşmeyi, intihar davranışı veya düşüncelerinin başlangıcını veya davranışta olağandışı değişiklikleri izlemeleri ve tedavi eden doktora derhal bildirmeleri gerektiği konusunda bilgilendirilmelidir.
Akatizi / psikomotor huzursuzluk: Fluoksetin kullanımı, "sübjektif olarak hoş olmayan veya rahatsız edici bir huzursuzluk ve genellikle oturma veya hareketsiz duramama ile birlikte hareket etme ihtiyacı" ile karakterize edilen akatizi gelişimi ile ilişkilendirilmiştir. Bu, daha olasıdır. tedavinin ilk birkaç haftasında ortaya çıkar.Bu semptomların görüldüğü hastalarda dozun arttırılması zararlı olabilir.
SSRI tedavisinin kesilmesiyle gözlenen kesilme semptomları: Tedavi durdurulduğunda, özellikle de tedavinin aniden kesilmesi durumunda, kesilme semptomları yaygındır ("İstenmeyen etkiler" bölümüne bakınız). Klinik çalışmalarda, hem fluoksetin hem de plasebo gruplarındaki hastaların yaklaşık %60'ında tedavinin aniden kesilmesiyle gözlenen advers olaylar meydana gelmiştir.Bu advers olayların fluoksetin grubunda %17'si ve fluoksetin grubunda %12'si plasebo ile şiddetli olmuştur. doğada.
Yoksunluk semptomları riski, tedavinin süresi ve dozu ve doz azaltma oranı dahil olmak üzere çeşitli faktörlere bağlı olabilir. En sık bildirilen reaksiyonlar baş dönmesi, duyu bozuklukları (parestezi dahil), uyku bozuklukları (uykusuzluk ve yoğun rüyalar dahil), asteni, ajitasyon veya anksiyete, bulantı ve/veya kusma, titreme ve baş ağrısıdır. Genellikle bu semptomlar hafif ila orta şiddettedir, ancak bazı hastalarda şiddetli olabilir. Bu semptomlar genellikle tedavinin kesilmesinden sonraki ilk birkaç gün içinde ortaya çıkar.Genellikle bu semptomlar kendi kendini sınırlar ve genellikle 2 hafta içinde düzelir, ancak bazı kişilerde uzayabilir (2-3 ay veya daha fazla) Bu nedenle Azur'un kademeli olarak tedavisini öneriyoruz. hastanın ihtiyaç duyduğu şekilde tedaviyi durdurmadan önce en az 1-2 haftalık bir süre boyunca azaltılarak azaltılır (bkz.
Kanama: SSRI'lar ile ekimoz ve purpura gibi kutanöz kanama belirtileri bildirilmiştir.Fluoksetin ile tedavi sırasında ekimoz seyrek görülen bir olay olarak bildirilmiştir. Diğer hemorajik belirtiler (örn. jinekolojik kanamalar, gastrointestinal kanama ve diğer kutanöz veya mukozal kanamalar) nadiren bildirilmiştir.
SSRI alan hastalarda, özellikle oral antikoagülanlar, trombosit fonksiyonunu etkilediği bilinen ilaçlar (örn. yanı sıra kanama bozukluğu öyküsü olan hastalarda.
Elektrokonvülsif tedavi (EKT): EKT tedavisi alan fluoksetin ile tedavi edilen hastalarda uzamış nöbetlere ilişkin seyrek raporlar olmuştur, bu nedenle dikkatli olunması önerilir.
Sarı kantaron: Seçici setononin geri alım inhibitörleri ve sarı kantaron (Hypericum perforatum) içeren bitkisel preparatlar birlikte kullanıldığında, serotonin sendromu gibi artmış serotonerjik tip etkiler meydana gelebilir.
Etkileşimler Hangi ilaçlar veya yiyecekler Azur'un etkisini değiştirebilir?
Yakın zamanda herhangi bir ilaç aldıysanız, reçetesiz de olsa, doktorunuza veya eczacınıza söyleyiniz.
Etkileşim çalışmaları sadece yetişkinlerde yapılmıştır.
Yarı ömür: Hem fluoksetinin hem de norfluoksetinin uzun eliminasyon yarı ömürleri, farmakodinamik veya farmakokinetik ilaç etkileşimleri değerlendirilirken (örn.
Monoamin Oksidaz İnhibitörleri: ("Kontrendikasyonlar" bölümüne bakınız).
Tavsiye edilmeyen kombinasyonlar: MAOI-Tip A ("Kontrendikasyonlar" bölümüne bakınız).
Kullanımları için önlem alınması gereken dernekler:
MAOI-Tip B (selegilin): serotonin sendromu riski. Klinik izleme önerilir.
Fenitoin: Fluoksetin ile kombine edildiğinde kan seviyelerinde değişiklikler gözlenmiştir. Bazı durumlarda, toksisite belirtileri meydana geldi. Bu nedenle fenitoinin konservatif terapötik rejimlere göre uygulanması ve hastanın klinik durumlarının dikkatle takip edilmesi tavsiye edilir.
Merkezi Sinir Sistemi İlaçları: Fluoksetin uygulaması karbamazepin, haloperidol, klozapin, alprazolam, imipramin ve desipramin kan düzeylerinin yükselmesine neden olabilir; bazı durumlarda toksisitenin klinik belirtileri gözlenmiştir. Bu nedenle, birlikte verilen ilacın ihtiyatlı terapötik şemalara göre uygulanması ve hastanın klinik durumlarının takip edilmesi tavsiye edilir.
Diazepam: Bu ilacın etkilerinin uzaması olabilir.
Serotonerjik ilaçlar: Serotonerjik ilaçlarla (örn. tramadol, triptanlar) birlikte uygulama, serotonin sendromu geliştirme riskini artırabilir. Triptanlarla ilişki, ek bir koroner vazokonstriksiyon ve arteriyel hipertansiyon riski ekler.
Lityum ve triptofan: SSRI'lar lityum veya triptofan ile kombinasyon halinde uygulandığında serotonin sendromu raporları olmuştur ve bu nedenle fluoksetinin bu ilaçlarla birlikte kullanımı dikkatle yapılmalıdır. Fluoksetin lityum ile kombinasyon halinde verildiğinde, daha hedefe yönelik ve sık klinik izleme gereklidir.
CYP2D6 izoenzimi: Fluoksetinin metabolizması (trisiklik antidepresanlar ve serotonin için diğer seçici antidepresanlarda olduğu gibi) karaciğerdeki sitokrom CYP2D6'nın izoenzimatik sistemini etkilediğinden, bu enzim sistemi tarafından eşit olarak metabolize edilen ilaçlarla eşzamanlı tedavi, ilaç etkileşimlerine yol açabilir. Ağırlıklı olarak bu izoenzim tarafından metabolize edilen ve sınırlı bir terapötik indekse sahip (flekainid, enkainid, karbamazepin ve trisiklik antidepresanlar gibi) ilaçlarla eşzamanlı tedavi, en düşük etkili dozdan başlatılmalı veya uyarlanmalıdır. Son 5 hafta içinde fluoksetin alınmış olsa bile bunun yapılması gerekecektir.
Oral antikoagülanlar: Homojen bir kategoriye girmeyen, ancak artan kanamayı içeren, değiştirilmiş antikoagülan etkiler (laboratuvar verileri ve/veya klinik semptom ve bulgular), fluoksetin ve oral antikoagülanların birlikte uygulanmasından sonra seyrek olarak gözlenmiştir. Varfarin alan hastalarda fluoksetin tedavisi başlatıldığında veya sonlandırıldığında, yakın pıhtılaşma takibi yapılmalıdır (bkz. "Kullanım Önlemleri", Kanama).
Elektrokonvülsif tedavi (EKT): EKT tedavisi alan fluoksetin ile tedavi edilen hastalarda uzamış nöbetlere ilişkin seyrek raporlar olmuştur, bu nedenle dikkatli olunması önerilir.
Alkol: Rutin testlerde fluoksetin kandaki alkol seviyelerinde artışa neden olmaz veya alkolün etkilerini potansiyalize etmez, ancak SSRI ve alkol tedavisinin kombinasyonu önerilmez.
Sarı kantaron: Fluoksetin ile sarı kantaron (Hypericum perforatum) içeren bitkisel preparat arasında, serotonerjik etkilerin artmasına ve yan etkilerin artmasına neden olabilecek farmakodinamik etkileşimler meydana gelebilir.
Uyarılar Şunları bilmek önemlidir:
Hamilelik, emzirme
Herhangi bir ilaç almadan önce doktorunuza veya eczacınıza danışınız. Hamileyseniz, hamile olduğunuzu düşünüyorsanız veya hamile kalmayı planlıyorsanız mümkün olan en kısa sürede doktorunuza söyleyiniz.
Hamile ve emzikli kadınlarda Azur tedavisi doktor ve kullanılan ilaç tarafından ancak beklenen yararlar fetüs üzerindeki potansiyel riski haklı çıkarıyorsa dikkatle değerlendirilmelidir.
Anneleri hamileliğin ilk aylarında Azur alan yeni doğan bebeklerle ilgili olarak, özellikle kalple ilgili olarak doğum kusurları riskinin arttığını gösteren veriler mevcuttur. Genel popülasyonda yaklaşık 1000 bebekten 1'i kalp kusurlu doğmaktadır, Azur alan annelerde bu oran 1000 bebekte 2'ye çıkmaktadır. Doktorunuzla birlikte, hamilelik sırasında Azur alımınızı kademeli olarak azaltmanın daha uygun olup olmadığına karar verebileceksiniz.Bununla birlikte, koşullara bağlı olarak, doktorunuz size Azur'u almaya devam etmenizi veya etmemenizi tavsiye edebilir.
Ebenizin ve/veya doktorunuzun Azur ile tedavi gördüğünüzü bildiğinden emin olun. Hamilelik sırasında, özellikle hamileliğin son 3 ayında alındığında, Azur gibi ilaçlar, yenidoğanda hızlı nefes almayı ve yenidoğanın görünümünü içeren yenidoğanda kalıcı pulmoner hipertansiyon (IPPN) olarak adlandırılan ciddi bir pediatrik durum riskini artırabilir. renk. mavimsi. Genellikle bu belirtiler bebek doğduktan sonraki ilk 24 saat içinde ortaya çıkar. Bebeğinizde bu belirtiler ortaya çıkarsa hemen ebenize ve/veya doktorunuza söyleyiniz.
Fluoksetin hamilelik sırasında, özellikle hamileliğin sonlarında veya doğum başlangıcından hemen önce kullanıldığında dikkatli olunmalıdır, çünkü yenidoğanlarda aşağıdaki etkiler rapor edilmiştir: sinirlilik, titreme, hipotoni, sürekli ağlama, emme veya uyuma güçlüğü. hem serotonerjik etkileri hem de yoksunluk sendromunu gösterir.
Laktasyon dönemi: Fluoksetin ve aktif metaboliti norfluoksetinin anne sütüne geçtiği bilinmektedir. Anne sütü ile beslenen bebeklerde advers olaylar bildirilmiştir. Fluoksetin tedavisi gerekli görülürse emzirmenin kesilmesi düşünülmeli, ancak emzirmeye devam edilirse etkili en düşük fluoksetin dozu reçete edilmelidir.
Erkek Doğurganlığı: Fluoksetinin hayvan çalışmalarında sperm kalitesini düşürdüğü gösterilmiştir. Teorik olarak, bu doğurganlığı etkileyebilir, ancak insan doğurganlığı üzerindeki etkisi henüz gözlemlenmemiştir.
Araç ve makine kullanma
Fluoksetinin sağlıklı gönüllülerde psikomotor performansı etkilemediği gösterilmiş olsa da, herhangi bir psikoaktif ilaç muhakeme veya mesleki becerileri bozabilir. Hastalara araç veya tehlikeli makine kullanmamaları tavsiye edilmelidir.
Dozaj ve kullanım yöntemi Azur nasıl kullanılır: Dozaj
Oral uygulama için.
Majör depresif dönemler
Yetişkinler ve yaşlılar:
Önerilen doz günde 20 mg'dır. Gerekirse, dozaj, tedavinin başlamasından sonraki 3-4 hafta içinde gözden geçirilmeli ve düzeltilmelidir ve ardından klinik olarak uygunsa değerlendirilmelidir.Daha yüksek dozlarda artan yan etkiler için bir potansiyel olmasına rağmen, 20 mg'a yetersiz terapötik yanıt olan bazı hastalarda , doz kademeli olarak maksimum 60 mg'a kadar artırılabilir. Hastayı en düşük etkili dozda tutmak için her bir birey için doz ayarlamaları dikkatli bir şekilde yapılmalıdır.
Depresyonlu hastalar, semptomsuz olduklarından emin olmak için en az 6 aylık yeterli bir süre boyunca tedavi edilmelidir.
Obsesif kompulsif bozukluk
Yetişkinler ve yaşlılar: Önerilen doz günde 20 mg'dır. Günde 20 mg'dan daha yüksek dozlarda bazı hastalarda yan etkilerde potansiyel bir artış olmasına rağmen, iki hafta sonra 20 mg'a yetersiz terapötik yanıt varsa, doz kademeli olarak maksimum 60 mg'a yükseltilebilir.
10 hafta içinde herhangi bir iyileşme gözlenmezse fluoksetin tedavisi yeniden değerlendirilmelidir. İyi bir terapötik yanıt elde edilmişse, tedaviye bireysel olarak ayarlanmış bir dozda devam edilebilir. Fluoksetin tedavisine ne kadar süreyle devam edileceğini belirleyen sistematik bir çalışma olmamasına rağmen, OKB kronik bir durumdur ve yanıt veren hastalarda tedaviyi 10 haftadan fazla uzatmayı düşünmek mantıklıdır. Hastayı en düşük etkili dozda tutmak için her bireyde doz değişiklikleri dikkatli bir şekilde yapılmalıdır. Tedavi ihtiyacı periyodik olarak yeniden değerlendirilmelidir. Farmakoterapiye iyi yanıt veren hastalarda, bazı klinisyenler eşzamanlı davranışsal psikoterapiyi faydalı bulmaktadır.
OKB'de uzun süreli etkinlik (24 haftanın ötesinde) gösterilmemiştir.
Bulimia nervoza
Yetişkinler ve yaşlılar: Günde 60 mg'lık bir doz önerilir. Bulimia nervozada uzun süreli etkinlik (3 ayın ötesinde) gösterilmemiştir.
yetişkinler
Tüm endikasyonlarda: Önerilen doz artırılabilir veya azaltılabilir. Günde 80 mg'ın üzerindeki dozlar sistematik olarak değerlendirilmemiştir.
Fluoksetin, yemekle birlikte veya yemeksiz tek veya bölünmüş dozlarda uygulanabilir.
Dozlama durdurulduğunda, farmakolojik olarak aktif maddeler vücutta haftalarca kalacaktır.Tedaviye başlarken veya durdururken bu akılda tutulmalıdır.
8 yaş ve üzeri çocuklar ve ergenler (Orta ila şiddetli majör depresif dönem)
Azur, 8 ila 18 yaş arası çocuklarda ve ergenlerde yalnızca orta ila şiddetli majör depresif atakların tedavisinde kullanım içindir ve diğer endikasyonlarda kullanılmamalıdır.
Tedaviye uzman gözetiminde başlanmalı ve izlenmelidir. Başlangıç dozu günde 10 mg'dır. Hastayı en düşük etkili dozda tutmak için doz ayarlamaları bireysel olarak dikkatli bir şekilde yapılmalıdır.
Bir ila iki hafta sonra, doz günde 20 mg'a yükseltilebilir. 20 mg'ın üzerindeki günlük dozlarla ilgili klinik deneyim minimumdur.9 haftadan sonraki tedaviyle ilgili yalnızca sınırlı veri vardır.
Düşük vücut ağırlığına sahip çocuklar
Düşük vücut ağırlıklı çocuklarda elde edilen daha yüksek plazma seviyeleri nedeniyle, daha düşük dozlarda terapötik etki elde edilebilir.
Tedaviye yanıt veren pediatrik hastalarda 6 ay sonra tedaviye devam etme ihtiyacı yeniden değerlendirilmelidir. 9 hafta içinde klinik yarar sağlanamazsa, tedavi yeniden gözden geçirilmelidir.
Yaşlılar: Doz artırılırken dikkatli olunması önerilir ve günlük doz genellikle 40 mg'ı geçmemelidir. Önerilen maksimum doz günde 60 mg'dır.
Karaciğer yetmezliği olan hastalarda veya "Azur ile kombinasyon halinde alınan tıbbi ürünler arasında etkileşim" potansiyeli olan hastalarda daha düşük veya daha az sıklıkta bir doz (örn. gün aşırı 20 mg) düşünülmelidir (bkz. Etkileşimler paragrafı).
Azur tedavisinin kesilmesiyle görülen yoksunluk belirtileri:
Azur tedavisi durdurulurken, yoksunluk reaksiyonları riskini azaltmak için doz en az 1-2 haftalık bir süre içinde kademeli olarak azaltılmalıdır (bkz. "). Doz azaltıldıktan veya tedavinin kesilmesinden sonra tolere edilemeyen semptomlar ortaya çıkarsa, önceden reçete edilen dozun yeniden başlatılması düşünülebilir. Bundan sonra, doktor dozu azaltmaya devam edebilir, ancak daha yavaş olabilir.
Aşırı doz Çok fazla Azur aldıysanız ne yapmalısınız?
Azur'un kazara yutulması/aşırı dozda alınması durumunda derhal doktorunuza haber veriniz veya en yakın hastaneye başvurunuz.
Tek başına fluoksetine bağlı doz aşımı vakaları genellikle hafif seyreder. Doz aşımı semptomları mide bulantısı, kusma, nöbetler, asemptomatik aritmiden kardiyak arreste kadar değişen kardiyovasküler disfonksiyon, pulmoner disfonksiyon ve heyecandan komaya kadar değişen bir CNS durumunun değişmiş belirtilerini içerir. kardiyak fonksiyon ve yaşamsal belirtilerin yanı sıra genel semptomatik ve destekleyici önlemleri izlemek için Spesifik bir antidot bilinmemektedir.
Zorla diürez, diyaliz, hemoperfüzyon ve replasman transfüzyonunun fayda sağlaması olası değildir.Sorbitol ile birlikte kullanılabilen aktif kömür, kusma veya gastrik lavajdan bile daha etkili bir tedavi olabilir. Bir doz aşımını tedavi ederken, çoklu ilaç tutulum olasılığını göz önünde bulundurun. Aşırı miktarda trisiklik antidepresan alan hastalarda, fluoksetin de alıyorlarsa veya yakın zamanda almışlarsa, yakın tıbbi gözlem için daha uzun bir süre gerekebilir.
Azur'un kullanımı hakkında şüpheniz varsa, doktorunuza veya eczacınıza danışınız.
İHMAL EDİLMİŞ YÖNETİM (ÇEKİM SENDROMU).
Bir veya daha fazla dozun kazara alınmaması durumunda, yoksunluk sendromunun başlama riski minimumdur.
Yan Etkiler Azur'un yan etkileri nelerdir?
Tüm ilaçlar gibi, Azur da yan etkilere neden olabilir, ancak bu yan etkiler herkeste görülmez.İstenmeyen etkilerin yoğunluğu ve sıklığı tedavinin devam etmesiyle azalabilir ve genellikle tedavinin kesilmesine yol açmaz.
Diğer SSRI'larda olduğu gibi, aşağıdaki yan etkiler gözlenmiştir:
Bir bütün olarak vücut: Aşırı duyarlılık belirtileri (örneğin, kaşıntı, döküntü, ürtiker, anafilaktoid reaksiyon, vaskülit, serum hastalığına benzer reaksiyon, anjiyoödem) ("Kontrendikasyonlar" bölümüne ve "Kullanım önlemleri" bölümüne bakın), titreme , serotonin sendromu, Stevens-Johnson sendromu veya toksik epidermal nekroliz (Lyell sendromu) başlangıcına kadar ilerleyebilen ışığa duyarlılık ve çok nadiren eritema multiforme.
Kardiyovasküler sistem: Angina pektoris, aritmiler, 1. derece atriyoventriküler blok, hipotansiyon, hipertansiyon.
Sindirim sistemi: Gastrointestinal rahatsızlıklar (örn. ishal, bulantı, kusma, hazımsızlık, yutma güçlüğü, tat değişikliği), ağız kuruluğu. Anormal karaciğer fonksiyon testleri nadiren bildirilmiştir. Çok nadir idiyosenkratik hepatit vakaları.
Sinir sistemi: Baş ağrısı, uyku bozuklukları (örn. anormal rüyalar, uykusuzluk, uyuklama), baş dönmesi, anoreksi, yorgunluk, somnolans (örn. uyuşukluk), öfori, geçici anormal hareketler (örn. sinir tikleri, ataksi, titreme, miyoklonus), nöbetler ve nadiren psikomotor Huzursuzluk / akatizi ("Kullanım önlemleri" bölümüne bakınız) Çok nadiren serotonin sendromu.
Psikiyatrik bozukluklar: Halüsinasyonlar, manik reaksiyon, konfüzyon, ajitasyon, anksiyete ve ilişkili semptomlar (örn. sinirlilik), bozulmuş konsantrasyon ve bilişsel süreç (örn. duyarsızlaşma), panik atak, intihar davranışı ve düşünceleri (bu semptomlar altta yatan bir hastalığa bağlı olabilir).
Fluoksetin tedavisi sırasında veya tedavinin kesilmesinden hemen sonra intihar düşüncesi ve intihar davranışı vakaları bildirilmiştir (bkz. "Kullanım önlemleri" bölümü).
Ürogenital sistem: İdrar retansiyonu ve değişen idrar sıklığı.
Üreme sistemi bozuklukları: cinsel işlev bozukluğu (gecikmiş veya yok boşalma, anorgazmi), priapizm, galaktore, hiperprolaktinemi.
Çeşitli: Alopesi, esneme, görme anormallikleri (örn. bulanık görme, midriyazis), terleme, vazodilatasyon, artralji, miyalji, postural hipotansiyon, ekimoz, hipoglisemi, hipokalemi. Nadiren diğer hemorajik belirtiler (örn. jinekolojik kanamalar, gastrointestinal kanama ve diğer kutanöz veya mukozal kanamalar) bildirilmiştir (bkz. "Kullanım Önlemleri", Kanama).
Hiponatremi: Hiponatremi (110 mmol / l'nin altındaki sodyum seviyeleri dahil) nadiren bildirilmiştir ve fluoksetinin kesilmesiyle geri dönüşümlüdür.Bazı vakalar muhtemelen uygunsuz antidiüretik hormon salgılanması sendromuna bağlıydı.Çoğu rapor yaşlı hastalarda ve hastalarda bulunmuştur. diüretiklerle veya başka herhangi bir nedenle kan hacminde azalma ile tedavi edilir.
Solunum sistemi: Farenjit, dispne. Nadiren pulmoner olaylar (değişken histopatoloji ve/veya fibrozun inflamatuar süreçleri dahil) bildirilmiştir. Dispne tek uyarı semptomu olabilir.
Kemik kırıkları: Bu tür ilaçları alan hastalarda kemik kırığı riskinde artış gözlenmiştir.
Fluoksetin Tedavisi Kesildiğinde Görülen Yoksunluk Belirtileri: Fluoksetin tedavisinin kesilmesi genellikle yoksunluk belirtilerine yol açar. En sık bildirilen reaksiyonlar baş dönmesi, duyu bozuklukları (parestezi dahil), uyku bozuklukları (uykusuzluk ve yoğun rüyalar dahil), asteni, ajitasyon veya anksiyete, bulantı ve/veya kusma, titreme ve baş ağrısıdır. Genellikle bu semptomlar hafif ila orta şiddettedir ve kendi kendini sınırlar, ancak bazı hastalarda şiddetli ve/veya uzun süreli olabilir (bkz. Azur ile tedavi artık gerekli olmadığında dozlayın (bkz. "Doz, uygulama yöntemi ve zamanı" ve "Kullanım önlemleri" bölümü).
Çocuklar ve ergenler ("Kullanım Önlemleri" bölümüne bakın):
Pediyatrik klinik çalışmalarda, intiharla ilgili davranışlar (intihar girişimi ve intihar düşünceleri) ve düşmanca tutum, antidepresanlarla tedavi edilen çocuk ve ergenlerde plasebo ile tedavi edilenlere göre daha sık gözlenmiştir.
Fluoksetinin güvenliği, 19 haftadan uzun süren kronik tedaviler için sistematik olarak değerlendirilmemiştir.
Pediyatrik klinik çalışmalarda, mani ve hipomani (fluoksetin ile tedavi edilen hastalarda %2,6 ve plasebo kontrollü hastalarda %0) dahil olmak üzere manik reaksiyonlar rapor edilmiş ve çoğu vakada tedavinin kesilmesine neden olmuştur. Bu hastalarda daha önce hipomani / mani atağı yoktu.
19 haftalık tedaviden sonra, bir klinik çalışmada fluoksetin ile tedavi edilen pediyatrik hastalar, plasebo ile tedavi edilen deneklere göre ortalama 1,1 cm daha kısa (p = 0,004) ve ağırlık olarak 1,1 kg daha az (p = 0,008) rapor etmiştir.
Klinik kullanımda izole büyüme geriliği vakaları da bildirilmiştir.Pediatrik klinik kullanımda potansiyel olarak gecikmiş cinsel olgunlaşmayı veya cinsel işlev bozukluğunu gösteren izole advers olay vakaları bildirilmiştir.
Pediyatrik klinik çalışmalarda, fluoksetin tedavisi, kandaki alkalin fosfataz seviyelerinde bir azalma ile ilişkilendirilmiştir.
Yan etkilerden herhangi biri ciddileşirse veya bu kullanma talimatında listelenmeyen herhangi bir yan etki fark ederseniz, lütfen doktorunuza veya eczacınıza haber veriniz.
Kullanma talimatında yer alan talimatlara uyulması, istenmeyen etki riskini azaltır. Kullanma talimatında belirtilmemiş olsa bile istenmeyen etkilerin doktor veya eczacıya bildirilmesi önemlidir.
Son Kullanma ve Saklama
Paketin üzerinde yazılı olan son kullanma tarihine bakın.
Son kullanma tarihi, ürünün bozulmamış ambalajında, doğru şekilde saklanmış olduğunu ifade eder.
Uyarı: Paket üzerinde belirtilen son kullanma tarihinden sonra ilacı kullanmayınız. 30°C'nin altında saklayınız.
İlaçlar atık su veya evsel atıklar yoluyla atılmamalıdır.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorunuz.Bu çevrenin korunmasına yardımcı olacaktır.
TIBBİ ÜRÜNÜ ÇOCUKLARIN ERİŞİMİNDEN VE GÖRÜŞÜNDEN UZAK TUTUN
Kompozisyon ve farmasötik form
KOMPOZİSYON
Her kapsül içerir:
aktif madde: Fluoksetin hidroklorür 22.36 mg
fluoksetin 20 mg'a eşdeğer
yardımcı maddeler: Mısır nişastası, Dimetikon, Jelatin, Titanyum dioksit.
FARMASÖTİK FORM VE İÇERİĞİ
20 mg sert kapsüller. 28 kapsüllük kutu
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
AZUR 20 MG SERT KAPSÜL
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Her kapsül içerir:
Aktif prensip:
Fluoksetin hidroklorür 22.36 mg
fluoksetin 20 mg'a eşittir
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakınız.
03.0 FARMASÖTİK FORM
Sert kapsüller
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
AZUR, depresyon, obsesif kompulsif bozukluk ve bulimia nervoza tedavisinde endikedir.
04.2 Pozoloji ve uygulama yöntemi
Oral uygulama için.
Majör depresif dönemler
Yetişkinler ve yaşlılar:
Önerilen doz günde 20 mg'dır. Gerekirse, doz yeniden incelenmeli ve tedavinin başlangıcından sonraki 3-4 hafta içinde düzeltilmeli ve daha sonra klinik olarak uygunsa değerlendirilmelidir. 20 mg, doz kademeli olarak maksimum 60 mg'a kadar artırılabilir (bkz. bölüm 5.1 "Farmakodinamik özellikler") Hastayı en düşük etkili dozda tutmak için doz ayarlamaları bireysel olarak dikkatli bir şekilde yapılmalıdır.
Depresyonlu hastalar, semptomsuz olduklarından emin olmak için en az 6 aylık yeterli bir süre boyunca tedavi edilmelidir.
Obsesif kompulsif bozukluk
Yetişkinler ve yaşlılar: Önerilen doz günde 20 mg'dır. Günde 20 mg'dan daha yüksek dozlarda bazı hastalarda yan etkilerde potansiyel bir artış olmasına rağmen, iki hafta sonra 20 mg'a yetersiz terapötik yanıt varsa, doz kademeli olarak maksimum 60 mg'a yükseltilebilir.
10 hafta içinde herhangi bir iyileşme gözlenmezse fluoksetin tedavisi yeniden değerlendirilmelidir. İyi bir terapötik yanıt elde edilmişse, tedaviye bireysel olarak ayarlanmış bir dozda devam edilebilir. Fluoksetin tedavisine ne kadar süreyle devam edileceğini belirleyen sistematik bir çalışma olmamasına rağmen, OKB kronik bir durumdur ve yanıt veren hastalarda tedaviyi 10 haftadan fazla uzatmayı düşünmek mantıklıdır. Hastayı en düşük etkili dozda tutmak için her bireyde doz değişiklikleri dikkatli bir şekilde yapılmalıdır. Tedavi ihtiyacı periyodik olarak yeniden değerlendirilmelidir. Farmakoterapiye iyi yanıt veren hastalarda, bazı klinisyenler eşzamanlı davranışsal psikoterapiyi faydalı bulmaktadır.
OKB'de uzun süreli etkinlik (24 haftanın ötesinde) gösterilmemiştir.
Bulimia nervoza
Yetişkinler ve yaşlılar: Günde 60 mg'lık bir doz önerilir. Bulimia nervozada uzun süreli etkinlik (3 ayın ötesinde) gösterilmemiştir.
yetişkinler
Tüm göstergelerde: Önerilen doz artırılabilir veya azaltılabilir. Günde 80 mg'ın üzerindeki dozlar sistematik olarak değerlendirilmemiştir.
Fluoksetin, yemekle birlikte veya yemeksiz tek veya bölünmüş dozlarda uygulanabilir.
Dozlama durdurulduğunda, farmakolojik olarak aktif maddeler vücutta haftalarca kalacaktır.Tedaviye başlarken veya durdururken bu akılda tutulmalıdır.
8 yaş ve üzeri çocuklar ve ergenler (Orta ila şiddetli majör depresif dönem)
Tedaviye uzman gözetiminde başlanmalı ve izlenmelidir. Başlangıç dozu günde 10 mg'dır. Hastayı en düşük etkili dozda tutmak için doz ayarlamaları bireysel olarak dikkatli bir şekilde yapılmalıdır.
Bir ila iki hafta sonra, doz günde 20 mg'a yükseltilebilir. 20 mg'ın üzerindeki günlük dozlarla ilgili klinik deneyim minimumdur.9 haftadan sonraki tedaviyle ilgili yalnızca sınırlı veri vardır.
Düşük vücut ağırlığına sahip çocuklar
Düşük vücut ağırlıklı çocuklarda elde edilen daha yüksek plazma seviyeleri nedeniyle, terapötik etki daha düşük dozlarla elde edilebilir (bkz. bölüm 5.2).
Tedaviye yanıt veren pediatrik hastalarda 6 ay sonra tedaviye devam etme ihtiyacı yeniden değerlendirilmelidir. 9 hafta içinde klinik yarar sağlanamazsa, tedavi yeniden gözden geçirilmelidir.
Yaşlılar: Doz artırılırken dikkatli olunması önerilir ve günlük doz genellikle 40 mg'ı geçmemelidir. Önerilen maksimum doz günde 60 mg'dır.
Karaciğer yetmezliği olan hastalarda (bkz. bölüm 5.2 Farmakokinetik özellikler) veya "Azur. kombinasyon (bkz. Bölüm 4.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleri).
Azur tedavisinin kesilmesiyle gözlenen yoksunluk belirtileri:
Azur tedavisinin aniden kesilmesinden kaçınılmalıdır.Azur tedavisi kesilirken, yoksunluk reaksiyonları riskini azaltmak için doz en az 1-2 haftalık bir süre içinde kademeli olarak azaltılmalıdır (bkz. bölüm 4.4 "Özel kullanım uyarıları ve önlemleri" ve bölüm 4.8" İstenmeyen etkiler ") Dozun azaltılmasını veya tedavinin kesilmesini takiben tolere edilemeyen semptomlar ortaya çıkarsa, daha önce reçete edilen doza devam edilmesi düşünülebilir. Bundan sonra, doktor dozu azaltmaya devam edebilir, ancak daha yavaş olabilir.
04.3 Kontrendikasyonlar
Kimyasal açıdan ürünün bileşenlerine veya yakından ilişkili diğer maddelere karşı aşırı duyarlılık.
Fluoksetin, MAO inhibitörleri ile aynı zamanda alınmamalıdır (bkz. bölüm 4.4 "Özel kullanım uyarıları ve özel önlemler" ve bölüm 4.5 "Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim şekilleri").
Genellikle hamilelikte kontrendikedir (bkz. bölüm 4.6 "Hamilelik ve emzirme").
Fluoksetine veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
Monoamin Oksidaz İnhibitörleri: Bir monoamin oksidaz inhibitörü (MAOI) ile kombinasyon halinde SSRI alan hastalarda ve yakın zamanda bir SSRI ile tedaviyi bırakmış ve bir MAOI ile tedaviye başlayan hastalarda ciddi ve bazen ölümcül reaksiyon vakaları bildirilmiştir. Fluoksetin tedavisine ancak geri dönüşü olmayan bir MAOI ile tedavi durdurulduktan 2 hafta sonra ve geri dönüşümlü bir MAO-A durdurulduktan bir gün sonra başlanmalıdır.
Bazı vakalar serotonin sendromuna benzer özellikler sunmuştur (nöroleptik malign sendroma benzeyebilir ve teşhis edilebilir). Siproheptadin veya dantrolen, bu tür reaksiyonları olan hastalarda faydalı olabilir. Bir MAOI ile bir ilaç etkileşiminin semptomları şunları içerir: hipertermi, sertlik, miyoklonus, hayati belirtilerde olası hızlı dalgalanmalar ile otonom sinir sistemi kararsızlığı, konfüzyon, sinirlilik ve deliryum ve komaya yol açan aşırı ajitasyon dahil zihinsel durum değişiklikleri.
Bu nedenle fluoksetin, seçici olmayan bir MAOI ile kombinasyon halinde kontrendikedir. Aynı şekilde, bir MAOI ile tedaviye başlamadan önce fluoksetin tedavisinin kesilmesinden sonra en az 5 hafta geçmelidir Fluoksetin uzun süre ve/veya yüksek dozlarda reçete edilirse, daha uzun bir zaman aralığı düşünülmelidir.
Fluoksetinin geri dönüşümlü bir MAOI (örn. moklobemid) ile kombinasyonu önerilmez Fluoksetin tedavisine geri dönüşümlü bir MAOI ile tedavi durdurulduktan sonraki gün başlanabilir.
04.4 Özel uyarılar ve uygun kullanım önlemleri
Kullanıma İlişkin Özel Uyarılar ve Önlemler
Uyarılar
18 yaşın altındaki çocuklar ve ergenler tarafından kullanım için
İntiharla ilgili davranışlar (intihar girişimi ve intihar düşünceleri) ve düşmanca tutum (özellikle saldırgan, karşı gelme ve öfke davranışı), antidepresanlarla tedavi edilen çocuk ve ergenlerin klinik çalışmalarında, plasebo ile tedavi edilenlere göre daha sık gözlenmiştir. Azur, 8 ila 18 yaş arası çocuklarda ve ergenlerde yalnızca orta ila şiddetli majör depresif atakların tedavisinde kullanım içindir ve diğer endikasyonlarda kullanılmamalıdır. Tıbbi ihtiyaca göre tedavi kararı verilirse, hasta intihar semptomlarının ortaya çıkması açısından dikkatle izlenmelidir. Ayrıca, büyüme, cinsel olgunlaşma ve bilişsel, duygusal ve davranışsal gelişim üzerindeki etkiler de dahil olmak üzere güvenlik üzerindeki uzun vadeli etkilere ilişkin çocuklarda ve ergenlerde yalnızca sınırlı veriler mevcuttur (bkz. bölüm 5.3).
19 haftalık bir klinik çalışmada, fluoksetin ile tedavi edilen çocuk ve adolesanlarda boy ve kilo artışında azalma gözlenmiştir (bkz. bölüm 4.8) Boy, normal yetişkin boyuna ulaşılması üzerinde bir etkisi olup olmadığı belirlenmemiştir. Ergenlikte gecikme olasılığı göz ardı edilemez (bkz. Bölüm 5.3 ve 4.8). Bu nedenle fluoksetin tedavisi sırasında ve sonrasında pubertal büyüme ve gelişme (boy, kilo ve TANNER'a göre etki aşamaları) izlenmelidir.Her ikisi de yavaşlarsa, bir pediatrik değerlendirme istenmelidir.
Pediyatrik klinik çalışmalarda mani ve hipomani sıklıkla bildirilmiştir (bkz. bölüm 4.8). Bu nedenle mani/hipomani başlangıcı için düzenli izleme önerilir. Manik faza giren herhangi bir hastada fluoksetin kesilmelidir.
Doktorun çocuk veya genç ve/veya ebeveynleri ile tedavinin risklerini ve yararlarını dikkatlice tartışması önemlidir.
Deri döküntüsü ve alerjik reaksiyonlar: Döküntü, anafilaktoid olaylar ve bazen ciddi (cilt, böbrek, karaciğer veya akciğeri içeren) ilerleyici sistemik olaylar bildirilmiştir. Farklı bir etiyolojisi tanımlanamayan deri döküntüsü veya diğer alerjik fenomenlerin ortaya çıkması üzerine fluoksetin uygulaması kesilmelidir.
Önlemler
Konvülsiyonlar: nöbetler, antidepresan ilaçlarla potansiyel bir risk oluşturur. Bu nedenle, diğer antidepresanlarda olduğu gibi, fluoksetin nöbet öyküsü olan hastalara dikkatle uygulanmalıdır. Nöbet gelişen veya nöbet sıklığında artış görülen herhangi bir hastada tedavi kesilmelidir. Stabil olmayan nöbet bozuklukları / epilepsisi olan hastalarda fluoksetin uygulamasından kaçınılmalı ve kontrollü epilepsisi olan hastalar dikkatle izlenmelidir.
mani: Mani/hipomani öyküsü olan hastalarda antidepresanlar dikkatli kullanılmalıdır. Tüm antidepresan ilaçlar gibi, manik faza giren herhangi bir hastada fluoksetin kesilmelidir.
Hepatik / Böbrek Fonksiyonu: Fluoksetin, karaciğer tarafından büyük ölçüde metabolize edilir ve böbrekler tarafından elimine edilir. Önemli karaciğer fonksiyon bozukluğu olan hastalarda günde 20 mg'lık daha düşük bir doz önerilir, örn. alternatif bir gün dozu. 2 ay boyunca günde 20 mg fluoksetin uygulandığında, şiddetli böbrek yetmezliği (GFR diyalizi) olan hastalar, normal böbrek fonksiyonu olan kontrol deneklerine kıyasla fluoksetin veya norfluoksetinin plazma seviyelerinde hiçbir fark göstermedi.
Kalp hastalığı: Çift kör klinik çalışmalarda fluoksetin alan 312 hastada EKG'de kardiyak arreste yol açan iletim değişikliklerinin hiçbiri gözlenmedi.
Bununla birlikte, akut kalp hastalığında klinik deneyim sınırlıdır ve dikkatli olunması önerilir.
Kilo kaybıFluoksetin alan hastalarda kilo kaybı olabilir, ancak bu genellikle başlangıç vücut ağırlığı ile orantılıdır.
Şeker hastalığı: Diyabetik hastalarda SSRI tedavisi glisemik kontrolü bozabilir. Fluoksetin tedavisi sırasında hipoglisemi meydana gelirken, ilacın kesilmesinden sonra hiperglisemi gelişti. İnsülin ve/veya oral hipoglisemik ajanın doz ayarlaması gerekebilir.
İntihar / intihar düşünceleri veya klinik kötüleşme: Depresyon, intihar düşünceleri, kendine zarar verme ve intihar (intiharla ilgili olaylar) riskinin artmasıyla ilişkilidir. Bu risk, hastalıkta belirgin bir remisyon gerçekleşene kadar devam eder. Tedavinin ilk veya sonraki haftalarında düzelme olmayabileceğinden, hastalar iyileşme gerçekleşene kadar yakından izlenmelidir. İyileşme sürecinin erken dönemlerinde intihar riskinin artabileceği genel klinik deneyimdir.
Azur'un reçete edildiği diğer psikiyatrik durumlar da intiharla ilgili olayların riskinin artmasıyla ilişkilendirilebilir. Ayrıca, bu durumlar majör depresif bozuklukla birlikte olabilir. Bu nedenle, majör depresif bozukluğu olan hastaları tedavi ederken gözlemlenen önlemlerin aynıları, diğer psikiyatrik bozuklukları olan hastaları tedavi ederken de uygulanmalıdır.
İntiharla ilgili olay öyküsü olan hastalar arasında, tedaviye başlamadan önce önemli derecede intihar düşüncesi olanlar, artan intihar düşüncesi ve intihar girişimi riskine sahiptir ve tedavi sırasında yakından izlenmelidir. Psikiyatrik bozuklukların tedavisinde plaseboya kıyasla antidepresan ilaçlarla yürütülen çalışmalar, plaseboya kıyasla antidepresanlarla tedavi edilen 25 yaşın altındaki hastalarda intihar davranışı riskinde artış göstermiştir.
Hastaların ve özellikle yüksek risk altındakilerin yakın gözetimi, özellikle tedavinin ilk aşamalarında ve doz değişikliklerinden sonra ilaç tedavisine eşlik etmelidir. Hastalar (veya bakıcıları), bu semptomlar ortaya çıkarsa, klinik tablodaki herhangi bir kötüleşmeyi, intihar davranışı veya düşüncelerinin başlangıcını veya davranışta olağandışı değişiklikleri izlemeleri ve tedavi eden doktora derhal bildirmeleri gerektiği konusunda bilgilendirilmelidir.
Akatizi / psikomotor huzursuzluk: Fluoksetin kullanımı, "sübjektif olarak hoş olmayan veya rahatsız edici bir huzursuzluk ve sıklıkla oturma veya hareketsiz duramama ile birlikte hareket etme ihtiyacı" ile karakterize akatizi gelişimi ile ilişkilendirilmiştir. Bu durumun, tedavinin ilk haftalarında ortaya çıkması daha olasıdır. Bu semptomları gelişen hastalarda dozun arttırılması zararlı olabilir.
SSRI tedavisinin kesilmesiyle gözlenen yoksunluk semptomları: Tedavi durdurulduğunda, özellikle tedavi aniden kesilirse, kesilme semptomları yaygındır (bkz. bölüm 4.8 "İstenmeyen etkiler") Klinik çalışmalarda, hem fluoksetin hem de plasebo grubundaki hastaların yaklaşık %60'ında tedavinin aniden kesilmesiyle gözlenen advers olaylar görülmüştür. . Bu yan etkilerden fluoksetin grubunda %17'si ve plasebo grubunda %12'si şiddetliydi.
Yoksunluk semptomları riski, tedavinin süresi ve dozu ve doz azaltma oranı dahil olmak üzere çeşitli faktörlere bağlı olabilir. En sık bildirilen reaksiyonlar baş dönmesi, duyu bozuklukları (parestezi dahil), uyku bozuklukları (uykusuzluk ve yoğun rüyalar dahil), asteni, ajitasyon veya anksiyete, bulantı ve/veya kusma, titreme ve baş ağrısıdır. Genellikle bu semptomlar hafif ila orta şiddettedir, ancak bazı hastalarda şiddetli olabilir. Bu semptomlar genellikle tedaviyi bıraktıktan sonraki ilk birkaç gün içinde ortaya çıkar.Genellikle bu semptomlar kendi kendini sınırlar ve bazı kişilerde uzayabilir (2-3 ay veya daha fazla) olmasına rağmen genellikle 2 hafta içinde düzelir.Bu nedenle Azur'un kademeli olarak tedavisini öneriyoruz. hastanın ihtiyaç duyduğu şekilde tedaviyi durdurmadan önce en az 1-2 haftalık bir süre boyunca azaltılır (bkz. "Azur tedavisinin kesilmesiyle gözlenen yoksunluk semptomları" bölüm 4.2 Pozoloji ve uygulama yöntemi).
kanamaSSRI'ların kullanımı ile ekimoz ve purpura gibi deri kanaması belirtileri bildirilmiştir. Diğer hemorajik belirtiler (örn. jinekolojik kanamalar, gastrointestinal kanama ve diğer kutanöz veya mukozal kanamalar) nadiren bildirilmiştir.
SSRI alan hastalarda, özellikle oral antikoagülanlar, trombosit fonksiyonunu etkilediği bilinen ilaçlar (örn. yanı sıra kanama bozukluğu öyküsü olan hastalarda.
Elektrokonvülsif tedavi (ECT): EKT tedavisi alan fluoksetin ile tedavi edilen hastalarda uzamış nöbetlere ilişkin seyrek raporlar olmuştur, bu nedenle dikkatli olunması önerilir.
Sarı Kantaron: Seçici serotonin geri alım inhibitörleri ve St. John's wort içeren bitkisel müstahzarlar (Hypericum perforatum) birlikte kullanıldığında serotonin sendromu gibi artmış serotonerjik tip etkiler meydana gelebilir.
Nadir durumlarda, özellikle fluoksetin diğer serotonerjik ilaçlarla (diğerlerinin yanı sıra L-triptofan) ve/veya nöroleptiklerle birlikte uygulandığında, fluoksetin tedavisiyle ilişkili olarak bir serotonin sendromu veya nöroleptik malign sendrom benzeri olayların gelişimi bildirilmiştir. Bu sendromlar hasta için potansiyel olarak yaşamı tehdit eden durumlara yol açabileceğinden, bu tür olaylar meydana gelirse (hipertermi, rijidite, miyoklonus, otonom sinir sistemi dengesizliği ve hayati belirtilerde olası hızlı dalgalanmalar gibi semptom grupları ile karakterize edilir, konfüzyon, sinirlilik ve deliryum ve komaya varan aşırı ajitasyon) fluoksetin tedavisi kesilmeli ve semptomatik destekleyici tedavi başlatılmalıdır.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Etkileşim çalışmaları sadece yetişkinlerde yapılmıştır.
Yarım hayat: Hem fluoksetinin hem de norfluoksetinin uzun eliminasyon yarı ömürleri, farmakodinamik veya farmakokinetik ilaç etkileşimleri (örn.
Monoamin Oksidaz İnhibitörleri: (bkz. bölüm 4.3 "Kontrendikasyonlar").
Tavsiye edilmeyen kombinasyonlar: MAOI-Tip A (bkz. bölüm 4.3).
Kullanımları için önlem alınması gereken dernekler:
MAOI-Tip B (selegilin): serotonin sendromu riski.Klinik izleme önerilir.
fenitoinFluoksetin ile kombine edildiğinde kan seviyelerinde değişiklikler gözlenmiştir. Bazı durumlarda, toksisite belirtileri meydana geldi. Bu nedenle fenitoinin konservatif terapötik rejimlere göre uygulanması ve hastanın klinik durumlarının dikkatle takip edilmesi tavsiye edilir.
Merkezi sinir sistemi ilaçları: Fluoksetin uygulaması karbamazepin, haloperidol, klozapin, alprazolam, imipramin ve desipramin kan düzeylerinin artmasına neden olabilir; bazı durumlarda toksisitenin klinik belirtileri gözlenmiştir. Bu nedenle, birlikte verilen ilacın ihtiyatlı terapötik şemalara göre uygulanması ve hastanın klinik durumlarının takip edilmesi tavsiye edilir.
diazepam: Bu ilacın etkilerinde uzama olabilir.
Serotonerjik ilaçlar: Serotonerjik ilaçlarla (örn. tramadol, triptanlar) birlikte uygulama, serotonin sendromu geliştirme riskini artırabilir. Triptanlarla ilişki, ek bir koroner vazokonstriksiyon ve arteriyel hipertansiyon riski ekler.
Lityum ve triptofan: SSRI'lar lityum veya triptofan ile kombinasyon halinde uygulandığında serotonin sendromu raporları olmuştur ve bu nedenle fluoksetinin bu ilaçlarla birlikte kullanımı dikkatle yapılmalıdır. Fluoksetin lityum ile kombinasyon halinde verildiğinde, daha hedefe yönelik ve sık klinik izleme gereklidir.
CYP2D6 izoenzim: Fluoksetinin metabolizması (trisiklik antidepresanlar ve serotonin için diğer seçici antidepresanlar için olduğu gibi) karaciğerdeki CYP2D6 izoenzimatik sistemini etkilediğinden, bu enzim sistemi tarafından eşit olarak metabolize edilen ilaçlarla eşzamanlı tedavi, ilaç etkileşimlerine yol açabilir. Ağırlıklı olarak bu izoenzim tarafından metabolize edilen ve sınırlı bir terapötik indekse sahip (flekainid, enkainid, karbamazepin ve trisiklik antidepresanlar gibi) ilaçlarla eşzamanlı tedavi, en düşük etkili dozdan başlatılmalı veya uyarlanmalıdır. Son 5 hafta içinde fluoksetin alınmış olsa bile bunun yapılması gerekecektir.
Oral antikoagülanlarHomojen bir kategoriye girmeyen, ancak artan kanamayı içeren değişen antikoagülan etkiler (laboratuvar verileri ve/veya klinik semptom ve bulgular), fluoksetin ve oral antikoagülanların birlikte uygulanmasından sonra seyrek olarak gözlenmiştir. Varfarin alan hastalarda fluoksetin tedavisi başlatıldığında veya sonlandırıldığında, dikkatli pıhtılaşma takibi yapılmalıdır (bkz. bölüm 4.4 "Özel kullanım uyarıları ve önlemleri", kanama).
Elektrokonvülsif tedavi (ECT): EKT tedavisi alan fluoksetin ile tedavi edilen hastalarda uzamış nöbetlere ilişkin seyrek raporlar olmuştur, bu nedenle dikkatli olunması önerilir.
Alkol: Rutin testlerde fluoksetin kandaki alkol seviyelerinde artışa neden olmaz veya alkolün etkilerini potansiyalize etmez, ancak SSRI ve alkol tedavisinin kombinasyonu önerilmez.
Sarı Kantaron: Fluoksetin ile sarı kantaron içeren bitkisel preparat arasında farmakodinamik etkileşimler meydana gelebilir (Hypericum perforatum)serotonerjik etkilerde artışa ve istenmeyen etkilerde artışa neden olabilir.
04.6 Hamilelik ve emzirme
Gebelik:
Hamile ve emzikli kadınlarda Azur tedavisi doktor ve kullanılan ilaç tarafından ancak beklenen yararlar fetüs üzerindeki potansiyel riski haklı çıkarıyorsa dikkatle değerlendirilmelidir.
Epidemiyolojik veriler, hamileliğin ilk üç ayında fluoksetin kullanımıyla ilişkili kardiyovasküler kusur riskinde artış olduğunu bildirmektedir. Mekanizma bilinmemektedir. Genel olarak veriler, annenin fluoksetine maruz kalmasının ardından kardiyovasküler kusurlu bir çocuğa sahip olma riskinin arttığını göstermektedir. genel popülasyonda aynı kusurların yaklaşık %1'lik bir beklenen oranı ile karşılaştırıldığında %2 mertebesi.
Epidemiyolojik veriler, gebelikte, özellikle geç gebelikte SSRI kullanımının yenidoğanda kalıcı pulmoner hipertansiyon (PPHN) riskini artırabileceğini göstermektedir.Gözlenen risk yaklaşık 1000 gebelikte 5'tir.Genel popülasyonda, 1- Her 1000 hamile kadında yenidoğanda 2 kalıcı pulmoner hipertansiyon vakası.
Ek olarak, fluoksetin hamilelik sırasında kullanılabilse de, özellikle hamileliğin sonlarında veya doğumun başlangıcından hemen önce, yenidoğanlarda aşağıdaki etkiler rapor edildiğinden dikkatli olunmalıdır: sinirlilik, titreme, hipotoni, sürekli ağlama, emme güçlüğü veya Bu semptomlar hem serotonerjik etkileri hem de yoksunluk sendromunu gösterebilir Bu semptomların başlama zamanı ve süresi, fluoksetinin (4-6 gün) ve aktif metaboliti norfluoksetinin (4-16 gün) uzun yarılanma ömrü ile ilişkili olabilir. günler).
Besleme zamanı: Fluoksetin ve aktif metaboliti norfluoksetinin anne sütüne geçtiği bilinmektedir. Anne sütü ile beslenen bebeklerde advers olaylar bildirilmiştir. Fluoksetin tedavisi gerekli görülürse emzirmenin kesilmesi düşünülmeli, ancak emzirmeye devam edilirse etkili en düşük fluoksetin dozu reçete edilmelidir.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
Fluoksetinin sağlıklı gönüllülerde psikomotor performansı etkilemediği gösterilmiş olsa da, herhangi bir psikoaktif ilaç muhakeme veya mesleki becerileri bozabilir. Hastalara araç veya tehlikeli makine kullanmamaları tavsiye edilmelidir.
04.8 İstenmeyen etkiler
İstenmeyen etkilerin yoğunluğu ve sıklığı tedavinin devam etmesiyle azalabilir ve genellikle tedavinin kesilmesine yol açmaz.
Diğer SSRI'larda olduğu gibi, aşağıdaki yan etkiler gözlenmiştir:
Bir bütün olarak vücut: Aşırı duyarlılık belirtileri (örn. kaşıntı, döküntü, ürtiker, anafilaktoid reaksiyon, vaskülit, serum hastalığı benzeri reaksiyon, anjiyoödem) (bkz. bölüm 4.3 "Kontrendikasyonlar" ve bölüm 4.4 "Kullanım için özel uyarılar ve önlemler"), titreme, serotonin sendromu, ışığa duyarlılık ve çok nadiren Stevens-Johnson sendromunun veya toksik epidermal nekrolizin (Lyell sendromu) başlangıcına kadar ilerleyebilen eritema multiforme.
Sindirim sistemi: Gastrointestinal rahatsızlıklar (örn. ishal, bulantı, kusma, dispepsi, disfaji, tat değişikliği), ağız kuruluğu. Anormal karaciğer fonksiyon testleri nadiren bildirilmiştir. Çok nadir idiyosenkratik hepatit vakaları.
Gergin sistem: Baş ağrısı, uyku bozuklukları (örn. anormal rüyalar, uykusuzluk, somnolans), baş dönmesi, anoreksi, yorgunluk, somnolans (örn. uyuşukluk), öfori, geçici anormal hareketler (örn. (bkz. bölüm 4.4 "Özel kullanım uyarıları ve önlemleri"). Çok nadiren serotonin sendromu.
Kardiyovasküler sistem: Angina pektoris, aritmiler, 1. derece atriyoventriküler blok, hipotansiyon, hipertansiyon.
Psikolojik bozukluklar: Halüsinasyonlar, manik reaksiyon, konfüzyon, ajitasyon, anksiyete ve ilişkili semptomlar (örn. sinirlilik), bozulmuş konsantrasyon ve bilişsel süreç (örn. duyarsızlaşma), panik ataklar, intihar davranışı ve düşünceleri (bu belirtiler altta yatan bir hastalığa bağlı olabilir).
Fluoksetin tedavisi sırasında veya tedavinin kesilmesinden hemen sonra intihar düşüncesi ve intihar davranışı vakaları bildirilmiştir (bkz. bölüm 4.4).
Ürogenital sistem: İdrar retansiyonu ve değişen idrar sıklığı.
Üreme sistemi bozuklukları: cinsel işlev bozukluğu (gecikmiş veya yok boşalma, anorgazmi), priapizm, galaktore, hiperprolaktinemi.
Çeşitli: Alopesi, esneme, görme anormallikleri (örn. bulanık görme, midriyazis), terleme, vazodilatasyon, artralji, miyalji, postural hipotansiyon, ekimoz, hipoglisemi, hipokalemi. Nadiren diğer hemorajik belirtiler (örn. jinekolojik kanamalar, gastrointestinal kanama ve diğer kutanöz veya mukozal kanamalar) bildirilmiştir (bkz. bölüm 4.4 "Özel kullanım uyarıları ve önlemleri", kanama).
hiponatremiHiponatremi (110 mmol / l'nin altındaki sodyum değerleri dahil) nadiren bildirilmiştir ve fluoksetinin kesilmesiyle geri dönüşlüdür.Bazı vakalar muhtemelen uygunsuz antidiüretik hormon salgılanması sendromuna bağlıydı.Raporların çoğu yaşlı hastalarda ve diüretiklerle tedavi edilen veya başka herhangi bir nedenle kan hacmi azalmış hastalarda bulunmuştur.
Solunum sistemi: Farenjit, dispne. Nadiren pulmoner olaylar (değişken histopatoloji ve/veya fibrozun inflamatuar süreçleri dahil) bildirilmiştir. Dispne tek uyarı semptomu olabilir.
Kemik kırıkları: Esas olarak 50 yaş ve üzerindeki hastalarda yürütülen epidemiyolojik çalışmalar, SSRI'lar ve trisiklik antidepresanlar (TCA'lar) ile tedavi edilen hastalarda artmış kemik kırığı riskini göstermektedir. Bu riske neden olan mekanizma bilinmemektedir.
Fluoksetin tedavisinin kesilmesiyle gözlenen yoksunluk belirtileri: Fluoksetin tedavisinin kesilmesi genellikle yoksunluk semptomlarına yol açar En sık bildirilen reaksiyonlar baş dönmesi, duyu bozuklukları (parestezi dahil), uyku bozuklukları (uykusuzluk ve yoğun rüyalar dahil), asteni, ajitasyon veya anksiyete, bulantı ve/veya kusma, titreme ve Baş ağrısı Genellikle bu semptomlar hafif ila orta şiddettedir ve kendi kendini sınırlar, ancak bazı hastalarda şiddetli ve/veya uzun süreli olabilir (bkz. bölüm 4.4 "Özel kullanım uyarıları ve önlemleri"). bu nedenle, Azur ile tedavi artık gerekli olmadığında azaltma önerilir (bkz. bölüm 4.2 "Pozoloji ve uygulama yöntemi" ve bölüm 4.4 "Kullanım için özel uyarılar ve önlemler").
Çocuklar ve ergenler (bkz. bölüm 4.4):
Pediyatrik klinik çalışmalarda, intiharla ilgili davranışlar (intihar girişimi ve intihar düşünceleri) ve düşmanca tutum, antidepresanlarla tedavi edilen çocuk ve ergenlerde plasebo ile tedavi edilenlere göre daha sık gözlenmiştir.
Fluoksetinin güvenliği, 19 haftadan uzun süren kronik tedaviler için sistematik olarak değerlendirilmemiştir.
Pediyatrik klinik çalışmalarda, mani ve hipomani (fluoksetin ile tedavi edilen hastalarda %2,6 ve plasebo kontrollü hastalarda %0) dahil olmak üzere manik reaksiyonlar rapor edilmiş ve çoğu vakada tedavinin kesilmesine neden olmuştur. Bu hastalarda daha önce hipomani / mani atağı yoktu.
19 haftalık tedaviden sonra, bir klinik çalışmada fluoksetin ile tedavi edilen pediyatrik hastalar, plasebo ile tedavi edilen deneklere kıyasla ortalama 1,1 cm daha kısa (p = 0,004) ve ağırlık olarak 1,1 kg daha az (p = 0,008) bildirmiştir. Klinik kullanımda izole büyüme geriliği vakaları da bildirilmiştir.
Pediyatrik klinik kullanımda potansiyel olarak gecikmiş cinsel olgunlaşmayı veya cinsel işlev bozukluğunu gösteren izole advers olay vakaları bildirilmiştir (ayrıca bkz. bölüm 5.3).
Pediyatrik klinik çalışmalarda, fluoksetin tedavisi, kandaki alkalin fosfataz seviyelerinde bir azalma ile ilişkilendirilmiştir.
04.9 Doz aşımı
Tek başına fluoksetine bağlı doz aşımı vakaları genellikle hafif seyreder. Doz aşımı semptomları mide bulantısı, kusma, nöbetler, asemptomatik aritmiden kardiyak arreste kadar değişen kardiyovasküler disfonksiyon, pulmoner disfonksiyon ve heyecandan komaya kadar değişen bir CNS durumunun değişmiş belirtilerini içerir. kardiyak fonksiyon ve yaşamsal belirtilerin yanı sıra genel semptomatik ve destekleyici önlemleri izlemek için Spesifik bir antidot bilinmemektedir.
Zorla diürez, diyaliz, hemoperfüzyon ve replasman transfüzyonunun fayda sağlaması olası değildir.Sorbitol ile birlikte kullanılabilen aktif kömür, kusma veya gastrik lavajdan bile daha etkili bir tedavi olabilir. Bir doz aşımını tedavi ederken, çoklu ilaç tutulum olasılığını göz önünde bulundurun. Aşırı miktarda trisiklik antidepresan alan hastalarda, fluoksetin de alıyorlarsa veya yakın zamanda almışlarsa, yakın tıbbi gözlem için daha uzun bir süre gerekebilir.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
ATC kodu: N06AB03
Fluoksetin (INN), seçici bir serotonin geri alım inhibitörüdür.
Fluoksetin, bir (±) -N-metil-3-fenil-3 - [(a, a, a, -trifloro-p-tolil) -oksi] -propilamin hidroklorür olup, antidepresan etkisi muhtemelen bağlantılı olan trisiklik olmayan bir yapıya sahiptir. merkezi nöronlarda serotonin alımının inhibisyonu İnsan trombosit çalışmalarında, fluoksetinin trombositlere serotonin alımını bloke ettiği gösterilmiştir.
Hayvan çalışmaları ayrıca fluoksetinin serotonin alımı üzerinde diğer monoaminlerin alımı üzerinde uygulanandan çok daha güçlü bir inhibitör etki uyguladığını göstermektedir.
Klasik trisiklik antidepresanların çeşitli antikolinerjik ve kardiyovasküler etkilerinden "muskarinik, histamin ve alfa1-adrenerjik reseptörler üzerindeki antagonistik bir etkinin sorumlu olduğu varsayılmıştır. Fluoksetin bunlara ve diğer membran reseptörlerine trisiklik ilaçlardan çok daha az bağlanır.
05.2 Farmakokinetik özellikler
Oral uygulamadan sonra emilim hızlı ve tamdır İnsanlarda, 40 mg'lık tek bir dozdan sonra, 6-8 saat sonra 15 ila 55 ng/ml arasında değişen fluoksetinin plazma zirveleri gözlenir.
Fluoksetinin kapsüller, çözünür tabletler ve oral kullanım için çözelti içindeki preparatları biyoeşdeğerdir.
Fluoksetin, emilimi biraz yavaşlatabilmesine rağmen, gıda sistemik biyoyararlanımı değiştirmediğinden yemekle birlikte veya yemeksiz uygulanabilir.
Fluoksetin karaciğerde ağırlıklı olarak norfluoksetin ve daha sonra böbrek tarafından atılan diğer inaktif metabolitlere metabolize edilir.
Fluoksetin vücutta yaygın olarak dağılır ve plazma proteinlerine geniş ölçüde bağlanır.
Fluoksetinin eliminasyon yarı ömrü 4-6 gündür, aktif metabolitininki ise 4-16 gündür (P450IID6 enzim sistemi eksikliği olan hastalarda bu değerler daha da uzayabilir). Bunlardan kronik kullanımda aktif ürünler. Denge plazma konsantrasyonlarına ancak haftalarca tedaviden sonra ulaşılır.
Aşağıdaki tablo en belirgin farmakokinetik özellikleri özetlemektedir.
* P450IID6 enzim sistemi eksikliği olan hastalarda bu değerler daha da uzayabilir.
Karaciğer yetmezliğinin varlığı fluoksetinin eliminasyonunu engelleyebilir.
Şiddetli böbrek yetmezliği olan hastalarda fluoksetin veya metabolitlerinin daha fazla birikmesi meydana gelebilir.
05.3 Klinik öncesi güvenlik verileri
Hem fluoksetin hem de aktif metaboliti norfluoksetin, primatlar dahil çeşitli hayvan türlerinde tek ve tekrarlanan doz, subakut ve kronik toksisite testlerinde yüksek derecede tolere edilebilirlik göstermiştir.
Akut uygulama için LD50 (mg / kg):
Toksik fenomenlere neden olan akut dozlar, insanlardaki terapötik dozlardan (0.3-1.0 mg/kg/gün) birkaç kat fazladır.Kronik toksisite testlerinde bulunan herhangi bir toksik etki (anoreksiya, kilo kaybı, bazı hayvan türlerinde fosfolipidoz) tespit edilmiştir. tedavinin kesilmesiyle geri dönüşümlü olduğu gösterilmiştir.
Üreme Çalışmaları: Fluoksetin, test edilen dozlarda doğurganlığı ve üreme kapasitesini etkilemez.
Teratojenik çalışmalar: Fluoksetin, doğum öncesi gelişimi veya fetal ağırlığı olumsuz etkilemez ve önemli teratojenik etkiler kaydedilmemiştir.
Mutajenite Çalışmaları: Fluoksetin ve norfluoksetin, hem in vitro hem de in vivo mutajenik etkilerden aridir.
Kanserojenlik Çalışmaları: 2 yıllık bir süre boyunca insanlarda önerilen günlük dozun yaklaşık on katı ortalama dozlarda, sıçanlarda ve farelerde hiçbir kanserojen etki gözlenmemiştir.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
Mısır nişastası, Dimetikon, Jelatin, Titanyum dioksit.
06.2 Uyumsuzluk
Rapor etme.
06.3 Geçerlilik süresi
2 yıl.
06.4 Depolama için özel önlemler
30°C'nin altında saklayınız.
06.5 İç ambalajın yapısı ve paketin içeriği
1 adet kullanma talimatı içeren 28 kapsüllük litografili karton kutu.
06.6 Kullanım ve kullanım talimatları
Özel talimat yok
07.0 PAZARLAMA YETKİ SAHİBİ
BIORES ITALIA S.r.l. "Via Vittorio Grassi n. 13." 00155 Roma
08.0 PAZARLAMA YETKİ NUMARASI
AZUR 20 mg kapsül. "28 kapsül A.I.C. n.: 034375030
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
22.11.2000
10.0 METİN REVİZYON TARİHİ
Mayıs 2011