Aktif maddeler: Flutikazon (flutikazon propiyonat)
FLIXOTIDE 100 mcg İnhalasyon için toz
FLIXOTIDE 250 mcg İnhalasyon için toz
FLIXOTIDE 500 mcg İnhalasyon için toz
Paket boyutları için Flixotide prospektüsleri mevcuttur: - FLIXOTIDE 100 mcg İnhalasyon tozu, FLIXOTIDE 250 mcg İnhalasyon tozu, FLIXOTIDE 500 mcg İnhalasyon tozu
- FLIXOTIDE 500 mcg / 2 ml Nebulize edilecek süspansiyon
- FLIXOTIDE 50 mcg Basınçlı inhalasyon süspansiyonu, FLIXOTIDE 125 mcg Basınçlı inhalasyon süspansiyonu, FLIXOTIDE 250 mcg Basınçlı inhalasyon süspansiyonu
Flixotide neden kullanılır? Bu ne için?
FARMAKOTERAPÖTİK KATEGORİ
Aerosoller tarafından obstrüktif solunum yolu sendromları için diğer ilaçlar - Glikokortikoidler.
TEDAVİ ENDİKASYONLARI
Astımlı hastalık ve bronkostenoz koşullarının gelişiminin kontrolü.
Kontrendikasyonlar Flixotide ne zaman kullanılmamalıdır?
Etkin maddeye veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılık (bkz. "Bileşim").
Genellikle hamilelik ve emzirme döneminde kontrendikedir (bkz. "Özel uyarılar").
Kullanım Önlemleri Flixotide kullanmadan önce bilmeniz gerekenler
Astım tedavisi, normal olarak, hastalığın şiddetine göre uyarlanmış bir terapötik plan çerçevesinde gerçekleştirilmelidir; Hastanın tedaviye yanıtı hem klinik olarak hem de varsa solunum fonksiyon testleri ile doğrulanmalıdır.
Hızlı etkili inhale beta2-agonistlerin daha sık kullanılması ihtiyacı astım kontrolünün kötüleştiğini gösterir; bu durumda hastanın tedavi planı değiştirilmelidir.
Astımın ani ve ilerleyici alevlenmesi potansiyel olarak yaşamı tehdit eder ve kortikosteroid dozunun artırılmasına dikkat edilmelidir. Risk altında olduğu düşünülen hastalarda günlük pik akım takibi önerilir.
Özellikle uzun süreler için yüksek dozlarda reçete edildiğinde, inhale kortikosteroidlerle sistemik etkiler ortaya çıkabilir. Bu etkilerin ortaya çıkması, oral kortikosteroid tedavisine göre daha az olasıdır. Olası sistemik etkiler arasında Cushing sendromu, Cushingoid görünüm, adrenal baskılanma, çocuklarda ve ergenlerde büyüme geriliği, azalmış kemik mineral yoğunluğu, katarakt ve glokom bulunur ve nadiren psikomotor hiperaktivite dahil bir dizi psikolojik ve davranışsal etkiler görülebilir. , sinirlilik, uyku bozuklukları , kaygı, depresyon, saldırganlık, davranış bozuklukları (ağırlıklı olarak çocuklarda). Dozu kullanma talimatında belirtildiği şekilde veya doktorunuzun önerdiği şekilde almanız önemlidir. İlk önce doktorunuza danışmadan dozu artırmamalı veya azaltmamalısınız. Uzun süreler boyunca önerilenden daha yüksek dozlara (basınçlı süspansiyon ile inhalasyon yoluyla veya eşdeğer dozlarda diğer inhale kortikosteroidler veya diğer flutikazon propiyonat formları ile uygulandığında yaklaşık 1000 mikrogram/gün) maruz kalan erkek çocuklarda çok seyrek olarak akut adrenal kriz vakaları olmuştur. (birkaç ay veya yıl).
Uzun süreli inhale kortikosteroid tedavisi alan çocukların boylarının düzenli olarak izlenmesi önerilir.
Yetersiz adrenal yanıt olasılığı nedeniyle, daha önce oral steroidlerle tedavi edilen ve inhale flutikazon propiyonat tedavisine geçen hastalar özel bir dikkatle tedavi edilmeli ve adrenal fonksiyon düzenli olarak izlenmeli, sistemik steroid tedavisinin kesilmesi kademeli olmalı ve hastalara stres zamanlarında ek kortikosteroid tedavisi gerektirebileceklerini gösteren bir belirteç.
Acil durumlarda (cerrahi müdahaleler dahil) ve ayrıca strese neden olabilecek elektif müdahalelerde yetersiz adrenal yanıt olasılığı, özellikle uzun süre yüksek doz alan hastalarda her zaman akılda tutulmalıdır. Klinik duruma uygun ek kortikosteroid tedavisi düşünülmelidir (bkz. "Aşırı doz").
Sistemik kortikosteroid tedavisinin inhalasyon tedavisi ile değiştirilmesi, daha önce sistemik ilaçlar tarafından maskelenen alerjik rinit veya egzama gibi alerjileri ortaya çıkarabilir.
Flutikazon propiyonat ile tedavi aniden kesilmemelidir.
Kan glukoz seviyelerinde çok nadir artış raporları olmuştur (bkz. "İstenmeyen Etkiler") ve bu durum, diyabetes mellitus öyküsü olan hastalara ilaç reçete edilirken dikkate alınmalıdır.
Tüm inhale kortikosteroidlerde olduğu gibi, akciğer tüberkülozunun aktif veya uyku halindeki formları olan hastalarda özel bakım gereklidir.
Flutikazon propiyonat ve ritonavir ile tedavi edilen hastalarda, Cushing sendromu ve adrenal süpresyon dahil olmak üzere sistemik kortikosteroid etkilere neden olan, pazarlama sonrası kullanım sırasında klinik olarak anlamlı ilaç etkileşimleri vakaları bildirilmiştir. hastaya yararı, sistemik kortikosteroid yan etkilerinin ortaya çıkma risklerinden daha ağır basarsa (bkz. "Etkileşimler").
İnhalasyon yoluyla uygulanan diğer ilaçlarda olduğu gibi, ilacı aldıktan hemen sonra artan hışıltı ile paradoksal bronkospazm olasılığı göz önünde bulundurulmalıdır.Bu durumda hemen hızlı etkili bir bronkodilatör alınız. gerekirse tedavi edin (bkz. "İstenmeyen Etkiler").
500 mikrogram flutikazon propiyonat alan kronik obstrüktif akciğer hastalığı (KOAH) hastalarında yapılan çalışmalarda pnömoni raporlarında artış olmuştur (bkz. klinikler genellikle örtüşür
Etkileşimler Hangi ilaçlar veya yiyecekler Flixotide'in etkisini değiştirebilir?
Yakın zamanda başka ilaçlar aldıysanız, hatta reçetesiz bile olsa, doktorunuza veya eczacınıza söyleyiniz.
Normal koşullar altında, geniş ilk geçiş metabolizması ve bağırsakta ve karaciğerde sitokrom P450 3A4'ün aracılık ettiği yüksek sistemik klirens nedeniyle inhale uygulamadan sonra flutikazon propiyonatın düşük plazma konsantrasyonları elde edilir.Bu nedenle etkileşimler olası değildir.flutikazon propiyonatın aracılık ettiği klinik olarak anlamlı ilaç.
Sağlıklı gönüllülerde yürütülen bir etkileşim çalışması, ritonavirin (çok güçlü bir sitokrom P450 3A4 inhibitörü) flutikazon propiyonatın plazma konsantrasyonlarını önemli ölçüde artırabildiğini ve bunun sonucunda serum kortizol konsantrasyonlarının önemli ölçüde azalmasına neden olduğunu göstermiştir.
Pazarlama sonrası kullanım sırasında, intranazal veya inhale flutikazon propiyonat ve ritonavir ile tedavi edilen hastalarda, Cushing sendromu ve adrenal süpresyon dahil olmak üzere sistemik kortikosteroid etkilere neden olan klinik olarak anlamlı ilaç etkileşimleri vakaları bildirilmiştir.
Bu nedenle, hastaya sağlayacağı potansiyel yarar sistemik kortikosteroid yan etkilerinin risklerinden daha fazla olmadıkça flutikazon propiyonat ve ritonavirin birlikte kullanımından kaçınılmalıdır.
Çalışmalar, diğer sitokrom P450 3A4 inhibitörlerinin, flutikazon propiyonata sistemik maruziyette ihmal edilebilir (eritromisin) ve küçük (ketokonazol) artışlar ürettiğini ve serum kortizol konsantrasyonlarında kayda değer bir azalma olmadığını göstermiştir.Ancak, güçlü sitokrom P450 3A4 inhibitörleri (örn. ketokonazol) olduğunda dikkatli olunması önerilir. ) flutikazon propiyonata artan sistemik maruziyet potansiyeli bulunduğundan eşzamanlı olarak uygulanır.
Yakın zamanda başka ilaçlar aldıysanız, hatta reçetesiz bile olsa, doktorunuza veya eczacınıza söyleyiniz.
Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme
Herhangi bir ilaç almadan önce doktorunuza veya eczacınıza danışınız.
Gebe kadınlarda flutikazon propiyonat ile ilgili yeterli ve kontrollü çalışma bulunmamaktadır. Flutikazon propiyonatın kadınlarda gebelik üzerindeki etkisi bilinmemektedir.Flutikazon propiyonatın gebelikte tolere edilebilirliği ile ilgili bilgiler halen sınırlıdır.
Flutikazon propiyonatın üreme işlevi üzerindeki herhangi bir etkileşimini değerlendirmek için yapılan hayvan çalışmaları, önerilen terapötik inhale dozda gözlenenden çok daha fazla sistemik maruziyet seviyelerinde sadece glukokortikoidlerin karakteristik etkilerini göstermiştir.
Genotoksisite testleri, molekülün mutajenik potansiyelini göstermedi
Bununla birlikte, diğer ilaçlarda olduğu gibi, hamilelik sırasında flutikazon propiyonat uygulaması, yalnızca anneye beklenen yararın fetüse yönelik olası risklerden daha ağır basması durumunda düşünülmelidir.
Flutikazon propiyonatın anne sütüne geçip geçmediği bilinmemektedir. Sıçanlarda subkutan uygulamayı takiben, anne sütünde ölçülebilir plazma konsantrasyonlarında flutikazon propiyonat varlığı bulundu. Bununla birlikte, önerilen inhale dozlarda flutikazon propiyonat alan hastalarda plazma düzeylerinin düşük olması muhtemeldir.
Araç ve makine kullanma yeteneği üzerindeki etkiler
Flutikazon propiyonatın araç ve makine kullanma yeteneğini etkilemesi olası değildir.
Bazı bileşenler hakkında önemli bilgiler
FLIXOTIDE DISKUS laktoz içerir. Eğer daha önceden doktorunuz tarafından bazı şekerlere karşı intoleransınız olduğu söylenmişse, bu ilacı almadan önce doktorunuzla temasa geçiniz.
Dozaj ve kullanım yöntemi Flixotide nasıl kullanılır: Pozoloji
Flutikazon propiyonat sadece oral inhalasyon yoluyla uygulanmalıdır.
Her dozun içeriği, basınçlı bir aerosolü doğru kullanamayan hastalarda bile ilacın solunmasını sağlayan özel multidoz inhaler (DISKUS) tarafından doğrudan solunur.
Flutikazon propiyonat ile inhalasyon tedavisi koruyucu olduğundan, belirgin semptomlar olmasa bile ilaç uygulamasına başlanmalı ve semptomlar düzeldikten sonra bile devam edilmelidir.
Hastalar, ilacın etkinliğinin hemen olmadığı ve bu nedenle düzenli olarak alınması gerektiği konusunda bilgilendirilmelidir; terapötik etkinin başlangıcı 4 ila 7 gün arasındadır, ancak bazı durumlarda hastalarda ilk 24 saat içinde bir iyileşme meydana gelebilir. Daha önce inhale steroidlerle tedavi edilmemiş.
Flutikazon propiyonat dozu, astımın şiddeti ve tedavi aşamasına göre hastaya göre ayarlanmalıdır.
Hastanın solunum fonksiyonu stabilize olduğunda, minimum etkili idame dozuna ulaşılana kadar günlük doz bireysel cevaba göre kademeli olarak azaltılmalıdır.
Hasta, hızlı etkili beta2-agonistlerin etkinliğinde bir azalma veya kullanım sıklığının daha yüksek olduğunu fark ederse, tıbbi yardım istenmelidir.
Flutikazon propiyonat ile tedavi aniden kesilmemelidir.
Yaşlı hastalarda veya karaciğer veya böbrek yetmezliği olan hastalarda ilaç dozunun azaltılmasına gerek yoktur.
yetişkinler
Standart doz, her biri 100 mikrogramlık iki doza bölünmüş, günde 200 mikrogramdır.
Dozaj günde 400 mikrograma kadar arttırılabilir.
Başlangıç dozu daha sonra kontrol sağlanana kadar ayarlanabilir veya bireysel cevaba göre en düşük etkili doza düşürülebilir.
Reçete yazan hekim, flutikazon propiyonatın günlük yaklaşık yarım mikrogram dozunda diğer inhale steroidler kadar etkili olduğunu bilmelidir. Örneğin, 100 mikrogram flutikazon propiyonat, yaklaşık olarak 200 mikrogram beklometazon dipropionat veya budesonid dozuna eşdeğerdir.
Flutikazon propiyonatın etkinlik ve tolere edilebilirlik profili, sıklıkla oral steroidlerle tedaviye başvurmak zorunda kalan şiddetli formları olan hastaların bile bu inhale steroid ile tedavi edilmesine olanak tanır.
Bu hastalarda, günde maksimum 2000 mikrogram flutikazon propiyonat dozu, oral steroid kullanımını önemli ölçüde azaltarak yeterli hastalık kontrolüne izin verebilir Alevlenmeler sırasında, flutikazon propiyonatın günlük 2000 mikrogram dozları bazı durumlarda oral steroid sikluslarının yerini alabilir. .
4 yaşından büyük çocuklar
Standart doz, her biri 50 mikrogramlık iki doza bölünmüş, günde 100 mikrogramdır.
Dozaj günde 200 mikrograma kadar arttırılabilir.
Astımı yeterince kontrol altına alınamayan hastalar için doz günde iki kez 200 mikrograma kadar artırılarak ek bir fayda sağlanabilir.
Tedavi, hastalığın şiddetine uygun bir dozda başlatılmalıdır.
Doz daha sonra kontrol sağlanana kadar ayarlanabilir veya bireysel cevaba göre en düşük etkili doza düşürülebilir.
1 ila 4 yaş arası çocuklar
İnhalasyon tozu farmasötik formu 1 ila 4 yaş arası çocuklar için uygun değildir; Bu yaş grubundaki ilacın dozu ile ilgili olarak, FLIXOTIDE Basınçlı inhalasyon süspansiyonu bilgilerine bakınız.
Çocuklarda izin verilen maksimum doz günde iki kez 200 mikrogramdır.
Kullanım ve kullanım talimatları
FLIXOTIDE, her biri bir doz (100 - 250 - 500 mikrogram) toz içeren, düzenli aralıklarla ayrı ayrı alveollerin ("kabarcık") düzenlendiği bir şerit şerit içeren, kalıplanmış plastik malzemeden DISKUS inhalatörleri aracılığıyla solunmalıdır. laktoz içinde dağılmış flutikazon propiyonatın solunması.
FLIXOTIDE - DISKUS inhaler içinde inhalasyon tozu
DİSK BİLGİLERİ
DISKUS, kutudan çıkarıldığında "kapalı" konumdadır.
DISKUS, bireysel olarak korunan 60 doz ilaç tozu içerir.
Her doz dikkatle ölçülür ve hijyenik olarak korunur. DISKUS bakım gerektirmez ve şarj edilemez.
DISKUS'un üst kısmındaki doz göstergesi, halen mevcut olan dozların sayısını gösterir.
5'ten 0'a kadar olan sayılar, yalnızca birkaç doz kaldığını belirtmek için KIRMIZI renktedir.
DISKUS'un kullanımı kolaydır.
İlacın bir dozunu almak için aşağıdaki dört basit adımı izleyin:
1. Açılış
2. Dozun hazırlanması
3. Soluma
4. Kapanış
DİSK NASIL ÇALIŞIR
DİSKUS'un kolu kaydırılarak ağızlıkta küçük bir delik açılır ve inhalasyona hazır bir doz hazırlanır. DISKUS kapatıldığında, kol otomatik olarak orijinal konumuna döner ve bir sonraki ilaç dozunu hazırlamaya hazırdır.
Dış kapak kullanılmadığında DISKUS'u korur.
1. Açılış
DISKUS'u açmak için bir elinizle dış kısmından tutun ve diğer elin başparmağını girintiye yerleştirin. Bir klik sesi duyana kadar cihazın içini döndürürken baş parmağınızla itin.
2. Dozun hazırlanması
DISKUS'u ağızlık kullanıcıya bakacak şekilde tutun.Kolu tık sesi gelene kadar ileri kaydırın.DISKUS artık kullanıma hazırdır.
Kol her kaydırıldığında, doz göstergesinde gösterildiği gibi inhalasyon için bir doz hazır hale gelir.
Kolu, dozları boşa harcamamak için yalnızca ilacı solumanız gerektiğinde kullanın.
3. Soluma
Teneffüs etmeden önce bu bölümü dikkatlice okuyun.
DISKUS'u ağzınızdan uzak tutun. Mümkün olduğunca derin nefes verin. DISKUS'a asla üflemeyin.
Ağızlığı dudaklarınızın arasına koyun.
Burundan değil, DISKUS'tan derin ve düzenli bir şekilde nefes alın.
DISKUS'u ağzınızdan çıkarın.
Nefesinizi yaklaşık 10 saniye veya mümkün olduğunca uzun süre tutun.
Yavaşça nefes verin.
4. Kapanış
DISKUS'u kapatmak için başparmağınızı girintiye yerleştirin ve gidebildiği kadar geriye doğru kaydırın.
DISKUS kapatıldığında keskin bir kapanma sesi çıkarır. Bu, kolu otomatik olarak orijinal konumuna döndürür.
DISKUS artık tekrar kullanılmaya hazırdır.
İki inhalasyon reçete edilmişse, ilk inhalasyondan sonra DISKUS'u kapatmak ve ardından 1 ila 4 arasındaki adımları tekrarlamak gerekir.
DİKKAT: DISKUS'u kuru tutun
Kullanılmadığı zaman DISKUS'u kapalı tutun
DISKUS'a asla üflemeyin
Kolu yalnızca ilacı almaya hazır olduğunuzda kaydırın
DISKUS'tan sadece ağzınızla nefes alın
Önerilen dozu aşmayınız
Doz aşımı: Çok fazla Flixotide aldıysanız ne yapmalısınız?
İlacın yanlışlıkla aşırı dozda alınması durumunda derhal doktorunuza haber veriniz veya en yakın hastaneye başvurunuz.
FLIXOTIDE'ın kullanımıyla ilgili herhangi bir sorunuz varsa, doktorunuza veya eczacınıza sorunuz.
İlacın önerilenden daha yüksek dozlarda akut inhalasyonu, hipotalamus-hipofiz-adrenal ekseninin geçici olarak baskılanmasına neden olabilir. Adrenal fonksiyon tipik olarak birkaç gün içinde normale döndüğünden, bu normalde acil müdahale kurumunu gerektirmez.
Onaylananlardan daha yüksek dozlar uzun süre kullanılırsa, önemli adrenal baskılanma meydana gelebilir. Adrenal rezervin izlenmesi gerekli olabilir. Uzun süreli (birkaç ay veya yıl) önerilenden daha yüksek dozlara (tipik olarak 1000 mikrogram/gün ve üzeri) maruz kalan çocuklarda çok seyrek olarak akut adrenal kriz vakaları olmuştur; gözlemlenen belirtiler arasında hipoglisemi ve azalmış bilinç ve/veya konvülsiyon sekelleri yer alır.
Akut adrenal krizi potansiyel olarak tetikleyebilecek durumlar arasında travmaya, ameliyata, enfeksiyona veya dozajda herhangi bir hızlı azalmaya maruz kalma yer alır.
Onaylanandan daha yüksek dozlarla tedavi edilen hastalar yakından izlenmeli ve doz kademeli olarak azaltılmalıdır.
Yan Etkiler Flixotide'in yan etkileri nelerdir?
Tüm ilaçlar gibi, FLIXOTIDE herkeste görülmese de yan etkilere neden olabilir.
İstenmeyen etkiler aşağıda organ, organ/sistem ve sıklık bazında listelenmiştir. Sıklıklar şu şekilde tanımlanmıştır: çok yaygın (≥1/10), yaygın (≥1/100 ila
Enfeksiyonlar ve istilalar
Çok yaygın: Ağız ve boğazda kandidiyazis
Bazı hastalarda orofaringeal kandidiyazis (pamukçuk) oluşabilir. Bu tür hastalar ilacı aldıktan sonra ağızlarını suyla çalkalamaktan fayda görebilirler Semptomatik kandidiyaz, flutikazon propiyonat kullanımını durdurmadan topikal antifungal tedavi ile tedavi edilebilir.
Yaygın: pnömoni (KOAH hastalarında)
Çok seyrek: Özofagus kandidiyazisi.
Bağışıklık sistemi bozuklukları
Aşağıdaki gibi ortaya çıkan aşırı duyarlılık reaksiyonları bildirilmiştir:
Yaygın olmayan: ciltte aşırı duyarlılık reaksiyonları
Çok seyrek: Anjiyoödem (esas olarak yüzde ve orofarenkste ödem), solunum semptomları (dispne ve/veya bronkospazm) ve anafilaktik reaksiyonlar.
endokrin patolojiler
Olası sistemik etkiler şunları içerir ("Kullanım Önlemleri" bölümüne bakın):
Çok seyrek: Cushing sendromu, Cushingoid görünüm, adrenal supresyon, büyüme geriliği, kemik mineral yoğunluğunda azalma, katarakt, glokom.
Metabolizma ve beslenme bozuklukları
Çok seyrek: hiperglisemi.
Psikolojik bozukluklar
Çok seyrek: Anksiyete, uyku bozuklukları ve psikomotor hiperaktivite ve irritabilite dahil davranış bozuklukları (ağırlıklı olarak çocuklarda).
Bilinmiyor: Depresyon ve saldırganlık (ağırlıklı olarak çocuklarda).
Solunum, göğüs ve mediastinal bozukluklar
Yaygın: ses kısıklığı Bazı hastalarda ses kısıklığı oluşabilir; bu durumlarda bile inhalasyondan hemen sonra ağzı suyla çalkalamak avantajlı olabilir.
Çok seyrek: paradoksal bronkospazm ("Kullanım Önlemleri" bölümüne bakınız).
Deri ve deri altı doku bozuklukları
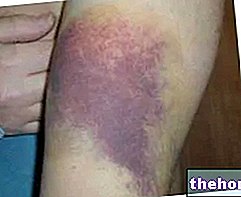
Yaygın: morluklar Kullanma talimatında yer alan talimatlara uyulması yan etki riskini azaltır.
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuzla veya eczacınızla konuşun.Bu kullanma talimatında listelenmeyen olası yan etkiler de buna dahildir. İstenmeyen etkiler, https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse adresindeki ulusal raporlama sistemi aracılığıyla da doğrudan rapor edilebilir.Yan etkileri bildirerek, bu ilacın güvenliği hakkında daha fazla bilgi sağlamaya yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Son kullanma tarihi: ambalajın üzerinde yazılı olan son kullanma tarihine bakın.
Son kullanma tarihi, ürünün bozulmamış ambalajında, doğru şekilde saklanmış olduğunu ifade eder.
Uyarı: Paket üzerinde belirtilen son kullanma tarihinden sonra ilacı kullanmayınız.
Koruma kuralları
Kuru bir yerde saklayın
İlacı nemden korumak için orijinal ambalajında saklayınız.
DISKUS, yalnızca tıbbi ürün ilk kez kullanıldığında açılması gereken koruyucu bir laminat örtü ile kapatılmıştır. Koruyucu laminat zarf açıldıktan sonra atılmalıdır.
İlaçlar atık su veya evsel atıklar yoluyla bertaraf edilmemelidir.Artık kullanmadığınız ilaçları nasıl bertaraf edeceğinizi eczacınıza sorunuz.Bu, çevrenin korunmasına yardımcı olacaktır.
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
KOMPOZİSYON
FLIXOTIDE 100 mcg
inhalasyon için toz
Bir porsiyon şunları içerir:
Aktif madde: flutikazon propiyonat 100 mcg
Yardımcı maddeler: laktoz (süt proteinleri içerir)
FLIXOTIDE 250 mcg İnhalasyon için toz
Bir porsiyon şunları içerir:
Aktif madde: flutikazon propiyonat 250 mcg
Yardımcı maddeler: laktoz (süt proteinleri içerir)
FLIXOTIDE 500 mcg İnhalasyon için toz
Bir porsiyon şunları içerir:
Aktif madde: flutikazon propiyonat 500 mcg
Yardımcı maddeler: laktoz (süt proteinleri içerir)
FARMASÖTİK FORM VE İÇERİĞİ
60 dozluk DISKUS inhaler içinde inhalasyon tozu.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
FLIXOTIDE
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
FLIXOTIDE 125 mcg - Solunum için basınçlı süspansiyon
120 nefeslik basınçlı bir kap şunları içerir:
Aktif madde: flutikazon propiyonat (hareket başına 125 mcg) 15.00 mg
FLIXOTIDE 250 mcg - Solunum için basınçlı süspansiyon
120 nefeslik basınçlı bir kap şunları içerir:
Aktif madde: flutikazon propiyonat (arz başına 250 mcg) 30,00 mg
FLIXOTIDE 50 mcg - Solunum için basınçlı süspansiyon
120 nefeslik basınçlı bir kap şunları içerir:
Aktif madde: flutikazon propiyonat (hareket başına 50 mcg) 6.00 mg
FLIXOTIDE 250 mcg - İnhalasyon tozu 60 doz şeritli DISKUS inhaler içinde
Bir porsiyon şunları içerir:
Aktif madde: flutikazon propiyonat 250 mcg
Yardımcı maddeler: laktoz
FLIXOTIDE 500 mcg - İnhalasyon tozu 60 doz şeritli DISKUS inhaler içinde
Bir porsiyon şunları içerir:
Aktif madde: flutikazon propiyonat 500 mcg
Yardımcı maddeler: laktoz
FLIXOTIDE 100 mcg - İnhalasyon tozu 60 doz şeritli DISKUS inhaler içinde
Bir porsiyon şunları içerir:
Aktif madde: flutikazon propiyonat 100 mcg
Yardımcı maddeler: laktoz
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakınız.
03.0 FARMASÖTİK FORM
Solunum için basınçlı süspansiyon. İnhalasyon için toz.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Astımlı hastalık ve bronkostenoz koşullarının gelişiminin kontrolü.
04.2 Pozoloji ve uygulama yöntemi
Flutikazon propiyonat sadece oral inhalasyon yoluyla uygulanmalıdır.
Hastalara, inhale flutikazon propiyonat tedavisinin profilaktik doğası ve semptomlar düzeldikten sonra bile düzenli olarak kullanılması gerektiği konusunda bilgi verilmelidir.
Hastalar, ilacın etkinliğinin hemen olmadığı ve bu nedenle düzenli olarak alınması gerektiği konusunda bilgilendirilmelidir; terapötik etkinin başlangıcı 4 ila 7 gün arasındadır, ancak bazı durumlarda hastalarda ilk 24 saat içinde bir iyileşme meydana gelebilir. Daha önce inhale steroidlerle tedavi edilmemiş.
Hasta, hızlı etkili beta2-agonistlerin etkinliğinde bir azalma veya kullanım sıklığının daha yüksek olduğunu fark ederse, tıbbi yardım istenmelidir.
Flutikazon propiyonat dozu, hastalığın şiddetine göre hastaya göre uyarlanmalıdır. astım ve tedavi aşaması.
Hastanın solunum fonksiyonu stabilize olduğunda, minimum etkili idame dozuna ulaşılana kadar günlük doz bireysel cevaba göre kademeli olarak azaltılmalıdır.
Flutikazon propiyonat ile tedavi aniden kesilmemelidir.
Yaşlı hastalarda veya karaciğer veya böbrek yetmezliği olan hastalarda ilaç dozunun azaltılmasına gerek yoktur.
FLIXOTIDE - Solunum için basınçlı süspansiyon
Tüm ilaçlarda olduğu gibi, inhalasyon yoluyla, dozlanmış bir aerosol vasıtasıyla, dozun iki inhalasyon halinde alınması tavsiye edilir.
Hareket koordinasyonu zayıf olan hastalarda uygun spacer cihazları kullanılabilir.
FLIXOTIDE - Solunum için toz
Her dozun içeriği, basınçlı bir aerosolü doğru kullanamayan hastalarda bile ilacın solunmasını sağlayan özel multidoz inhaler (DISKUS) tarafından doğrudan solunur.
yetişkinler
Standart doz günde 200 mcg'dir ve her biri 100 mcg'lik iki doza bölünmüştür.
Dozaj günde 400 mcg'ye kadar arttırılabilir.
Başlangıç dozu daha sonra kontrol sağlanana kadar ayarlanabilir veya bireysel cevaba göre en düşük etkili doza düşürülebilir.
Reçete yazan hekim, flutikazon propiyonatın günlük yaklaşık yarım mcg dozunda diğer inhale steroidler kadar etkili olduğunu bilmelidir. Örneğin, 100 mcg flutikazon propiyonat, yaklaşık olarak 200 mcg beklometazon dipropionat (CFC içeren formülasyonlarda) veya budesonide eşdeğerdir.
Flutikazon propiyonatın etkinlik ve tolere edilebilirlik profili, sıklıkla oral steroid tedavisine başvurmak zorunda kalan şiddetli formları olan hastaların bile bu inhale steroid ile tedavi edilmesine olanak sağlar.Bu hastalarda flutikazon propiyonat günde maksimum 2000 mcg dozunda yeterli hastalık kontrolüne izin verebilir. oral steroidlerin kullanımını büyük ölçüde azaltarak.
Alevlenmeler sırasında, günde 2000 mcg flutikazon propiyonat dozları bazı durumlarda oral steroid kürlerinin yerini alabilir.
4 yaşından büyük çocuklar
Standart doz, her biri 50 mcg'lik iki doza bölünmüş, günde 100 mcg'dir.
Dozaj günde 200 mcg'ye kadar arttırılabilir.
Astımı yeterince kontrol altına alınamayan hastalar için doz günde iki kez 200 mikrograma kadar artırılarak ek bir fayda sağlanabilir.
Tedavi, hastalığın şiddetine uygun bir dozda başlatılmalıdır.
Doz daha sonra kontrol sağlanana kadar ayarlanabilir veya bireysel cevaba göre en düşük etkili doza düşürülebilir.
Bu dozun uygulanması için sadece 50 mcg basınçlı inhalasyon süspansiyonunun uygun olduğuna dikkat edilmelidir.
Basınçlı inhalasyon süspansiyonu, gerekli pediatrik dozun uygulanmasına izin vermeyebilir; eğer öyleyse, DISKUS inhaler yoluyla inhalasyon yoluyla toz flutikazon propiyonat vermeyi düşünün.
1 ila 4 yaş arası çocuklar
FLIXOTIDE - Solunum için basınçlı süspansiyon
100 mcg günde iki kez yüz maskesi ile donatılmış bir ayırıcı cihaz (pediatrik kullanım için ayırıcı cihaz) aracılığıyla uygulanır.
Flutikazon propiyonatın küçük çocuklara uygulanması, sık ve kalıcı astım semptomlarının kontrolünde faydalıdır ve yalnızca semptomlar günde bir kez beta agonist tedavisi ile yeterince kontrol altına alınamadığında endikedir.
Çocuklarda izin verilen maksimum doz günde iki kez 200 mcg'dir.
1-4 yaş arası çocuklarda yürütülen klinik çalışmalar, günde iki kez 100 mcg verilmesiyle astım semptomlarının optimal kontrolünün sağlandığını göstermiştir.Küçük çocukların daha büyük çocuklara göre daha yüksek dozlara ihtiyacı vardır. solunum yolları, spacer cihazı kullanma ihtiyacı ve nazal inhalasyon miktarındaki artış.
Astım tanı ve tedavisi sürekli izlenmelidir.
FLIXOTIDE - Solunum için toz
İnhalasyon tozu farmasötik formu 1 ila 4 yaş arası çocuklar için uygun değildir; Bu yaş grubundaki ilacın dozu ile ilgili olarak, FLIXOTIDE Basınçlı inhalasyon süspansiyonu bilgilerine bakınız.
04.3 Kontrendikasyonlar
Etkin maddeye veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık. Genellikle hamilelik ve emzirme döneminde kontrendikedir (bkz. bölüm 4.6).
04.4 Özel uyarılar ve uygun kullanım önlemleri
Astım tedavisi, normal olarak, hastalığın şiddetine göre uyarlanmış bir terapötik plan çerçevesinde gerçekleştirilmelidir; Hastanın tedaviye yanıtı hem klinik olarak hem de varsa solunum fonksiyon testleri ile doğrulanmalıdır.
Hızlı etkili inhale beta2-agonistlerin daha sık kullanılması ihtiyacı astım kontrolünün kötüleştiğini gösterir; bu durumda hastanın tedavi planı değiştirilmelidir.
Astımın ani ve ilerleyici alevlenmesi potansiyel olarak yaşamı tehdit eder ve kortikosteroid dozunun artırılmasına dikkat edilmelidir. Risk altında olduğu düşünülen hastalarda günlük pik akım takibi önerilir.
Özellikle uzun süreler için yüksek dozlarda reçete edildiğinde, inhale kortikosteroidlerle sistemik etkiler ortaya çıkabilir. Bu etkilerin ortaya çıkması, oral kortikosteroid tedavisine göre daha az olasıdır. Olası sistemik etkiler arasında Cushing sendromu, Cushingoid görünüm, adrenal baskılanma, çocuklarda ve ergenlerde büyüme geriliği, azalmış kemik mineral yoğunluğu, katarakt, glokom ve daha nadiren psikomotor hiperaktivite, irritabilite, uyku bozuklukları, anksiyete gibi bir dizi psikolojik veya davranışsal etki yer alır. , depresyon, saldırganlık veya davranış bozuklukları (özellikle çocuklarda). Bu nedenle, inhale kortikosteroid dozunun, astımın etkili kontrolünün sürdürüldüğü mümkün olan en düşük doz olması önemlidir.Önerilenden daha yüksek dozlara (yaklaşık 1000 mcg/gün) maruz kalan erkek çocuklarda çok nadir akut adrenal kriz vakaları olmuştur. Basınçlı süspansiyon veya diğer inhale kortikosteroidlerin veya diğer flutikazon propiyonat formlarının eşdeğer dozları ile inhalasyon yoluyla uzun süreli (birkaç ay veya yıl) uygulanır (bkz. bölüm 4.8).
Uzun süreli inhale kortikosteroid tedavisi alan çocukların boylarının düzenli olarak izlenmesi önerilir.
Bazı insanlar inhale kortikosteroidlerin etkilerine çoğu hastadan daha duyarlı olabilir.
Yetersiz adrenal yanıt olasılığı nedeniyle, daha önce oral steroidlerle tedavi edilen ve inhale flutikazon propiyonat tedavisine geçen hastalar özel bir dikkatle tedavi edilmeli, adrenal fonksiyon düzenli olarak izlenmeli, sistemik steroid tedavisinin kademeli olarak kesilmesi ve hastalara tavsiye edilmelidir. stres zamanlarında ek kortikosteroid tedavisi gerektirebileceklerini gösteren bir işaret taşımak.
Acil durumlarda (cerrahi müdahaleler dahil) ve ayrıca strese neden olabilecek elektif müdahalelerde yetersiz adrenal yanıt olasılığı, özellikle uzun süre yüksek doz alan hastalarda her zaman akılda tutulmalıdır. Klinik duruma uygun ek kortikosteroid tedavisi düşünülmelidir (bkz. bölüm 4.9).
Sistemik kortikosteroid tedavisinin inhalasyon tedavisi ile değiştirilmesi, daha önce sistemik ilaçlar tarafından maskelenen alerjik rinit veya egzama gibi alerjileri ortaya çıkarabilir.
Flutikazon propiyonat ile tedavi aniden kesilmemelidir.
Kan glukoz seviyelerinde çok nadir artış raporları olmuştur (bkz. bölüm 4.8) ve bu, diyabetes mellitus öyküsü olan hastalara ilaç reçete edilirken göz önünde bulundurulmalıdır.
Tüm inhale kortikosteroidlerde olduğu gibi, akciğer tüberkülozunun aktif veya uyku halindeki formları olan hastalarda özel bakım gereklidir.
Flutikazon propiyonat ve ritonavir ile tedavi edilen hastalarda, Cushing sendromu ve adrenal süpresyon dahil olmak üzere sistemik kortikosteroid etkilere neden olan, pazarlama sonrası kullanım sırasında klinik olarak anlamlı ilaç etkileşimleri vakaları bildirilmiştir. hastaya yararı, sistemik kortikosteroid yan etkilerinin ortaya çıkma riskinden daha ağır basarsa (bkz. bölüm 4.5).
Diğer inhale ilaçlarda olduğu gibi, ilacı aldıktan hemen sonra artan dispne ile paradoksal bronkospazm meydana gelebilir.Bu durumda, hemen hızlı etkili bir bronkodilatör alın, flutikazon propiyonat tedavisini hemen bırakın, hastayı yeniden değerlendirin ve gerekirse alternatif tedavi uygulayın (bkz. 4.8)
500 mcg flutikazon propiyonat alan KOAH hastaları üzerinde yapılan çalışmalarda pnömoni raporlarında artış olmuştur (bkz. bölüm 4.8).
FLIXOTIDE - Solunum için basınçlı süspansiyon
Basınçlı süspansiyon kullanılıyorsa, ilacın akciğerlere en uygun şekilde verilmesini sağlamak için inhalerin aktivasyonunun inspirasyonla senkronize olduğundan emin olmak için hastanın inhalasyon tekniği doğrulanmalıdır.
İlacın sistemik absorpsiyonu akciğer yoluyla gerçekleştiğinden, spacer kullanımı ilacın akciğerdeki konsantrasyonunu ve dolayısıyla sistemik advers reaksiyon riskini artırabilir.
FLIXOTIDE - Solunum için toz
Flixotide inhalasyon tozu laktoz içerir: Nadir kalıtsal galaktoz intoleransı, Lapp laktaz eksikliği veya glukoz-galaktoz malabsorpsiyonu sorunları olan hastalar bu tıbbi ürünü almamalıdır (ayrıca bkz. bölüm 4.5).
Laktoz eksipiyanı süt proteinleri içerdiğinden süt proteinlerine karşı intoleransı olan kişiler için uygun değildir.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Normal koşullar altında, geniş ilk geçiş metabolizması ve bağırsakta ve karaciğerde sitokrom P450 3A4'ün aracılık ettiği yüksek sistemik klirens nedeniyle inhale uygulamadan sonra flutikazon propiyonatın düşük plazma konsantrasyonları elde edilir.Bu nedenle etkileşimler olası değildir.flutikazon propiyonatın aracılık ettiği klinik olarak anlamlı ilaç.
Sağlıklı gönüllülerde yürütülen bir etkileşim çalışması, ritonavirin (çok güçlü bir sitokrom P450 3A4 inhibitörü) flutikazon propiyonatın plazma konsantrasyonlarını önemli ölçüde artırabildiğini ve bunun sonucunda serum kortizol konsantrasyonlarını önemli ölçüde düşürebildiğini göstermiştir. Pazarlama sonrası kullanım sırasında, intranazal veya inhale flutikazon propiyonat ve ritonavir ile tedavi edilen hastalarda, Cushing sendromu ve adrenal süpresyon dahil olmak üzere sistemik kortikosteroid etkilere neden olan klinik olarak anlamlı ilaç etkileşimleri vakaları bildirilmiştir.
Bu nedenle, hastaya sağlayacağı potansiyel yarar sistemik kortikosteroid yan etkilerinin risklerinden daha fazla olmadıkça flutikazon propiyonat ve ritonavirin birlikte kullanımından kaçınılmalıdır.
Çalışmalar, diğer sitokrom P450 3A4 inhibitörlerinin, flutikazon propiyonata sistemik maruziyette ihmal edilebilir (eritromisin) ve küçük (ketokonazol) artışlar ürettiğini ve serum kortizol konsantrasyonlarında kayda değer bir azalma olmadığını göstermiştir.Yine de, güçlü sitokrom P450 3A4 inhibitörleri (örn. ketokonazol) olduğunda dikkatli olunması önerilir. ) flutikazon propiyonata artan sistemik maruziyet potansiyeli bulunduğundan eşzamanlı olarak uygulanır.
04.6 Hamilelik ve emzirme
Gebelik
Gebe kadınlarda flutikazon propiyonat ile ilgili yeterli ve kontrollü çalışma bulunmamaktadır. Flutikazon propiyonatın kadınlarda gebelik üzerindeki etkisi bilinmemektedir Flutikazon propiyonatın olası üreme etkileşimini değerlendirmek için yapılan hayvan çalışmaları, yalnızca sistemik maruziyet düzeylerinde glukokortikoidlerin karakteristik etkilerini göstermiştir, önerilen terapötik dozda inhalasyon yoluyla gözlenmiştir Genotoksisite testler, molekülün mutajenik potansiyelini ortaya çıkarmadı.
Bununla birlikte, diğer ilaçlarda olduğu gibi, hamilelik sırasında flutikazon propiyonat uygulaması, yalnızca anneye beklenen yararın fetüse yönelik olası risklerden daha ağır basması durumunda düşünülmelidir.
Besleme zamanı
Flutikazon propiyonatın anne sütüne geçip geçmediği bilinmemektedir.
Sıçanlarda subkutan uygulamayı takiben, anne sütünde ölçülebilir plazma konsantrasyonlarında flutikazon propiyonat varlığı bulundu. Bununla birlikte, önerilen inhale dozlarda flutikazon propiyonat alan hastalarda plazma düzeylerinin düşük olması muhtemeldir.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
Flutikazon propiyonatın araç ve makine kullanma yeteneğini etkilemesi olası değildir.
04.8 İstenmeyen etkiler
Advers olaylar aşağıda organ, organ/sistem ve sıklığa göre listelenmiştir. Sıklıklar şu şekilde tanımlanmıştır: çok yaygın (≥1/10), yaygın (≥1/100 ila
Enfeksiyonlar ve istilalar
Çok yaygın: Ağız ve boğazda kandidiyazis
Bazı hastalarda orofaringeal kandidiyazis (pamukçuk) oluşabilir. Bu tür hastalar ilacı aldıktan sonra ağızlarını suyla çalkalamaktan fayda görebilirler Semptomatik kandidiyaz, flutikazon propiyonat kullanımını durdurmadan topikal antifungal tedavi ile tedavi edilebilir.
Yaygın: pnömoni (KOAH hastalarında)
Çok seyrek: Özofagus kandidiyazisi.
Bağışıklık sistemi bozuklukları
Aşağıdaki gibi ortaya çıkan aşırı duyarlılık reaksiyonları bildirilmiştir:
Yaygın olmayan: ciltte aşırı duyarlılık reaksiyonları
Çok seyrek: Anjiyoödem (esas olarak yüzde ve orofarenkste ödem), solunum semptomları (dispne ve/veya bronkospazm) ve anafilaktik reaksiyonlar.
endokrin patolojiler
Olası sistemik etkiler şunları içerir (bkz. bölüm 4.4):
Çok seyrek: Cushing sendromu, Cushingoid görünüm, adrenal supresyon, büyüme geriliği, kemik mineral yoğunluğunda azalma, katarakt, glokom.
bozukluklar metabolizma ve beslenme
Çok seyrek: hiperglisemi.
Psikolojik bozukluklar
Çok seyrek: Anksiyete, uyku bozuklukları ve psikomotor hiperaktivite ve sinirlilik dahil davranış bozuklukları (ağırlıklı olarak çocuklarda).
Bilinmiyor: Depresyon ve saldırganlık (ağırlıklı olarak çocuklarda).
Solunum patolojileri , torasik ve mediastinal
Yaygın: ses kısıklığı
Bazı hastalarda ses kısıklığı oluşabilir; bu durumlarda bile inhalasyondan hemen sonra ağzı suyla çalkalamak avantajlı olabilir.
Çok seyrek: paradoksal bronkospazm (bkz. bölüm 4.4).
Deri ve deri altı doku bozuklukları
Yaygın: morluklar
Şüpheli advers reaksiyonların raporlanması.
İlacın ruhsatlandırılmasından sonra meydana gelen şüpheli advers reaksiyonların raporlanması, tıbbi ürünün fayda/risk dengesinin sürekli olarak izlenmesine imkan verdiği için önemlidir. Sağlık profesyonellerinden şüpheli advers reaksiyonları ulusal raporlama sistemi aracılığıyla bildirmeleri istenir. "adres www. agenziafarmaco.gov.it/it/responsabili.
04.9 Doz aşımı
Belirtiler ve işaretler
İlacın önerilenden daha yüksek dozlarda akut inhalasyonu, hipotalamus-hipofiz-adrenal ekseninin geçici olarak baskılanmasına neden olabilir. Adrenal fonksiyon tipik olarak birkaç gün içinde normale döndüğünden, bu normalde acil müdahalelerin kurulmasını gerektirmez.
Onaylananlardan daha yüksek dozlar uzun süre kullanılırsa, önemli adrenal baskılanma meydana gelebilir. Adrenal rezervin izlenmesi gerekli olabilir.
Uzun süreli (birkaç ay veya yıl) önerilenden daha yüksek dozlara (tipik olarak 1000 mcg/gün ve üzeri) maruz kalan çocuklarda çok seyrek olarak akut adrenal kriz vakaları olmuştur; gözlemlenen belirtiler arasında hipoglisemi ve bilinç azalması ve/veya kasılmaların sekelleri yer alır).
Akut adrenal krizi potansiyel olarak tetikleyebilecek durumlar arasında travmaya, ameliyata, enfeksiyona veya dozajda herhangi bir hızlı azalmaya maruz kalma yer alır.
Tedavi
Onaylanandan daha yüksek dozlarla tedavi edilen hastalar yakından izlenmeli ve doz kademeli olarak azaltılmalıdır.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: aerosol - glukokortikoidler tarafından obstrüktif solunum yolu sendromları için diğer ilaçlar.
ATC kodu: R03BA05.
Hareket mekanizması
Önerilen dozlarda inhalasyon yoluyla uygulanan flutikazon propiyonat, akciğerlerde güçlü bir anti-inflamatuar aktivite uygulayarak astım alevlenmesi semptomlarını ve ataklarını azaltır.
05.2 Farmakokinetik özellikler
absorpsiyon
Flutikazon propiyonatın her bir inhalasyon regülatör tipi için mutlak biyoyararlanımı, inhale veya intravenöz uygulamayı takiben farmakokinetik verilerin karşılaştırmalı çalışmalarında ve karşılaştırmalı çalışmalarında değerlendirilmiştir Sağlıklı yetişkin deneklerde Diskus inhaler içinde inhalasyon için Flutikazon propiyonat tozunun mutlak biyoyararlanımı Sırasıyla (%7.8) ve flutikazon propiyonat inhalasyon basınçlı süspansiyonu (%10.9) değerlendirildi.Astımlı veya Kronik Obstrüktif Akciğer Hastalığı (KOAH) olan hastalarda, inhale flutikazon propiyonata daha düşük bir sistemik maruziyet seviyesi gözlendi.Sistemik emilim esas olarak akciğerlerde ve başlangıçta hızlıdır ve daha sonra uzar. Solunan dozun geri kalan kısmı yutulabilir, ancak düşük sulu çözünürlük ve sistem öncesi metabolizma nedeniyle sistemik maruziyete ihmal edilebilir derecede katkıda bulunur ve oral kullanılabilirliği %1'den azdır. Solunan dozdaki artışa bağlı olarak sistemik maruziyette doğrusal bir artış vardır.
Dağıtım
Flutikazon propiyonat, büyük bir kararlı durum dağılım hacmine sahiptir (yaklaşık 300 l). Plazma protein bağlanması orta derecede yüksektir (%91).
biyotransformasyon
Flutikazon propiyonat, esas olarak CYP3A4 enzim sisteminin sitokrom P450 tarafından inaktif bir karboksilik asit bileşiğine metabolize edilerek sistemik dolaşımdan çok hızlı bir şekilde temizlenir. Flutikazon propiyonata sistemik maruziyette artış potansiyeli bulunduğundan, CYP3A4 enzim sistemini inhibe ettiği bilinen ilaçlar uygulanırken dikkatli olunmalıdır.
Eliminasyon
Flutikazon propiyonatın eliminasyonu, "yüksek plazma klerensi (1150 ml/dak) ve" yaklaşık 8 saatlik bir terminal eliminasyon yarı ömrü ile karakterize edilir. Flutikazon propiyonatın renal klerensi ihmal edilebilir (%0.2'den az) ve 5'ten azdır. % metabolit olarak elimine edilir.
05.3 Klinik öncesi güvenlik verileri
Toksikolojik testler, terapötik kullanım için önerilenlerden daha yüksek dozlarda, yüksek potensli bir kortikosteroid için tipik olan tek etki sınıfını göstermiştir.
Kronik toksisite çalışmaları, üreme toksikolojisi ve teratojenez çalışmalarında olduğu gibi farklı nitelikteki etkileri vurgulamamıştır.
Flutikazon propiyonatın in vitro ve in vivo mutajenik olmadığı ve kemirgenlerde onkojenik olmadığı bulundu. Hayvan modellerinde flutikazon propiyonatın tahriş edici ve hassaslaştırıcı olmadığı bulunmuştur.
CFC olmayan itici gaz HFA 134a'nın, iki yıllık süreler boyunca itici gaza günlük olarak maruz kalan çok sayıda hayvan türünde, hastaların maruz kalacağından çok daha yüksek, çok yüksek buhar konsantrasyonlarında toksik etkilere neden olmadığı gösterilmiştir. .
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
İnhalasyon için basınçlı süspansiyon İtici HFA 134a
inhalasyon için toz
Laktoz (süt proteinleri içerir).
06.2 Uyumsuzluk
İlgili değil
06.3 Geçerlilik süresi
FLIXOTIDE - Solunum için basınçlı süspansiyon: 2 yıl.
FLIXOTIDE 100 mcg
İnhalasyon tozu: 2 yıl; FLIXOTIDE 250 mcg
İnhalasyon tozu, FLIXOTIDE 500 mcg
İnhalasyon tozu: 3 yıl.
06.4 Depolama için özel önlemler
Solunum için basınçlı süspansiyon
Klik sesini duyana kadar inhaler kapağını sıkıca yerine takın.
Paketler güneş ışığından uzak tutulmalı ve donmaya karşı korunmalıdır.
Çoğu basınçlı dozlu aerosol ilaçta olduğu gibi, basınçlı kap soğuksa terapötik etki daha az olabilir.
Basınçlı kaplar, görünüşte boş olsalar bile kırılmamalı, delinmemeli veya yakılmamalıdır.
inhalasyon için toz
Kuru bir yerde saklayın.
İlacı nemden korumak için orijinal ambalajında saklayınız.
DISKUS, yalnızca tıbbi ürün ilk kez kullanıldığında açılması gereken koruyucu bir laminat örtü ile kapatılmıştır. Koruyucu laminat zarf açıldıktan sonra atılmalıdır.
06.5 İç ambalajın yapısı ve paketin içeriği
Ölçüm valfi ve ilgili inhaler ile alüminyum basınçlı kap içeren kartonlar.
FLIXOTIDE 125 mcg - Solunum için basınçlı süspansiyon
- her biri 125 mcg'lik 120 puf içeren basınçlı kap
FLIXOTIDE 250 mcg - Solunum için basınçlı süspansiyon
- her biri 250 mcg'lik 120 puf içeren basınçlı kap
FLIXOTIDE 50 mcg - Solunum için basınçlı süspansiyon
- her biri 50 mcg'lik 120 sprey içeren basınçlı kap
Kalıplanmış plastik malzemeden (DISKUS) çok dozlu inhalatörler, her biri içinde düzenli aralıklarla ayrı ayrı alveollerin ("kabarcık") düzenlendiği bir şerit şerit içeren, her biri bir doz (100 - 250 - 500 mcg) flutikazon dispersiyonlu inhalasyon tozu içeren laktoz içinde.
FLIXOTIDE 250 mcg - 60 doz 250 mcg şeritli DISKUS inhaler içinde inhalasyon için toz
FLIXOTIDE 500 mcg - 60 doz 500 mcg şeritli DISKUS inhaler içinde inhalasyon için toz
FLIXOTIDE 100 mcg - 60 dozluk 100 mcg şeritli DISKUS inhaler içinde inhalasyon için toz
06.6 Kullanım ve kullanım talimatları
FLIXOTIDE - Solunum için basınçlı süspansiyon
Solunum cihazının çalışmasını kontrol edin
İnhaleri ilk kez kullanmadan önce veya bir hafta boyunca kullanılmadığında, koruyucu kapağı kenarlarından hafifçe sıkarak ağızlıktan çıkarın, inhaleri kuvvetlice sallayın ve ardından emin olmak için havaya bir doz püskürtün. işe yarıyor.
inhalerin kullanımı
1. Koruyucu kapağı kenarlardan hafifçe sıkarak ağızlıktan çıkarın.
2. Ağızlık dahil olmak üzere inhalerin içini ve dışını yabancı cisimler açısından kontrol edin.
3. Herhangi bir yabancı maddenin temizlendiğinden ve inhalerin içeriğinin eşit şekilde karıştırıldığından emin olmak için inhaleri kuvvetlice sallayın.
4. İnhaleri başparmağınız ve işaret parmağınızla bastırmadan tutun (işaret parmağınız basınçlı kabın dibinde durmalıdır).
5. Tam olarak nefes alın, ardından ağızlığı ısırmaktan kaçınarak dudaklarınızın arasına sıkıca yerleştirin.
6. Ardından derin bir nefes alın ve derin nefes almaya devam ederken işaret parmağınızla kabın dibine bir kez basınç altında bastırın.İnhaleri çalıştırmadan hemen önce inhalasyonun yavaşça başlatılması önemlidir.
7. Mümkün olduğu kadar uzun süre nefesinizi tutun, ağızlığı çıkarın ve yavaşça nefes verin.
8. Bir sonraki inhalasyon gerekiyorsa en az yarım dakika bekleyin, ardından 3 ila 7 arasındaki adımları tekrarlayın.
9. Koruyucu kapağı tekrar ağızlığa takın ve tık sesi duyana kadar bastırın.
Önemli: 5, 6 ve 7. maddelerde belirtilen işlemleri aceleyle yapmayın. Nebulize materyalin inhalerin üstünden veya ağzın kenarlarından salınması, inhalasyonun doğru yapılmadığını gösterir; ardından işlemleri 2. noktadan itibaren tekrarlayın.
Doktorunuz inhaleri nasıl kullanacağınız konusunda size farklı bilgiler veriyorsa bunları dikkatli bir şekilde takip etmelisiniz. Doktora herhangi bir zorluk hakkında bilgi vermeniz de tavsiye edilir.
Solunum cihazının temizlenmesi
İnhaler haftada en az bir kez temizlenmelidir.
1. Basınçlı kabı inhalerden çıkarın ve koruyucu kapağı ağızlıktan çıkarın.
2. İnhaleri ve ağızlık koruyucu kapağını nemli bir bezle temizleyin.
3. Sıcak bir yerde kurumaya bırakın. Aşırı ısıdan kaçının.
4. Basınçlı kutuyu inhalere ve koruyucu kapağı tekrar ağızlığa yerleştirin.
Kabı BASINÇ ALTINDA SUYA BATIRMAYIN
FLIXOTIDE - DISKUS inhaler içinde inhalasyon tozu
DİSK BİLGİLERİ
DISKUS, kutudan çıkarıldığında "kapalı" konumdadır.
DISKUS, bireysel olarak korunan 60 doz ilaç tozu içerir.
Her doz dikkatle ölçülür ve hijyenik olarak korunur. DISKUS bakım gerektirmez ve şarj edilemez.
DISKUS'un üst kısmındaki doz göstergesi, halen mevcut olan dozların sayısını gösterir.
5'ten 0'a kadar olan sayılar, yalnızca birkaç doz kaldığını belirtmek için KIRMIZI renktedir. DISKUS'un kullanımı kolaydır.
İlacın bir dozunu almak için aşağıdaki dört basit adımı izleyin:
1. Açılış
2. Dozun hazırlanması
3. Soluma
4. Kapanış
DİSK NASIL ÇALIŞIR
DİSKUS'un kolu kaydırılarak ağızlıkta küçük bir delik açılır ve inhalasyona hazır bir doz hazırlanır. DISKUS kapatıldığında, kol otomatik olarak orijinal konumuna döner ve bir sonraki ilaç dozunu hazırlamaya hazırdır.
Dış kapak kullanılmadığında DISKUS'u korur.
1. Açılış
DISKUS'u açmak için bir elinizle dış kısmından tutun ve diğer elin başparmağını girintiye yerleştirin. Bir klik sesi duyana kadar cihazın içini döndürürken baş parmağınızla itin.
2. Dozun hazırlanması
DISKUS'u ağızlık kullanıcıya bakacak şekilde tutun.Kolu tık sesi gelene kadar ileri kaydırın.DISKUS artık kullanıma hazırdır.
Kol her kaydırıldığında, doz göstergesinde gösterildiği gibi inhalasyon için bir doz hazır hale gelir.
Kolu, dozları boşa harcamamak için yalnızca ilacı solumanız gerektiğinde kullanın.
3. Soluma
Teneffüs etmeden önce bu bölümü dikkatlice okuyun.
DISKUS'u ağzınızdan uzak tutun. Mümkün olduğunca derin nefes verin. DISKUS'a asla üflemeyin.
Ağızlığı dudaklarınızın arasına koyun.
Burundan değil, DISKUS'tan derin ve düzenli bir şekilde nefes alın. DISKUS'u ağzınızdan çıkarın.
Nefesinizi yaklaşık 10 saniye veya mümkün olduğunca uzun süre tutun.
Yavaşça nefes verin.
4. Kapanış
DISKUS'u kapatmak için başparmağınızı girintiye yerleştirin ve gidebildiği kadar geriye doğru kaydırın.
DISKUS kapatıldığında keskin bir kapanma sesi çıkarır. Bu, kolu otomatik olarak orijinal konumuna döndürür.
DISKUS artık tekrar kullanılmaya hazırdır.
İki inhalasyon reçete edilmişse, ilk inhalasyondan sonra DISKUS'u kapatmak ve ardından 1 ila 4 arasındaki adımları tekrarlamak gerekir.
DİKKAT
DISKUS'u kuru tutun.
Kullanılmadığı zaman DISKUS'u kapalı tutun. DISKUS'a asla üflemeyin.
Kolu yalnızca ilacı almaya hazır olduğunuzda kaydırın. DISKUS'tan sadece ağzınızla nefes alın.
Önerilen dozu aşmayınız.
07.0 PAZARLAMA YETKİ SAHİBİ
GlaxoSmithKline S.p.A. - Via A. Fleming, 2 - Verona
08.0 PAZARLAMA YETKİ NUMARASI
Solunum için basınçlı süspansiyon
FLIXOTIDE 125 mcg 120 puf 125 mcg A.I.C.: 028667095
FLIXOTIDE 250 mcg 120 ponpon 250 mcg A.I.C.: 028667107
FLIXOTIDE 50 mcg 120 puf 50 mcg A.I.C.: 028667020
FLIXOTIDE 250 mcg - 60 doz 250 mcg A.I.C.'lik şeritler ile DISKUS inhaler içinde inhalasyon için toz.: 028667184
FLIXOTIDE 500 mcg - 60 doz 500 mcg A.I.C.'lik şeritler içeren DISKUS inhaler içinde inhalasyon için toz.: 028667208
FLIXOTIDE 100 mcg - 60 dozluk 100 mcg A.I.C. şeritli DISKUS inhaler içinde inhalasyon için toz.: 028667160
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
27 Nisan 1993 / Şubat 2008